
17、(12分)I、(1)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵,则①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。 (2)已知某温度下,纯水中的C(H+)=5×10-7mol/L,则此时溶液的C(OH-)为 mol/L;若温度不变,将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
II、在一个容积固定的密闭容器中,要求通过调节体系的温度使反应A(g)+2B(g) 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
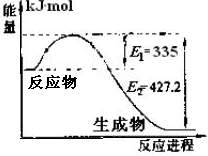
⑴若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应是 热反应。
⑵欲使反应维持向逆反应方向移动,则x的取值范围为 。
 ⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g)
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g) 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用
m、n表示;设A、B、C和D、E、F之间均不发生反应)。
16、常温下,下列各组数据中比值为2:1的是:
A.电解熔融氯化钠,在阴极和阳极上析出产物的物质的量之比 B.中和体积相同、pH相同的硫酸和盐酸消耗NaOH的物质的量之比 C.1 mol·L-1氨水溶液与0.5 mol·L-1氨水溶液中c(OH-)之比 D.等物质的量浓度(NH4)2SO4和NH4Cl的C(NH4+)之比
第Ⅱ卷(共52分)
15、下列有关结论中,正确的是: A.在所有能够溶解Al(OH)3的溶液中,Cu2+、ClO-、Cl-、Ca2+一定能够大量共存
B.常温时将pH=3的CH3COOH溶液与pH=13的NaOH溶液等体积混合后溶液pH=7
C.常温下,在25 mL 0.1 mol·L﹣1 NaOH溶液中逐滴加入amL 0.2 mol·L﹣1CH3COOH溶液,当c(CH3COO-)>c(Na+)时,a一定大于12.5
D.在相同条件下,将足量AgCl加入等体积的①0.01 mol·L-1 KCl②0.1 mol·L-1 KCl溶液③蒸馏水三种液体中,所能溶解的AgCl质量关系为:①>②>③
14、下列溶液中各微粒的浓度关系正确的是:
A.pH=x的氨水与pH=y的盐酸等体积混合所得溶液中(已知x+y=14):
C(Cl_) > C(NH4+) > C(H+) > C(OH_)
B.0.1mol/LKHC2O4溶液中:C(K+)+C(H+)=C(HC2O4_)+C(OH_)+C(C2O42_)
C.1L0.1mol/LCuSO4·(NH4)2SO4·6H2O的溶液中:
C(SO42_) >C(NH4+) >C(Cu2+) >C(H+) >C(OH_)
D.0.1mol/LNa2HPO4的溶液中:C(OH_)=C(H+)+C(H2PO4_)+2C(H3PO4)
13、CO2和H2的混合气体加热到850℃时,建立下列平衡:CO2(g)+H2(g)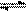 CO(g)+H2O(g)在一定温度下,反应平衡时有80%的氢气变成水,且c(CO2)×c(H2)=c(CO)×c(H2O),则原混合气体中CO2和H2分子数之比是:
CO(g)+H2O(g)在一定温度下,反应平衡时有80%的氢气变成水,且c(CO2)×c(H2)=c(CO)×c(H2O),则原混合气体中CO2和H2分子数之比是:
A.1:1 B. 4:1 C. 5:1 D.1:4
12、已知可逆反应2NO2(g)
 N2O4(g);△H<0;若初始温度相同,分别将等量的NO2气体置于编号为a、b、c的三个体积相同的密闭容器中,且已知a容器绝热恒容、b容器恒温恒容、c容器恒温恒压,则达到平衡后有关三个容器中气体颜色深浅的叙述中正确的是:
N2O4(g);△H<0;若初始温度相同,分别将等量的NO2气体置于编号为a、b、c的三个体积相同的密闭容器中,且已知a容器绝热恒容、b容器恒温恒容、c容器恒温恒压,则达到平衡后有关三个容器中气体颜色深浅的叙述中正确的是:
A. a容器颜色比b容器的深 B. b容器颜色比c容器的深
C. 题中条件无法确定哪个容器颜色最浅 D.三个容器种颜色一样
11、在一定条件下,已达平衡的可逆反应:2A(g)+B(g) 2C(g),下列说法中正确的是:
2C(g),下列说法中正确的是:
A.平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=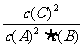
B.改变条件后,该反应的平衡常数K一定不变
C.如果改变压强并加入催化剂,平衡常数会随之变化
D.若平衡时增加A和B的浓度,则平衡常数会减小
10、用已知物质的量浓度的盐酸滴定未知物质的量浓度的NaOH溶液(酚酞作指示剂)。下列情况会使测定结果偏低的是: A.酸式滴定管用水洗后便装液体进行滴定 B.锥形瓶用蒸馏水洗涤后,又用待测液润洗
C.滴定前,酸式滴定管有气泡,滴定后消失 D.记录起始体积时,仰视读数,终点时俯视
9、a、b、c、d、e分别为MgC12、KHSO4、KOH、NaHCO3、A1C13溶液中的一种,已知:①a能与其他4种溶液反应,且a与c、e反应时有明显现象;②b与d反应只产生气泡;③e只能与a反应;下列推理不正确的是:
A.a一定是KOH B.c一定是A1C13 C.e一定是MgC12 D.b一定是KHSO4
8、某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是: A.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 B.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 C.加入适量的NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com