
7ЁЂФме§ШЗБэЪОЯТСаЗДгІЕФРызгЗНГЬЪНЪЧ(ЁЁ )
AЃЎАБЫЎжаЭЈШыЙ§СПCO2ЃК2NH3ЁЄH2O + CO2 = 2NH4+ + CO32- + H2O
BЃЎТШЛЏбЧЬњШмвКжаМгШыЯѕЫсЃКFe2+ + 4H+ + NO3- = Fe3+ + 2H2O + NOЁќ
CЃЎНЋБъзМзДПіЯТ112 mLТШЦјЭЈШы10 mL 1 molЁЄLЃ1ЕФфхЛЏбЧЬњШмвКжаЃК
2Fe2+ + 4BrЃ+ 3Cl2 ЃН 2Fe3+ + 6ClЃ + 2Br2
DЃЎдкЬМЫсЧтИЦШмвКжаМгШыЙ§СППСадМиШмвКЃКCa2++HCO3Ѓ+OHЃ=CaCO3Ё§+H2O
6ЁЂЪвЮТЯТЃЌЯТСаЛьКЯШмвКжаЃЌИїРызгХЈЖШЕФЙиЯЕе§ШЗЕФЪЧ
AЃЎPH = 12ЕФАБЫЎШмвКгыpH=2ЕФбЮЫсШмвКЕШЬхЛ§ЛьКЯc(NH4+)ЃОc(ClЃ)ЃОc(OHЃ)ЃОc(H+)
BЃЎХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФСђЫсЧтяЇШмвКгыЧтбѕЛЏФЦШмвКЕШЬхЛ§ЛьКЯ
c(Na+)ЃОc(SO42Ѓ)ЃОc(NH4+)ЃОc(H+)ЃОc(OHЃ)
CЃЎХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФаЁЫеДђШмвКгыЩеМюШмвКЕШЬхЛ§ЛьКЯ
c(Na+)+c(H+)ЃН2c(CO32Ѓ)+c(OHЃ)
DЃЎХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФДзЫсШмвКгыЧтбѕЛЏФЦШмвКЕШЬхЛ§ЛьКЯ
ЁЁc(Na+)ЃНc(CH3COOЃ)ЃОc(OHЃ)ЃНc(H+)
5ЁЂгУCH4ДпЛЏЛЙдNOxПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЁЃР§ШчЃК
Ђй CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) ЁЁЁЁЁїH ЃН-574 kJЁЄmol-1
Ђк CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)ЁЁ ЁЁЁЁЁїH ЃН-1160 kJЁЄmol-1
ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
AЃЎгЩЗДгІЂйПЩЭЦжЊЃКCH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(l) ЁїH <-574 kJЁЄmol-1
BЃЎЗДгІЂйЂкзЊвЦЕФЕчзгЪ§ЯрЭЌ
CЃЎ0.2mol ЁЁCH4 ЛЙд NO2жС N2ЃЌЗХГіЕФШШСПЮЊ 173.4 kJ
DЃЎШєгУБъзМзДПіЯТ4.48 L CH4 ЛЙд NO2жС N2ЃЌећИіЙ§ГЬжазЊвЦЕФЕчзгзмЪ§ЮЊ1.60 mol
4ЁЂАЂЗќМгЕТТоГЃЪ§дМЮЊ6.02ЁС1023 mol-1ЁЃЯТСаа№Ъіжае§ШЗЕФЪЧ
ЁЁЁЁЁЁ AЃЎ32 gКЌгаЩйСПГєбѕЕФбѕЦјжаЃЌЙВКЌгабѕдзгЪ§ЮЊ2ЁС6.02ЁС1023
ЁЁЁЁЁЁ BЃЎБъзМзДПіЯТЃЌ11.2 LЫФТШЛЏЬМКЌгаЕФЗжзгЪ§ЮЊ0.5ЁС602ЁС1023
ЁЁЁЁЁЁ CЃЎ5.6 gЬњЗлЭъШЋШмгкЯѕЫсЃЌЪЇШЅЕФЕчзгЪ§вЛЖЈЮЊ0.3ЁС6.02ЁС1023
DЃЎ1 L0.5 mol/L Na2CO3 ШмвКжаКЌгаЕФCO32ЃЪ§ФПЮЊ0.5ЁС6.02ЁС1023
3ЁЂЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЃЎ16O2гы18O2ЛЅЮЊЭЌЮЛЫиЃЌH2OЁЂD2OЁЂT2OЛЅЮЊЭЌЫивьаЮЬхЃЌN60КЭN2ЛЅЮЊЭЌЯЕЮя
BЃЎГ§ЯЁгаЦјЬхЭтЕФЗЧН№ЪєдЊЫиЖМФмЩњГЩВЛЭЌМлЬЌЕФКЌбѕЫс
CЃЎЗЧН№ЪєдЊЫиRЫљаЮГЩЕФКЌбѕЫсбЮ(MaROb)жаЕФRдЊЫиБиЖЈГЪЯже§Мл
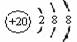 DЃЎCaЕФдзгНсЙЙЪОвтЭМЮЊЁЁ
DЃЎCaЕФдзгНсЙЙЪОвтЭМЮЊЁЁ
2ЁЂЯТСаЪЕбщВйзїжаЃЌвЧЦїашВхШывКУцЯТЕФгаЃКЂйжЦБИFe(OH)2ЃЌгУНКЭЗЕЮЙмНЋNaOHШмвК
ЕЮШыFeSO4ШмвКжаЃЛЂкжЦБИЧтЦјЃЌМђвззАжУжаГЄОБТЉЖЗЕФЯТЖЫЙмПкЃЛЂлЗжСѓЪЏгЭЪБВтСПЮТЖШЫљгУЕФЮТЖШМЦЃЛЂмгУввДМжЦБИввЯЉЪБЫљгУЕФЮТЖШМЦЃЛЂнгУЫЎЮќЪеАБЦјЪБЕФЕМЦјЙмЃЛЂоЯђЪдЙмжаЕФBaCl2ШмвКЕЮМгЯЁСђЫс
ЁЁ ЁЁЁЁ AЃЎЂлЂнЂоЁЁ ЁЁЁЁ ЁЁ BЃЎЂкЂнЁЁЁЁЁЁЁЁ CЃЎЂйЂкЂмЁЁ ЁЁЁЁ DЃЎЂйЂкЂлЂмЂнЂо
1ЁЂЯТСаа№Ъіе§ШЗЕФЪЧ
AЃЎЖўбѕЛЏЙшЪЧШЫРрНЋЬЋбєФмзЊЛЛЮЊЕчФмЕФГЃгУВФСЯ
BЃЎЖўбѕЛЏСђдкНгДЅЪвБЛбѕЛЏГЩШ§бѕЛЏСђЃЌдкЮќЪеЫўФкгУЫЎЮќЪежЦГЩХЈСђЫс
CЃЎЮЊМьбщЫсадШмвКжаЕФClЃКЭSO42ЃЃЌЯШМгBaCl2ШмвКЃЌТЫШЅГСЕэКѓдйМгAgNO3ШмвК
DЃЎЗжЩЂЯЕжаЗжЩЂжЪСЃзгЕФжБОЖЃКFe(OH)3аќзЧвКЃОFe(OH)3НКЬхЃОFeCl3ШмвК
|
23ЃЎЧывдЁАЩњУќжаЕФФЧеЕЕЦЁБЮЊЬтЃЌаДвЛЦЊЮФеТЁЃГ§ЪЋИшЭтЮФЬхВЛЯоЃЌЮФЬхЬиеїЯЪУїЃЌВЛЩйгк800зжЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com