
2、下列实验操作中正确的是
A 从试剂瓶中取出的任何药品,若有剩余不能放回原瓶B 可燃性气体点燃之前必须验纯
C 用胶头滴管向试管中加液体,一定要将滴管伸入试管中
D如果没有试管夹,可以临时手持试管给固体或液体加热
1、下列实验操作中正确的是
A 将氢氧化钠固体放在滤纸上称量 B 用10mL量筒量取8.58mL蒸馏水
C 制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
35.(现代生物科技专题,15分)我国首例绿色荧光蛋白转基因克隆猪在东北农业大学的种猪场自然分娩产出,这标志着我国在转基因克隆猪技术领域已达到世界领先水平。下图为我国首例绿色荧光蛋白转基因克隆猪的培育过程示意图,请据图回答:

(1)过程①和②必需用到的酶分别是 。
(2)重组质粒除了带有绿色荧光蛋白基因以外,还必须含有 、
和 _才能构成一个完整的基因表达载体。
(3)过程③将重组质粒导入猪胎儿成纤维细胞时,采用最多也最有效的方法是
。然后还要通过 技术来检测绿色荧光蛋白基因是否已重组到猪胎儿成纤维细胞的染色体DNA上。
(4)为了获得更多的猪卵母细胞,可通过对母猪注射_______________________,做超数排卵处理,并将所采集到的卵母细胞在体外培养到 期即可通过显微操作将其细胞核去除。
(5)早期胚胎的培养液成分较复杂,除一些无机盐和有机盐类外,还需添加维生素、激素、__________________________________等物质。
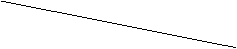
33.(8分)某生物兴趣小组开展多种环境因素对植物光合作用影响的探究活动。下表为实验测得的数据,其中 A 组为黑暗条件下马铃薯呼吸速率随温度变化的数据, B 、 C 、 D 、 E 为不同光照强度和不同 CO2 浓度下,马铃薯吸收( + )或释放(一)速率( mg/h)随温度变化的数据。请分析回答:
  温度℃ 温度℃数据(mg/h) 组别、条件 |
10℃ |
20℃ |
30℃ |
35℃ |
40℃ |
45℃ |
|
|
A |
黑暗 |
-5 |
-10 |
-18 |
-34 |
-40 |
-34 |
|
B |
弱光,CO2浓度为0.03% |
2 |
0 |
-8 |
-24 |
-33 |
-29 |
|
C |
适当遮荫,CO2浓度为0.03% |
3 |
5 |
0 |
-16 |
-24 |
-24 |
|
D |
全光照,CO2浓度为0.03% |
5 |
8 |
4 |
2 |
0 |
-14 |
|
E |
全光照,CO2浓度为1.22% |
10 |
20 |
40 |
28 |
12 |
0 |
(1)由表可知影响植物光合作用速率的因素有 。
(2)根据实验数据分析,实验中欲使马铃薯光合速率达到最强,所需的一组条件是 。
(3)欲使大棚中马铃薯长势最佳,所需的一组条件是 。
(4)甲、乙、丙三图分别表示几个环境因素对马铃薯光合作用速率的影响,除各图中的所示因素外,其他因素均控制在较适宜的范围。请据图回答以下问题:
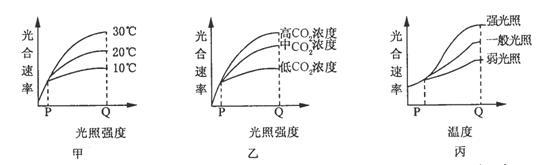
甲图 P 点,限制马铃薯光合作用速率的因素为 ;乙图 Q 点,高CO2浓度条件下,若要进一步提高马铃薯光合作用速率,可尝试采取的措施是 ;预计丙图 Q 点之后三条曲线的走势为 。

 34.(12分)赤霉素广泛存在于高等植物体内,它可以通过提高生长素(吲哚乙酸)含量间接促进植物生长。那么它是如何提高生长素含量的呢?某研究小组开展了探究。生长素在植物体内有一个合成和分解的代谢过程(如图1,IAA氧化酶是一种含铁蛋白)。研究小组据此提出假设:赤霉素通过促进生长素的合成提高生长素含量。
34.(12分)赤霉素广泛存在于高等植物体内,它可以通过提高生长素(吲哚乙酸)含量间接促进植物生长。那么它是如何提高生长素含量的呢?某研究小组开展了探究。生长素在植物体内有一个合成和分解的代谢过程(如图1,IAA氧化酶是一种含铁蛋白)。研究小组据此提出假设:赤霉素通过促进生长素的合成提高生长素含量。
图一 图二
为验证假设,研究小组设计了实验。材料用具包括燕麦幼苗,完全培养液、缺铁培养液、赤霉素溶液(以上溶液浓度均适宜),蒸馏水、琼脂块、刀片等。
(1)参考图2,补充完成以下实验步骤:
① 准备四个配有培养支架的烧杯,分别标记为1-4号。
② 向1号和2号烧杯中加入等量适量的完全培养液。
③ _________________,分别在1号和2号烧杯中培养一段时间。
④ 1号幼苗喷洒适量蒸馏水,2号幼苗喷洒等量赤霉素溶液。继续培养一段时间。
⑤ 。培养一段时间后,观察胚芽鞘的弯曲情况。
⑥ 向3号和4号烧杯中加入等量适量的缺铁培养液, 。
(2)实验分析:
步骤②→⑤的处理结果是去尖胚芽鞘弯向1号,这证明 。步骤⑥可能出现 种不同的实验结果。
(3)该研究小组只提出了一种假设,请你提出可能存在的其他假设。
32.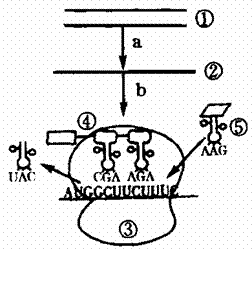 (每空1分,共7分)右图所示,为某基因表达的过程,据图回答:
(每空1分,共7分)右图所示,为某基因表达的过程,据图回答:
(1)能够将遗传信息从细胞核传递至细胞质的是_____(填数字),其基本组成单位是_______________。进行a过程所需的酶有______________________。
(2)图中含有五碳糖的物质有__________(填标号);图中⑤所运载的氨基酸是_______________。(密码子:AUG一甲硫氨酸、GCU一丙氨酸、AAG一赖氨酸、UUC一苯丙氨酸)
(3)图中信使RNA对应的DNA片段连续复制两次共需要游离的胸腺嘧啶脱氧核苷酸的数目为__________________个。
(4)若在图中AUG之后插入一个或两个核苷酸,则合成的多肽链中除第一个氨基酸不变外,其余氨基酸的排列顺序都发生了变化,而在AUG之后插入三个核苷酸时,合成的多肽链中除在甲硫氨酸后多一个氨基酸外,其余氨基酸的排列顺序没有发生变化,由此可以得出的结论是________________________。
[答案](1)② 核糖核苷酸 解旋酶、RNA聚合酶(写全才给分) (2)①②⑤(写全才给分) 苯丙氨酸 (3)18 (4)一个密码子由3个碱基(或核糖核苷酸)组成。
31.(12分)某年夏天,太湖爆发蓝藻灾害,导致水质严重恶化,无锡市因此出现饮用水荒。“无锡太湖蓝藻的爆发,既有自然因素,也有人为因素。”国家环保总局官员在新闻发布会上如是说。从自然因素上来讲,太湖水位出现50年以来最低值,水少;另外,4月无锡气温都在20℃左右,适合蓝藻生长。但是,人为因素也非常重要,上游河流污染物排放严重,太湖湖水中的氮、磷浓度升高,造成水体富营养化。
(1)水位低是太湖蓝藻爆发的原因之一,从本质上来看这是降低了太湖生态系统的 。
(2)为了防止太湖水源被污染,环保部门加强对太湖上游流域沿岸工厂的监测,现怀疑某工厂是污染源之一,并对其排污口进行了检测。检测人员沿河每隔100米取水样一次,共取9份并依次编号为①一⑨,已知⑤号水样正对工厂排水口。检验人员对所取水样进行了如下处理:I 检测水样中的蓝藻数量(A组);Ⅱ 滤除水样中全部蓝藻,每份水样分为三等份,编号B、C、D,其中B、C组分别添加适量的N和P,D组不添无机盐。然后加入等量的蓝藻,放置在阳光下若干天,再检测水样中蓝藻数量,统计数据如下表(蓝藻数量,单位:百万细胞/mm3),请回答有关问题:
|
水样编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|
A组(原始水样) |
0.2 |
0.3 |
0.3 |
l |
10 |
10 |
7 |
7 |
6.5 |
|
B组(添加N) |
1 |
1.5 |
2 |
2.5 |
20 |
19 |
18 |
17 |
18 |
|
C组(添加P) |
8 |
9 |
9.5 |
10 |
11 |
9.5 |
7.5 |
7.5 |
7 |
|
D组(无添加) |
0.2 |
0.2 |
0.3 |
l |
10 |
9 |
7 |
7 |
6.5 |
①通过A组数据可以判断工厂是污染源,依据是 。
②进行B、C、D分组实验的目的是探究工厂排出的污染物主要是N含量超标还是P含量超标,其中D组起 作用。实验结果显示,工厂上游水域限制蓝藻增长的主要因素分别是 和 ,由此得出的结论是 。
30. (14分)相对分子质量为94.5的有机物A,在一定条件下可以发生如下图所示的转化(其他产物和水已略去);

请回答下列问题:
(1)写出下列物质的结构简式:A , J 。
(2)上述①-⑨的反应中, 是取代反应(填编号), 是消去反应(填编号)。
(3)写出下列反应的化学方程式:
B→C 。
B→E 。
(4)有机物I在一定条件下可合成一种环保开支高分子材料,则该高分子结构简式为 。
(1)A:CH3-CH-CH2OH J: (2)⑤ ⑨;③ ④

 (3)CH3-CH-CHO+2Cu(OH)2 CH3-CH-COOH+Cu2O+2H2O
(3)CH3-CH-CHO+2Cu(OH)2 CH3-CH-COOH+Cu2O+2H2O

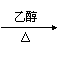
 CH3-CH-CHO+NaOH CH2=CH-CHO+NaCl+H2O
CH3-CH-CHO+NaOH CH2=CH-CHO+NaCl+H2O

(4)[ O-CH- C ]n
29.(15分)某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与过程探究。
(1)实验式的确定
①取样品A进行燃烧法测定。发现燃烧后只生成 ,某次燃烧后,经换算得到了
,某次燃烧后,经换算得到了 。据此得出的结论是_____ ___________________。
。据此得出的结论是_____ ___________________。
②另一实验中,取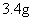 蜡状A在
蜡状A在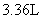 (标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成
(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成 和液态水。
和液态水。
由此得出的实验式是_____________________。
(2)结构式确定(经测定A的相对分子质量为136)
③取少量样品熔化,加入钠有氢气放出,说明A分子中含有________基。
④进行核磁共振,发现只有两个特征峰,且面积比为8:4,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:

则A的结构简式为______________________。
(3)性质探究
⑤A的四乙酸酯在稀硫酸催化下在 中发生水解的化学方程式(产物中注明
中发生水解的化学方程式(产物中注明 )为___________________________________。
)为___________________________________。
答案:①分子中 ,分子式为
,分子式为
② ③羟基 ④C(CH2OH)4
③羟基 ④C(CH2OH)4
⑤
28.(14分)研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+1价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、 、 (填字母)。
A.A1Cl3溶液 B.NaOH溶液 C.稀H2SO4 D.H2O2溶液
假若Cu(OH)2具有两性,应该看到的实验现象是 。
(2)为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98gCu(OH)2固体,加热至800C~1000C时,得到黑色固体粉末,继续加热到10000C以上,黑色粉末全部变成红色粉末X。冷却后称量,X的质量为72g。向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。据此可推得,X的化学式为 ,可以得出的结论是
、
(3)为解决问题③,设计了如下的实验装置(夹持及尾气处理装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体。装置A的作用是 ,B中发生反应的化学方程式为 。

解析(1)B C (各1分) Cu(OH)2既能溶于稀硫酸,又能溶于NaOH溶液(2分)
(2) Cu2O(2分) 高于1000℃时Cu2O比CuO稳定(2分) 在溶液中Cu2+比Cu+稳定(2分)
(3)干燥NH3(2分) 3CuO+2NH3===3Cu+N2+3H2O
27.(15分)有A、B、C、D、E、F、G七种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的元素。
(1)A的名称是____________,B位于周期表中第_________周期________族,C的原子结构示意图是________________。
(2)E的单质颜色是____________________。
(3)A元素与D元素形成化合物的电子式是__________________。
(4)G的单质与水反应的化学方程式是______________________________。
(5)F的元素符号是_____________________。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是_________,酸性最强的化学式是_______________,气态氢化物最稳定的化学式是______________。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是:___________________________________________。
答案(1)钠 3 ⅡA 
 (2)紫黑色(3)(2分)
(2)紫黑色(3)(2分)
(4)(2分)2F2+2H2O =4HF+O2(5)He (6)NaOH HBrO4 HF
(7)(2分)Al(OH)3+OH- =AlO2-+2H2O
解析:此题是根据原子结构,元素周期表的知识,结合相关已知条件,并利用短周期元素原子结构的特征规律以及某些元素的特征性质,才能推算出原子序数,判定元素在周期表中的位置。进而顺利作答本题。此题综合性较强,考查的知识面较广,在高考试题中经常出现。这就要求学生在复习的过程中,必须注意知识间的相互联系。具体解答为:
据①知A、B、C均为第3周期的金属元素(只有Na、Mg、Al),且原子半径A>B>C,则A、B、C分别为Na、Mg、Al;据②可知D、E均为VIIA族元素,D的单质为液体,则D为Br,E的单质为固体,则E为I;
据③知F为He,据④知G为氟。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com