
16. (07年高考全国理综卷II·9)已知:①1 mol H2分子中化学键断裂时需要吸收436 kJ的能量;
②1 mol Cl2分子中化学键断裂时需要吸收243 kJ的能量;③由H原子和Cl原子形成1 mol HCl分子时释放431 kJ的能量。下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g)+Cl2(g) = 2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的DH = 183 kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的DH =-183 kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的DH =-183 kJ/mol
15.(07年高考上海化学卷·14)已知:CH3CH2CH2CH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH =-2878 kJ·mol-1;(CH3)2CHCH3(g)+6.5O2(g)
4CO2(g)+5H2O(l);DH =-2878 kJ·mol-1;(CH3)2CHCH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH =-2869 kJ·mol-1
4CO2(g)+5H2O(l);DH =-2869 kJ·mol-1
下列说法正确的是
A.正丁烷分子储存的能量大于异丁烷分子 B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程 D.异丁烷分子中的碳氢键比正丁烷的多
14.(07年高考江苏卷·7)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g);DH = + 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g) = CO2(g)+2H2(g);DH =-192.9 kJ·mol-1

下列说法正确的是
A.CH3OH的燃烧热为192.9 kJ·mol-1 B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+1/2O2(g) = CO2(g)+2H2(g)的DH>-192.9 kJ·mol-1
13.(07年高考海南化学卷·6)已知:(1)Zn(s)+1/2O2(g) = ZnO(s);H =-348.3 kJ/mol
(2)2Ag(s)+1/2O2(g) = Ag2O(s);H =-31.0 kJ/mol
则Zn(s)+Ag2O(s) = ZnO(s)+2Ag(s)的H等于
A.-317.3 kJ/mol B.-379.3 kJ/mol C.-332.8 kJ/mol D.317.3 kJ/mol
12.(07年高考广东化学卷·16)灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g);DH1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g);DH2
③Sn(s、灰)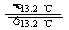 Sn(s、白);DH3=+2.1 kJ/mol
Sn(s、白);DH3=+2.1 kJ/mol
下列说法正确的是
A.DH1>DH2 B.锡在常温下以灰锡状态存在 C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
11.(08年上海化学·17)已知:H2(g)+F2(g)→2HF(g)+270 kJ,下列说法正确的是
A.2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量
B.1 mol氢气与1 mol氟气反应生成2mol液态氟化氢放出热量小于270 kJ
C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量
10.(08年海南化学·8)白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ·mol-1、P-O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A.(6a+5d-4c-12b)kJ·mol-1 B(4c+12b-6a-5d)kJ·mol-1
C.(4c+12b-4a-5d)kJ·mol-1 D.(4a+5d-4c-12b)kJ·mol-1
9.(08年重庆理综·13)化学反应N2+3H2 = 2NH3的能量变化如题13图所示,该反应的热化学方程式是
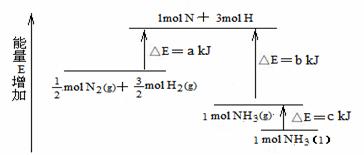
A.N2(g)+3H2(g) = 2NH3(l);⊿H = 2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g) = 2NH3(g) ;⊿H = 2(b-a)kJ·mol-1
C.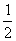 N2(g)+
N2(g)+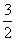 H2(g) = NH3(l) ;⊿H = (b+c-a)kJ·mol-1
H2(g) = NH3(l) ;⊿H = (b+c-a)kJ·mol-1
D.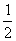 N2(g)+
N2(g)+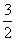 H2(g) =NH3(g) ;⊿H = (a+b)kJ·mol-1
H2(g) =NH3(g) ;⊿H = (a+b)kJ·mol-1
8.(08年四川理综·7)下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.CO(g)的燃烧热是283.0 kJ·mol-1则2CO2(g) =2CO(g)+O2(g)反应的ΔH=2×283.0 kJ·mol-1
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
7.已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8 kJ·mol-1、-1411.0 kJ·mol-1和-1366.8 kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.―44.2 kJ·mol-1 B.+44.2 kJ·mol-1 C.―330 kJ·mol-1 D.+330 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com