
3.2009年10月1日,在天安门广场举行了隆重的国庆阅兵仪式,展现了我国强大的综合国力,其中坦克的展示无疑是一个巨大的亮点。坦克的制造材料主要是各种金属的合金,铁便是其中十分重要的一种。下列关于铁的说法中正确的是
A.铁单质只具有还原性,其阳离子只具有氧化性
B.常温下,单质铁与浓硫酸不反应
C.铁元素属于过渡元素,其原子序数为26
D.比较与相同浓度的盐酸反应生成氢气的速率,纯铁比生铁的快
2.在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析的指示原子。下列说法中正确的是
A.32S与33S的中子数不等,属于两种不同的核素
B.13C和15N原子核内的质子数相差2
C.1H216O和2H218O分别与金属钠反应,所得气体的化学性质不同
D.2H+的酸性比1H+的酸性更强
1.化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是
A.纯净水几乎不含任何杂质,喝纯净水比喝矿泉水对人体更有营养
B.二氧化硫的大量排放是造成光化学烟雾的主要原因
C.某雨水样品放置一段时间后,pH由4.68变为4.28,是因为雨水中溶解了较多的CO2
D.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
26.(9分)某校化学兴趣小组的同学经查阅资料知道:淀粉在适当温度和酸催化条件下可转变为葡萄糖。为探究淀粉在不同温度下转化为葡萄糖的程度,他们每人都进行了如下两步实验:
步骤1. 用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度。实验过程中,各人控制温度不同,加热持续时间相同。
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水。观察并记录现象。
(1)由于各人控制的温度不同,出现了下列三种情况。请你根据已学知识,帮助他们完成下列实验情况汇总表。
|
|
现
象 |
结 论 |
|
第一种 情 况 |
A试管中:____________________________ B试管中:____________________________ |
淀粉没有转化为葡萄糖 |
|
第二种 情 况 |
A试管中:____________________________ B试管中:____________________________ |
______________________ |
|
第三种 情 况 |
A试管中:____________________________ B试管中:____________________________ |
淀粉全部转化为葡萄糖 |
(2)在步骤2中A试管内所加Na0H溶液的作用是 。
25.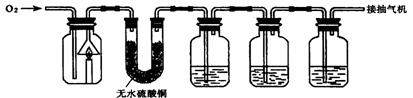 (8分)化学小组的同学为验证蜡烛(主要成分是石蜡)的燃烧产物,并测定蜡烛中碳、氢两种元素的质量比,设计的实验装置如下(注:反应前全套装置中残留的空气及反应后A瓶内残留的燃烧产物均忽略不计,且各装置均能吸收完全)。
(8分)化学小组的同学为验证蜡烛(主要成分是石蜡)的燃烧产物,并测定蜡烛中碳、氢两种元素的质量比,设计的实验装置如下(注:反应前全套装置中残留的空气及反应后A瓶内残留的燃烧产物均忽略不计,且各装置均能吸收完全)。
A B C D E
(1)实验步骤有:①称量②再称量③点燃蜡烛,并通入氧气(控制氧气流量)④停止通氧气,使蜡烛熄灭⑤按图示连接仪器⑥将装置冷却至室温。则实验步骤的顺序是(填数字序号) ______。
(2)可供选择的试剂有:稀硫酸、浓硫酸、盐酸、澄清石灰水、氢氧化钠浓溶液等。则装置C、D中所盛放的试剂依次为_________、________;装置E的作用是__________________________。
(3)为测定蜡烛中碳、氢两种元素的质量比,反应前、后必须称量装置(填装置序号) _______________的质量。
24. (5分)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如右图所示。请回答:
(1)实验中观察到的明显现象有:①剧烈反应,有气泡产生;
 ②镁条逐渐溶解;③_________________(2)产生上述现象③的原因是:①_______________________;②___________________。
②镁条逐渐溶解;③_________________(2)产生上述现象③的原因是:①_______________________;②___________________。
(3)写出相关的化学反应方程式:
23. (6分)
(1)写出编号①和②仪器的名称:① ②
(2)实验室用KMn04制O2时,应选用 做气体发生装置。已知MnO2固体和浓盐酸混合共热可制得氯气(Cl2),则应选用 做气体发生装置。
(3)有一名同学欲用F装置收集O2,则O2应从导管口 通入;另有一名同学欲用G装置收集O2,则O2应从导管口 通入。
22.(4分)我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。右表是几种物质在不同温度时的溶解度:
(1)从表中数据可以看出,温度对____________的溶解度影响不大。
(2)要使饱和溶液中的NH4C1结晶析出,在____(填“较高”或“较低”)温度下进行比较合适。
(3)“侯氏制碱法”制NaHC03的方程式是NaCl+C02+NH3+H20=NaHC03+NH4Cl,该反应能进行的原因是____________________________________________________________。
21.(8分)将铜、锌两种金属的混合物20g,放入100g稀硫酸中恰好完全反应,共放出0.2g氢气。求:⑴原混合物中锌的质量。 ⑵反应后所得溶液的质量分数。
|
|
0℃ |
20℃ |
40℃ |
60℃ |
|
NaHC03 |
6.9 |
9.6 |
2.7 |
6.4 |
|
NaCl |
35.7 |
35.8 |
6.6 |
37.3 |
|
NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
20. (6分)甘油在印刷、化妆品等工业中常用作润湿剂,也可用来制造医药和炸药。
(1)根据甘油的化学式C3H8O3, 你能得出哪些信息?(任写四条)① ;② ;③ ;④ ;
(2)瑞典化学家诺贝尔是安全使用硝化甘油炸药的第一人。硝化甘油(C3H5N3O9)是意大利化学家索布赖罗利用甘油和某物质X在一定条件下合成的,该反应的化学方程式为:C3H8O3+3X==C3H5N3O9 +3H2O 。则X的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com