
18.(12分)W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高。试回答下列各题:
(1)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,写出其中两种离子发生反应生成两种分子的离子方程式_______________________________________。
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A和B是日常生活中常用调味品的主要成分,且A与B能够反应生成C,试写出该反应的化学方程式___________________________________________________________。
(3)由W、X、Y、Z四种元素中的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式______________________________。
 (4)已知由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如图所示的转化关系。
(4)已知由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如图所示的转化关系。
①写出A与B反应生成C的化学方程式____________________________________;
②向50 mL4 mol·L-1的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中溶质的
物质的量之比为__________________________________。
(5)W、Y、Z三种元素可组成一种无机盐,其组成可表示为W4Y2Z3,则该溶液中离
子浓度由大到小的顺序为____________________________________________。
17.(12分)化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必需的技能,是学好化学的关键。试回答下列与实验有关的问题:
 (1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证。最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀。(部分夹持装置和加热装置省略)
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证。最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀。(部分夹持装置和加热装置省略)
①装置B中的试剂是_______________(填写名称);
②装置C的作用是______________________________________。
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分:Ag/a-Al2O3)来回收金属银和a-Al2O3,a-Al2O3作为催化剂的载体,且不溶于硝酸。(部分操作过程省略)
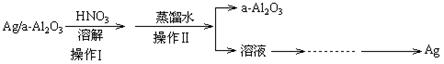
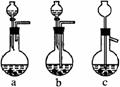 ①进行操作Ⅰ可选用右图所示装置中的装置_____(选填a、b、c);
①进行操作Ⅰ可选用右图所示装置中的装置_____(选填a、b、c);
②实验操作Ⅱ中,所需的主要玻璃仪器有______________________;
③实验操作Ⅱ中能否用自来水代替蒸馏水,_________(填“能”或“否”);为什么?_____________________________________________________________
_____________________________(请结合有关离子方程式回答)。
16.研究发现铜具有独特的杀菌功能,能较好地抑制病菌的生长。在工业上铜的冶炼大致可分为:①富集:将硫化物矿石进行浮选;②焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);③制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑;④电解精炼。
下列说法不正确的是
A.上述生产过程中的尾气可以通入氨水中,生产氮肥
B.每生产6mol Cu,理论上需消耗11mol O2
C.反应2Cu2O+Cu2S=6Cu+SO2↑中的还原剂是Cu2S
D.电解精炼时,粗铜应与外电源的正极相连
高三化学试题
第Ⅱ卷(共60分)
15.在室温条件下,向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,
恰好使溶液的pH=7,下列叙述正确的是
A.溶液中2c(Na+)=c(SO42-) B.a/2 mol>沉淀的物质的量>0
C.沉淀的物质的量= a/2 mol D.原溶液中c(H2SO4) = a/2 mol/L
14.下表是元素周期表的一部分,有关说法不正确的是
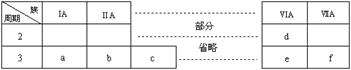
A.a、b、d、f四种元素的离子半径:f>d>a>b
B.元素b的单质不能与酸性氧化物发生化学反应
C.元素c的氧化物既能与酸反应又能与碱反应
D.a、c、e的最高价氧化物对应水化物之间能够相互反应
13.科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定的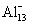 和
和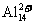 。下列说法不正确的是
。下列说法不正确的是
A.Al14与Al化学性质相似,都具有较强的还原性
B.Al13超原子中Al原子间是通过共价键结合的
C.Al14与稀盐酸反应的化学方程式可表示为:Al14+2HCl==Al14Cl2+H2↑
D.Al13表示质子数为13的铝原子
12.下列表述或判断正确的是
A.25℃时,pH=10的NaOH溶液与pH=10的氨水中:c(Na+)=c(NH4+)
B.相同条件下等物质的量浓度的①NaCl 溶液;②NaOH溶液;③HCl溶液中由
水电离出的c(H+):③>①>②
C.在Na2CO3、NaHCO3两种溶液中,离子种类不相同
D.25℃时,浓度为0.2 mol·L-1的Na2CO3溶液中只存在水解平衡,不存在电离平衡
11.下列反应的离子方程式书写正确的是
A.向四羟基合铝酸钠溶液中滴加过量的碳酸氢钠溶液:[Al(OH)4]-+4H+=Al3++2H2O
B.将少量SO2气体通入足量的NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
D.向沸水中滴加饱和氯化铁溶液:Fe3++3H2O=Fe(OH)3↓+3H+
10.X、Y、Z为三种单质。已知:Y能将Z从其化合物的水溶液中置换出来,而Z又能将X从其化合物的水溶液中置换出来。由此可以推断下列说法中可能正确的是
①单质的氧化性:Y>Z>X; ②单质的还原性:Y>Z>X;
③对应离子的氧化性:X>Z>Y; ④对应离子的还原性:X>Z>Y
A.只有① B.只有②③ C.只有①④ D.①②③④
9.下列关于有机物的说法中正确的是
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤塑料、橡胶和纤维都是合成高分子材料
⑥石油的分馏、裂化和煤的干馏都是化学变化
A.①⑤⑥ B.②④ C.①②③⑤ D.②④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com