
11、有人曾建议用AG表示溶液的酸度(acidity arede),AG的定义为
AG=lg[c(H+)/(OH-)]。现有25℃时0.1 mol·L-1的二元酸H2A溶液的AG=6.0,则下列说法正确的是
A、在Na2A、NaHA两溶液中,前者所含微粒种类多
B、在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数近似相等
C、某NaOH溶液与H2A溶液等体积混合后,其AG的值一定小于零
D、在25℃时,溶液的pH与AG的换算公式为pH=7-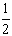 AG
AG
10、某无色溶液中存在SiO32-,若向其中加入NH4Cl溶液后产生白色沉淀,若向其中加入CaCl2溶液也产生白色沉淀,则下列各组离子能在该溶液中共存的是
A、F-、C17H35COO-、Na+、NO3- B、AlO2- 、NH4+、ClO-、CO32-
C、CO32-、NH4+、Ag+、MnO4- D、Na2+、Ca2+、C2O42-、Cl-
9、阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中正确的是
A.lmol·L-1的醋酸钠溶液中含CH3COOH、CH3COO-总数约为6.02×1023
B.71g氯气通入足量的水中,反应中转移的电子总数约为6.02×1023
C.常温常压下,14 g 碳烯(∶CH2)所含电子总数约为8×6.02×1023
D.常温常压下乙炔和1,3-丁二烯混合气a g,其中C-H键的数目约为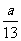 ×6.02×1023
×6.02×1023
8、若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1乙醇溶液的质量分数,且知2ω1=ω2,则下列推断正确的是(乙醇的密度比纯水的小)
A a<b<2a B 2b=a C b>2a D 2a=b
7、下列叙述中正确的是 A、CO2分子内含有极性键,所以CO2分子是极性分子
B、 分子晶体、原子晶体中一定含有共价键,离子晶体一定含有离子键
C、气态氢化物的稳定性:NH3>PH3>AsH3
D、某非金属元素从游离态变成化合态时,该元素一定被还原
6、下列工业生产的说法错误的是
A. 氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产方法又称“阳离子交换膜法”
B. 生产普通玻璃的主要原料及设备:石灰石、石英、纯碱及玻璃熔炉
C. 由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件
D. 合成氨的反应是放热反应,因此工业合成常采用低温条件
5、下列说法正确的是
A.苯酚、淀粉KI、乙酸、氢氧化钾四种溶液可用FeCl3溶液一次鉴别
B.CH3CH2OH、 CH2=CHCOOH、 CH3CHO、 CH3COOH四种溶液可用新制Cu(OH)2一次鉴别
C.CaCl2溶液中混有少量HCl,可加入过量的CaO,再过滤
D、KCl溶液中混有少量KI,可通入足量Cl2后,再用乙醇进行萃取、分液
4、下列关于反应能量的说法正确的是
A、 Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s);△H =-216 kJ·mol-1,E反应物>E生成物
B、CaCO3(s)=CaO(s)+CO2(g); △H =+178.5 kJ·mol-1,E反应物>E生成物
C、HI(g) =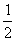 H2(g)+
H2(g)+ 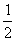 I2(s);△H
=--26.5kJ·mol-1,1mol HI在密闭容器中分解后放出26.5kJ的能量
I2(s);△H
=--26.5kJ·mol-1,1mol HI在密闭容器中分解后放出26.5kJ的能量
D、H+(aq)+OH-(aq)=H2O(l);△H =-57.2 kJ·mol-1,含1molNaOH水溶液与含0.5mol H2SO4的浓硫酸混合后放热57.2 kJ
3、下列说法中正确的是
A.苯酚溶液不慎沾到皮肤上,应立即用稀NaOH溶液洗涤 B.液氯不能用钢瓶贮存
C.用饱和NaHCO3溶液可以除去CO2气体中混有的少量SO2
D.实验室中所有药品使用后均不能放回原瓶
2、下列说法无科学性错误的是
A.铅笔芯的原料是重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒
B.CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收CO,防止煤气中毒
C.油条制作中常常加入明矾,不仅作为膨化剂,还有利于补充人体所需的微量元素
D.薯片、薯条等淀粉类油炸食品中丙烯酰氨(CH2=CHCONH2)含量较高,应谨慎食用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com