
⒘(10分)已知向量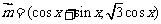 ,
, ,设函
,设函 数
数
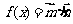 ,若角
,若角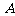 是锐角三角形的最大内角,求
是锐角三角形的最大内角,求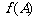 的取值范围.
的取值范围.
⒙(12分)将编号为1,2,3,4,5的五个相同小球,随机放入编码分别为1,2,3,
4,5的五个小盒中,每盒仅放一球,若第 号小球恰好落入第
号小球恰好落入第 号小盒中,则称其
号小盒中,则称其
为一个匹对,用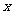 表示匹对的个数.
表示匹对的个数.
⑴ 求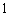 号小球不落入
号小球不落入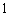 号盒子中,且
号盒子中,且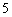 号小球不落入
号小球不落入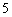 号盒子中的概率;
号盒子中的概率;
⑵ 求匹对数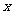 的分布列和数学期望.
的分布列和数学期望.
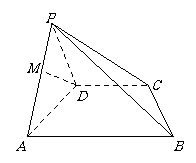
⒚(12分)如图,四棱锥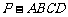 中,底面
中,底面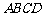 是直角梯形,
是直角梯形, ,
,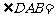
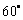 ,
,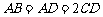 ,侧面
,侧面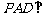 底面
底面 ,且
,且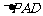 为等腰直角三角形,
为等腰直角三角形,
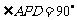 ,
,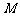 为
为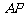
 的中点.
的中点.
⑴ 求证: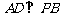 ;
;
⑵ 求二面角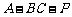 的大小.
的大小.
⒛(12分)已知数列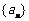 的首项为
的首项为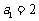 ,前
,前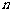 项和为
项和为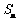 ,且对任意的
,且对任意的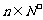 ,当
,当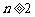
时,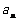 总是
总是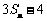 与
与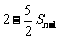 的等差中项.
的等差中项.
⑴ 求数列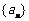 的通项公式;
的通项公式;
⑵ 设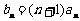 ,
,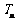 是数列
是数列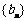 的前
的前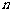 项和,
项和,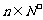 ,求
,求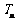 .
.
21.(12分)曲线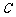 是中心在原点,焦点在
是中心在原点,焦点在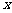 轴上的双曲线,已知它的一个焦点
轴上的双曲线,已知它的一个焦点 的
的
坐标为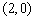 ,一条渐近线的方程为
,一条渐近线的方程为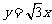 ,过焦点
,过焦点 作直线交曲线
作直线交曲线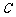 的右支于
的右支于
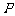 、
、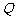 两点,
两点,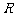 是弦
是弦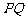 的中点.
的中点.
⑴ 求曲线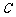 的方程;
的方程;
⑵ 若在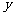 轴左侧能作出直线
轴左侧能作出直线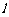 :
: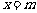 ,使以线段
,使以线段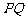 为直径的圆与直线
为直径的圆与直线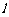 相切,
相切,
求实数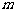 的取值范围.
的取值范围.
⒔ 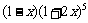 展开式按
展开式按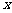 的升幂排列,则第3项的系数为 .
的升幂排列,则第3项的系数为 .
⒕ 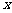 、
、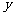 满足约束条件:
满足约束条件: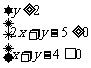 ,则
,则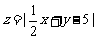 的最小值是 .
的最小值是 .
⒖ 已知两点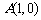
 ,
,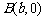 ,若抛物线
,若抛物线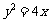 上存在点
上存在点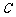 使
使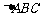 为等边三角形,
为等边三角形,
则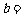 .
.
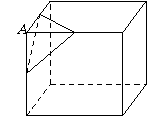 ⒗ 如图,设
⒗ 如图,设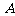 是棱长为
是棱长为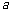 的正方体的一个顶点,过从此顶
的正方体的一个顶点,过从此顶
点出发的三条棱的中点作截面,对正方体的所有顶点都
如此操作,所得的各截面与正方体各面共同围成一个多
面体,则关于此多面体有以下结论:①
有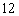 个顶点;
个顶点;
②
有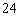 条棱;③ 有
条棱;③ 有
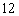 个面;④ 表面积为
个面;④ 表面积为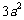 ;⑤ 体
;⑤ 体
积为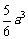 .其中正确的结论是 (要求填上所有正
.其中正确的结论是 (要求填上所有正
确结论的序号).
⒈ 在复平面内,复数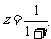 所对应的点位于
所对应的点位于
A.第一象限 B.第二象限 C.第三象限 D.第四象限
⒉ 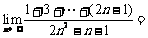
A.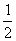 B.
B. C.
C.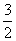 D.
D.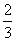
⒊ 在等差数列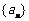 中,有
中,有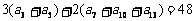 ,则此数列的前
,则此数列的前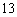 项和为
项和为
A.24
B.39 C.52
 D.104
D.104
⒋ 若曲线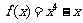 在点
在点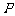 处的切线平行于直线
处的切线平行于直线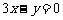 ,则点
,则点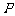 的坐标为
的坐标为
A.(1,3) B.(-1,3) C.(1,0) D.(-1,0)
⒌ 设偶函数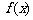 在
在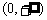 上为减函数,且
上为减函数,且 ,则不等式
,则不等式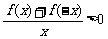 的
的
解集为
A.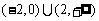 B.
B.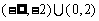 C.
C.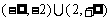 D.
D.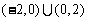
⒍ 设集合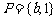 ,
,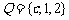 ,
,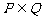 ,若
,若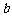 、
、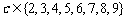 ,则
,则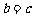 的
的
概率是
A.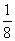 B.
B.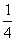 C.
C.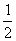 D.
D.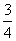
⒎ 已知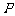 是边长为2的正
是边长为2的正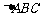 边
边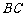 上的动点,则
上的动点,则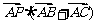 的值
的值
A.最大值为8 B.是定值6 C.最小值2 D.与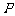 的位置有关
的位置有关
⒏ 将函数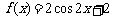 的图象按向量
的图象按向量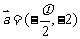 平移后得
平移后得 到的图象的函数为Z#X#X#K]
到的图象的函数为Z#X#X#K]
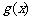 ,若函数
,若函数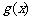 是奇函数,且在
是奇函数,且在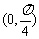 上是增函数,则
上是增函数,则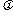 的一个值为
的一个值为
A.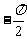 B.
B.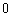 C.
C.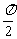 D.
D.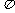
⒐ 已知四棱柱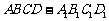 的底面为正方形,侧棱与底面边长相等,且点
的底面为正方形,侧棱与底面边长相等,且点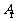 在底
在底
面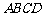 内的射影为正方形
内的射影为正方形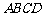 的中心,则
的中心,则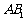 与底面
与底面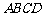 所成角的正弦值
所成角的正弦值
等于
A.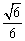 B.
B.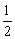 C.
C.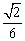 D.
D.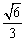
⒑ 已知函数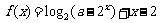 ,若
,若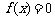 有解,则实数
有解,则实数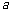 的取值范围是
的取值范围是
A.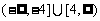 B.
B. C.
C.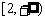 D.
D.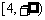
⒒ 将正方体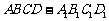 的各面涂色,任何相邻两个面不同色,现在有5种不同
的各面涂色,任何相邻两个面不同色,现在有5种不同
的颜色,并且涂好了过顶点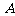 的3个面的颜色,那么其余的3个面的涂色方案共有
的3个面的颜色,那么其余的3个面的涂色方案共有
A.15种  B.14种
C.13种
D.12种
B.14种
C.13种
D.12种
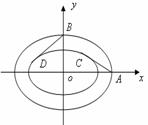 ⒓ 北京奥运会主体育场“鸟巢”的钢结构俯视图如图所示,
⒓ 北京奥运会主体育场“鸟巢”的钢结构俯视图如图所示,
内外两圈的钢骨架是离心率相同的椭圆,外层椭圆顶点
向内层椭圆引切线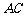 、
、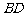 ,设内层椭圆方程为
,设内层椭圆方程为
 ,则外层椭圆
,则外层椭圆 方程可设为
方程可设为
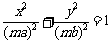
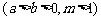 .若
.若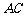 与
与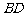 的斜
的斜
率之积为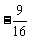 ,则椭圆的离心率为
,则椭圆的离心率为
A.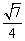 B.
B.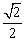 C.
C.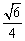 D.
D.
(二) 溶液计算
 基本公式及关系:
基本公式及关系:
(1)物质的量浓度:
①。
②稀释过程中溶质不变:C1V1=C2V2。
③同溶质的稀溶液相互混合:C混=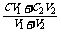
④质量分数换算为物质的量浓度:C=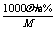
(2)溶质的质量分数。
①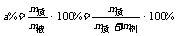
②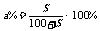 (饱和溶液,S代表溶质该条件下的溶解度)
(饱和溶液,S代表溶质该条件下的溶解度)
③混合:m1a1%+m2a2%=(m1+m2)a%混
④稀释:m1a1%=m2a2%
(3)有关溶解度的计算:
①S=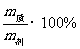 (饱和溶液:一定温度下)
(饱和溶液:一定温度下)
②S=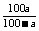 (a%:饱和溶液质量分数)
(a%:饱和溶液质量分数)
③有关pH值的计算:酸算H+,碱算OH-
Ⅰ. pH= -lg[H+]
Ⅱ. KW=[H+][OH-]=10-14(25℃下)
考试注意:
1. 要抓住关键字在题目的问题中,通常出现如下词:正确与错误、大与小、强与弱、能与否,由强到弱或由弱到强,名称与符号,分子式、结构简式、电子式,化学方程式与离子方程式等,即使题目会做,由于不注意上述词语,就有可能造成失分。
2. 注意各量的单位物质的量浓度(mol/L),摩尔质量(g/mol),深解度(g)、百分数、浓度互换时的体积易错等。
3. 题目中隐含性的限制条件如(1)酸性的无色透明溶液,(2)PH=0的溶液(3)水电离出的[OH-]=10-14mol/L的溶液等
4. 注意常见符号的应用如"=",可逆符号、"△H>0"、"△H<0"、沉淀、气体符号,电荷与价标、写电子式时"[ ]"的应用、物质的聚集状态、特殊的反应条件等等。
5. 实验填空题或简答题,注意文字要准确(1)不要用错别字:如脂与酯、铵与氨、坩与甘、蘸与粘、蓝与兰、褪与退、溶与熔、戊与戌、催与崔、苯与笨等。(2) 不用俗语:如a、打开分液漏斗的开关(活塞),b、将气体通进(入)盛溴水的洗气瓶,c、酸遇石蕊变红色(酸使石蕊呈红色)等。
(一)有关化学式的计算
1.通过化学式,根据组成物质的各元素的原子量,直接计算分子量。
2.已知标准状况下气体的密度,求气体的式量:M=22.4ρ。
3.根据相对密度求式量:M=MˊD。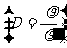
4.由气态方程求式量:M=
5.混合物的平均分子量:
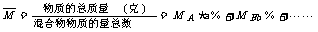
6.原子量
①原子的原子量=
②质量数=质子数+中子数
③元素原子量: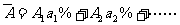
A1、A2表示同位素原子量,a1%、a2%表示原子的摩尔分数
④元素近似原子量: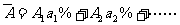
A1、A2表示同位素原子量,a1%、a2%表示原子的摩尔分数
②对气体使用体积时注意条件(温度及压强),否则气体体积无意义
Ⅴ、化学计算
酯的水解(70-80℃)、硝酸钾溶解度的测定(室温-100℃)需用温度计来控制温度;银镜反应需用温水浴加热即可。
(二)无机
1. 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物);
2. 亚铁盐及氢氧化亚铁;
3. -2价硫的化合物(H2S、氢硫酸、硫化物);
4. +4价硫的化合物(SO2、H2SO3及亚硫酸盐);
5. 双氧水(H2O2,其中氧为-1价)
※注:苯的同系物被KMnO4(H+)溶液氧化的规律:
侧链上与苯环直接相连的碳原子被氧化成羧基,其他碳原子则被氧化成CO2。
倘若侧链中与苯环直接相连的碳原子上没有氢,则不能被氧化。

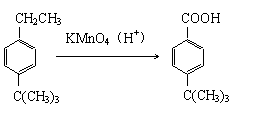
如:
Ⅳ、化学实验:
不宜长期暴露空气中的物质
1.由于空气中CO2的作用:生石灰、NaOH、Ca(OH)2溶液、Ba(OH)2溶液、NaAlO2溶液、水玻璃、碱石灰、漂白粉、苯酚钠溶液、Na2O、Na2O2;
2.由于空气中H2O的作用:浓H2SO4、P2O5、硅胶、CaCl2、碱石灰等干燥剂、浓H3PO4、无水硫酸铜、CaC2、面碱、NaOH固体、生石灰;
3.由于空气中O2的氧化作用:钠、钾、白磷和红磷、NO、天然橡胶、苯酚、-2价硫(氢硫酸或硫化物水溶液)、+4价硫(SO2水溶液或亚硫酸盐)、亚铁盐溶液、Fe(OH)2。
4.由于挥发或自身分解作用:AgNO3、浓HNO3、H2O2、液溴、浓氨水、浓HCl、Cu(OH)2。
化学实验设计思维模型:
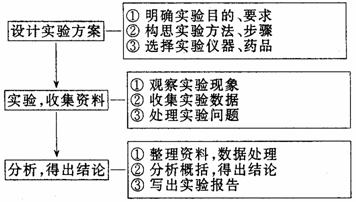 实验中水的妙用
实验中水的妙用
(一)有机
1. 不饱和烃(烯烃、炔烃、二烯烃、苯乙烯等);
2. 苯的同系物;※
3. 不饱和烃的衍生物(烯醇、烯醛、烯酸、卤代烃、油酸、油酸盐、油酸酯等);
4. 含醛基的有机物(醛、甲酸、甲酸盐、甲酸某酯等);
5. 酚类
6. 石油产品(裂解气、裂化气、裂化汽油等);
7. 煤产品(煤焦油);
8. 天然橡胶(聚异戊二烯)。
(二)无机
1. -2价硫(H2S及硫化物);
2. +4价硫(SO2、H2SO3及亚硫酸盐);
3. +2价铁:
 6FeSO4+3Br2=2Fe2(SO4)3+2FeBr3
6FeSO4+3Br2=2Fe2(SO4)3+2FeBr3
6FeCl2+3Br2=4FeCl3+2FeBr3 变色
2FeI2+3Br2=2FeBr3+2I2
4.Zn、Mg等单质 如Mg+Br2MgBr2
(此外,其中亦有Mg与H+、Mg与HbrO的反应)
5.-1价的碘(氢碘酸及碘化物) 变色
6.NaOH等强碱:Br2+2OH‾==Br‾+BrO‾+H2O
7.Na2CO3等盐:Br2+H2O==HBr+HBrO 2HBr+Na2CO3==2NaBr+CO2↑+H2O
HBrO+Na2CO3==NaBrO+NaHCO3
8.AgNO3
能萃取溴而使溴水褪色的物质
上层变无色的(ρ>1):卤代烃(CCl4、氯仿、溴苯等)、CS2;
下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、液态环烷烃、低级酯、液态饱和烃(如已烷等)等
能使酸性高锰酸钾溶液褪色的物质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com