
11Θ°œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «
AΘ°ΧΦΥα«βοß»ή“Κ”κΉψΝΩ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΘΚNH4++OHΘ≠ΘΫNH3ΓΛH2O
BΘ°Fe(OH)3”κ«βΒβΥα»ή“ΚΜλΚœΘΚFe(OH)3+3H+ΘΫFe3++3H2O
CΘ°ΒγΫβΨΪΝΕΆ≠ΒΡ“θΦΪΖ¥”Π «ΘΚCu2++2eΘ≠ΘΫCuΓΓΓΓ
DΘ°1 mol/LΒΡNaAlO2»ή“ΚΚΆ2.5 mol/LΒΡHClΒ»ΧεΜΐΜΞœύΨυ‘»ΜλΚœΘΚ
2AlO2-+5H+ ΘΫ Al(OH)3Γΐ+Al3++H2O
10Θ°ΗυΨί»»Μ·―ßΖΫ≥Χ ΫΘΚS(s)+O2(g)=SO2(g)ΘΜΓςH=Θ≠297.23kJΓΛmolΘ≠1Ζ÷Έωœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ
ΓΓΓΓΓΓ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
AΘ°S(g)+O2(g)=SO2(g)ΘΜΓςH<Θ≠297.23kJΓΛmolΘ≠1
BΘ°S(g)+O2(g)=SO2(g)ΘΜΓςH>Θ≠297.23kJΓΛmolΘ≠1
CΘ°S(g)+O2(g)=SO2(g)ΘΜΓςH<+297.23kJΓΛmolΘ≠1
DΘ°S(g)+O2(g)=SO2(g)ΘΜΓςH>+297.23kJΓΛmolΘ≠1
9Θ°NA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
AΘ°1 mol HNO3ΦϊΙβΖ÷ΫβΘ§ΉΣ“ΤΒγΉ” ΐ4NA
BΘ°28 gΨßΧεΙη÷–Κ§”–SiΘ≠SiΦϋΒΡ ΐΡΩΈΣ2NA
CΘ°100 mL 0.5 mol/LΒΡ(NH4)2SO4»ή“Κ÷–Θ§Κ§”–0.1NAΗωNH4+
DΘ°Cu”κ≈®œθΥα≤ζ…ζΒΡ22.4 L(±ξΉΦΉ¥Ωω)ΤχΧε÷–Κ§‘≠Ή” ΐΈΣ3NA
8Θ°‘Ύ»ΐ÷ß ‘Ιή÷–Θ§ΗςΉΔ»κ1mLΥ°Θ§Ζ÷±πΦ”»κ3mLΒΡ““ΥαΓΔ““Υα““θΞΚΆœθΜυ±ΫΓΘ»γœ¬ΆΦΥυ ΨΘ§
 ΓΓ
»ΐ÷ß ‘ΙήΔΌΔΎΔέ“ά¥Έ «(ΓΓ )
ΓΓ
»ΐ÷ß ‘ΙήΔΌΔΎΔέ“ά¥Έ «(ΓΓ )
ΓΓΓΓΓΓ AΘ°““ΥαΓΔ““Υα““θΞΚΆœθΜυ±ΫΓΓΓΓ
ΓΓΓΓΓΓ BΘ°““Υα““θΞΓΔ““ΥαΚΆœθΜυ±Ϋ
ΓΓΓΓΓΓ CΘ°œθΜυ±ΫΓΔ““ΥαΚΆ““Υα““θΞΓΓΓΓ
ΓΓΓΓΓΓ DΘ°““Υα““θΞΓΔœθΜυ±ΫΚΆ““Υα
7Θ°œ¬Ν–Έο÷ ΒΡΟϊ≥ΤΖ÷±π «
|
Οϊ≥Τ |
Νρ¥ζΝρΥαΡΤ |
ΕύΝρΜ·ΗΤ |
Ιΐ―θΜ·±Β |
≥§―θΜ·ΦΊ |
|
Μ·―ß Ϋ |
Na2S2O3 |
CaSx |
BaO2 |
KO2 |
‘ΉέΚœ…œ ωΟϋΟϊΙφ¬…Θ§Ζ÷ΈωΥΦΩΦΚσΜΊ¥πK2CO3ΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°»ΐΝρ¥ζΧΦΥαΦΊΓΓΓΓ BΘ°ΕύΝρΧΦΥαΦΊΓΓΓΓΓΓΓΓ CΘ°ΙΐΝρΧΦΥαΦΊΓΓΓΓΓΓΓΓ DΘ°≥§ΝρΧΦΥαΦΊ
6Θ°œ¬Ν–»ή“Κ÷–ΒΡΗςΉιάκΉ”Θ§“ρΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΕχ≤ΜΡή¥σΝΩΙ≤¥φΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°H+ΓΔNa+ΓΔNO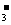 ΓΔSO
ΓΔSO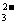 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°AlO
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°AlO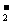 ΓΔOHΘ≠ΓΔNa+ΓΔNH
ΓΔOHΘ≠ΓΔNa+ΓΔNH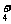 ΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓ CΘ°Fe3+ΓΔSCNΘ≠ΓΔSO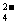 ΓΔClΘ≠ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°Fe3+ΓΔHCO
ΓΔClΘ≠ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°Fe3+ΓΔHCO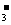 ΓΔClΘ≠ΓΔNH
ΓΔClΘ≠ΓΔNH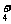
5Θ°œ¬Ν–≥ΐ»Ξ‘”÷ ΒΡΖΫΖ®≤Μ’ΐ»ΖΒΡ «
|
A |
≥ΐ»ΞNO÷–ΒΡ…ΌΝΩNO2 |
Ά®ΙΐH2O»ή“ΚΘ§ ’Φ·ΤχΧε |
|
B |
≥ΐ»ΞSO2÷–ΒΡ…ΌΝΩHCl |
Ά®ΙΐNa2SO3»ή“ΚΘ§ ’Φ·ΤχΧε |
|
C |
≥ΐ»ΞFeCl2»ή“Κ÷–ΒΡ…ΌΝΩCuCl2 |
Φ”»κΉψΝΩFe–ΦΘ§≥δΖ÷Ζ¥”ΠΚσΘ§Ιΐ¬Υ |
|
D |
≥ΐ»ΞKCl»ή“Κ÷–ΒΡ…ΌΝΩK2CO3 |
ΒΈ»κ ΝΩ―ΈΥα»ή“ΚΘ§÷±ΒΫΈόΤχ≈ί≤ζ…ζ |
4Θ°ΙΊ”ΎΡ≥»ή“ΚΥυΚ§άκΉ”Φλ―ιΒΡΖΫΖ®ΚΆΫα¬έ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
AΘ°Φ”»κΙΐΝΩNaOH»ή“ΚΘ§”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§‘ρ‘≠»ή“Κ“ΜΕ®”–Mg2+
BΘ°Φ”»κAgNO3»ή“Κ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§Φ”œΓ―ΈΥα≥ΝΒμ≤Μœϊ ßΘ§‘ρ‘≠»ή“Κ“ΜΕ®”–ClΘ≠
CΘ°Φ”»κ―ΈΥα≤ζ…ζΡή Ι≥Έ«ε ·Μ“Υ°±δΜκΉ«ΒΡΤχΧεΘ§‘ρ‘≠»ή“Κ÷–Ω…Ρή”–CO32Θ≠ΜρSO32Θ≠
DΘ°Φ”»κNaOH≤ΔΦ”»»Θ§≤ζ…ζ Ι Σ»σΒΡάΕ…Ϊ ·»ο ‘÷Ϋ±δΚλΒΡΤχΧεΘ§‘ρ‘≠»ή“Κ «οß―Έ»ή“Κ
3Θ°ΚψΈ¬ΓΔΚψ―Ιœ¬Θ§a molAΚΆb molB‘Ύ“ΜΗω»ίΜΐΩ…±δΒΡ»ίΤς÷–ΖΔ…ζ»γœ¬Ζ¥”ΠΘΚ
A(g)+2B(g) 2C(g)Θ§“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ§…ζ≥…n molCΓΘ‘ρœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «
2C(g)Θ§“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ§…ζ≥…n molCΓΘ‘ρœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «
ΓΓΓΓ AΘ°Έο÷ AΓΔBΒΡΉΣΜ·¬ ÷°±»ΈΣaΓΟb
BΘ°Τπ Φ ±ΩΧΚΆ¥οΤΫΚβΚσ»ίΤς÷–ΒΡ―Ι«Ω±»ΈΣ(a+b)ΓΟ(a+bΘ≠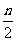 )
)
ΓΓΓΓ CΘ°»τΤπ Φ ±Ζ≈»κ2a molAΚΆ2b molBΘ§‘ρ¥οΤΫΚβ ±…ζ≥…2n molC
ΓΓΓΓ DΘ°Β±v’ΐ(A)ΘΫ2vΡφ(B) ±Θ§Ω…»ΖΕ®Ζ¥”Π¥οΤΫΚβ
2Θ°ΫΪSO2Ά®»κCuSO4ΚΆNaClΒΡ≈®»ή“Κ÷–Θ§»ή“Κ―’…Ϊ±δ«≥Θ§Έω≥ωΑΉ…Ϊ≥ΝΒμΘ§»ΓΗΟ≥ΝΒμΖ÷ΈωΘ§÷ΣΤδ÷–Κ§ClΘΚ35.7%Θ§CuΘΚ64.3%Θ§SO2‘Ύ…œ ωΖ¥”Π÷–Ής”Ο «
ΓΓ AΘ°ΥαΓΓΓΓΓΓ BΘ°Τ·ΑΉΦΝΓΓΓΓΓΓ CΘ°ΜΙ‘≠ΦΝΓΓΓΓΓΓ DΘ°―θΜ·ΦΝ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com