
20.在一定体积pH =12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH =11。若反应后溶液的体积等于Ba(OH)2溶液和NaHSO4溶液体积之和,则Ba(OH)2溶液和NaHSO4溶液体积之比是
A.1:9 B.1:1 C.1:2 D.1:4
第Ⅱ卷 (非选择题 共50分)
19.下列溶液中微粒的物质的量浓度关系正确的是
A.室温下,向0.01 mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
B.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
C.Na2CO3溶液:c(OH-)=c(HCO3-)+c(H2CO3)+c(H+)
D.25℃时,pH=4.75、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液:
c(CH3COO-)+c(OH-)<c(CH3COOH)+C(H+)
18.温度相同、浓度均为0.2 mol的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、
⑤C6H5ONa⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.①③⑥④②⑤ B.③①④②⑥⑤
C.③②①⑥④⑤ D.⑤⑥②④①③
17.以下说法正确的是
A.同体积同浓度的盐酸和醋酸和足量锌反应,开始时,醋酸反应速率快
B.同体积同pH的盐酸和醋酸与足量锌反应,盐酸放出H2多
C.同体积浓度的盐酸和醋酸与足量锌反应,盐酸放出的热量多
D.盐酸和醋酸分别与锌反应的离子方程式均为Zn+2H+=Zn2++H2
16.某温度下,在一容积可变的容器中,反应2A(g)+B(g)  2C(g)达到平衡时,A、B和C的物质的量分别为4moL 、2moL和4moL。保持温度和压强不变,对平衡混合物中三者的量做如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为4moL 、2moL和4moL。保持温度和压强不变,对平衡混合物中三者的量做如下调整,可使平衡右移的是
A.均减半 B.均加倍 C.均增加1moL D.均减少1moL
15.可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是:
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时生成2n molNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①③④ B.①④⑥ C.②③⑤ D.①②③④⑤⑥
14.将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.3molCu,此时在另一极上产生的气体体积(标准状况)为
A.4.48L B.5.6L C.6.72L D.7.84L
13.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) ;△H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) ;△H2
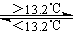
③Sn(s、灰) Sn(s、白) ; △H3=+2.1kJ/mol,下列说法正确的是
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
12.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物的水化物都是强酸
11.x、y、z为短周期元素,这些元素原子的最外层电子数分别是1、4、6。则由这三种元素组成的化合物的化学式不可能是 A.XYZ B.X2YZ C.X2YZ2 D.X2YZ3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com