
8.设NA为阿伏加德罗常数,下列说法正确的是:
A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA
B.标准状况下,14 g氮气含有的核外电子数为5NA
C.标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
D.标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA
7.下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g) =2CO(g)+O2(g)反应的
ΔH=+2×283.0 kJ·mol-1
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
6.下列各组离子在给定条件下可能大量共存的是
A.在pH=1溶液中:NH4+、K+、ClO-、Cl-
B.有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C.有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br-
D.在c(H+) =1.0×10-13 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
31.本题共分I、II两题(每空2分,共18分)
I.复等位基因是指一对同源染色体上的相同位点的等位基因有三个或三个以上(如B 和b是等位基因,b和b。是等位基因,则B、b、b。互称为复等位基因)。某二倍体植物的抗逆特性由4个复等位基因A、a1、a2、a3控制。请根据所学遗传知识回答下 列问题:
(1)基因的本质是具有 ,基因A、a1、a2、a3的根本来源是 。
(2)为探究基因之间的显、隐性关系,某生物实验小组将两种纯合子a1a1、a2a2进行杂交实验。以判定a1、a2之间是否存在明显的显、隐性关系。
实验原理:通过杂交子代的表现型的类型,可以判定基因间的显、隐性关系。
实验步骤:①将两种纯合子a1a1、a2a2进行杂交得到F1。
②再将F1自交得到F2 ③统计F2的表现型的种类。
实验结果及结论
若F2表现型有 种,则表明这两个基因之间有明显的显隐性关系。
若F2表现型有 种,则表明这两个基因之间无明显的显隐性关系。
(3)研究得知该植物的抗逆性和细胞内的水杨酸、多胺、脱落酸等非蛋白质类物质有关,请据所学知识推测基因控制该植物抗逆性的机理是:通过控制有关 ,从而间接控制该植物的抗逆性。
II.下图为某家族的遗传系谱图。设甲病显性基因为A,隐性基因为a;乙病显性基因为B,隐性基因为b。已知两种病中至少有一种为伴X染色体的遗传病,请分析回答:
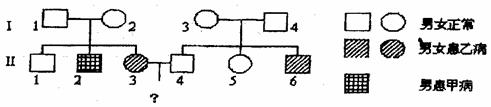
(1)甲病的遗传方式是 II2的基因型是 。
(2)若II3和II4婚配,生一个只患一种病的孩子的几率是 ;生一个同时患两种病的男孩的几率是 。
30.本题包括I、II两个小题(每空2分,共24分)
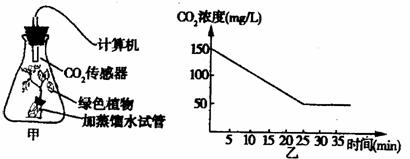 I、将一株绿色植物放入一个密封的三角瓶中。如图甲所示,在瓶口放一个测定瓶中CO2 浓度的传感器。传感器的另一端与计算机连接,以监测一段时间内瓶中CO2浓度的变化。根据实验所测数据绘制曲线如图乙。
I、将一株绿色植物放入一个密封的三角瓶中。如图甲所示,在瓶口放一个测定瓶中CO2 浓度的传感器。传感器的另一端与计算机连接,以监测一段时间内瓶中CO2浓度的变化。根据实验所测数据绘制曲线如图乙。
(1)如果图甲用于在适宜条件下测定植物光合作用速率,应首先将该装置置于 条件下,此时测定的数值表示的是 ;再将该装置置于适宜光照条件下,此时测定的数值表示的是 。
(2)由乙图知,25分钟后CO2浓度保持不变,其原因是
(3)欲使该植物继续正常生长一段时间,除把甲装置放在适宜光照条件下并控制温度适宜,还应采取的措施有:
①
②
 II、下图中的甲、乙两个细胞分别为人体内的不同细胞,请回答:
II、下图中的甲、乙两个细胞分别为人体内的不同细胞,请回答:
(1)若甲细胞表示胰岛A细胞,则乙细胞最可能是 细胞。在人体血糖偏低的情况下,乙细胞内会加快的代谢活动是
(2)若甲细胞是下丘脑细胞,则在寒冷或过度紧张的情况下,甲细胞会分泌 作用于乙细胞。乙细胞能产生 以促进幼儿生长,若幼年缺乏该物质会患
(3)若甲细胞是小肠上皮细胞,则该细胞从消化道内吸收葡萄糖的方式是
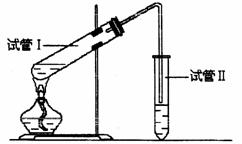
29.(18分)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式和实验装置如下:
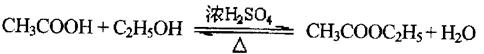
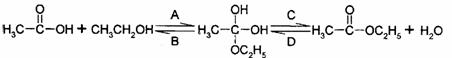 (1)该反应可能经历了如下反应过程:
(1)该反应可能经历了如下反应过程:
如果将反应按加成反应和消去反应进行分类,那么在A~D这四个反应中,属于加成反应的是 ;属于消去反应的是 。
(2)为了证明浓H2SO4在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
|
实验 编号 |
试管Ⅰ中的试剂 |
试管Ⅱ中试剂 |
测得有机层的厚度/cm |
|
A |
3mL乙醇、2mL乙酸、1mL
18mol/L浓硫酸 |
饱和碳酸钠溶液 |
5.0 |
|
B |
3mL乙醇、2mL乙酸 |
0.1 |
|
|
C |
3mL乙醇、2mL乙酸、6mL
3mol/L硫酸 |
1.2 |
|
|
D |
3mL乙醇、2mL乙酸、盐酸 |
1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 mL和 mol/L。
②分析实验 和 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是 。
③加热也有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是 。
(3)关于上述实验,下列说法正确的是(选填下列字母): 。
A.配制乙醇、浓H2SO4和乙酸的混合溶液时,各试剂加入试管的顺序是:先浓H2SO4,再乙醇,最后加乙酸。
B.试管II中饱和Na2CO3溶液的作用是:中和挥发出来的乙酸,溶解挥发出来的乙醇,便于闻乙酸乙酯的气味;降低乙酸乙酯的溶解度,有利于乙酸乙酯的分层。
C.饱和Na2CO3溶液还可用NaOH溶液代替。
D.装置中的长导管的作用主要是导气、冷凝,减少乙酸乙酯、乙酸和乙醇在空气中的挥发。
E.导气管的末端可以伸入到饱和Na2CO3溶液中。
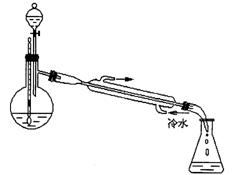 (4)某化学课外小组设计了如下图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去)
(4)某化学课外小组设计了如下图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去)
与前面装置相比, 该装置的主要优点有: 。
26.(10分)在一定条件下,可逆反应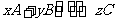 达到化学平衡状态。
达到化学平衡状态。
(1)如果A、B、C均为气体,在减压后化学平衡向逆反应方向移动,则x、y、z的关系是 。
(2)如果C是气体,并且x+y=z,在加压时化学平衡如发生移动,则平衡必向
方向移动(选填“正反应”或“逆反应”)。
(3)如果加热后,C的百分含量减小,则正反应是 反应(选填“吸热”或“放热”)。
(4)如果B、C均为气体,增加物质A的量,平衡不移动,说明物质A的状态为 。
(5)如果A、B、C均为气体,并且x+y>z,再向平衡体系中加入A、B、C使它们的浓度同时增大一倍,平衡向 方向移动(选填“正反应”或“逆反应”)。
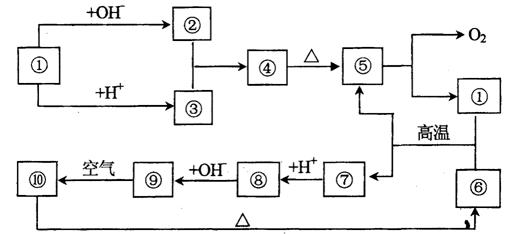 27.(18分)下图①-⑩分别代表有关反应物中的一种物质,它们均为中学化学中的常见物质。已知①-⑤和⑥-⑩中分别含有同一种元素,反应⑤→①+O2的反应条件为熔融、电解。有关转化关系如下图所示:
27.(18分)下图①-⑩分别代表有关反应物中的一种物质,它们均为中学化学中的常见物质。已知①-⑤和⑥-⑩中分别含有同一种元素,反应⑤→①+O2的反应条件为熔融、电解。有关转化关系如下图所示:
试回答下列问题:
(1)写出下列有关物质化学式:① ,⑦ 。
(2)写出①→②反应的离子方程式: 。
(3)写出②+③→④反应的离子方程式: 。
(4)写出①+⑥→⑤+⑦反应的方程式: 。
(5)写出⑨→⑩反应的方程式: 。
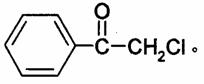 28.(14分)苯氯乙酮是一种具有荷花香味但具有强催泪作用的化学毒剂,它的结构简式为:
28.(14分)苯氯乙酮是一种具有荷花香味但具有强催泪作用的化学毒剂,它的结构简式为:
(1)已知HCHO分子中所有原子都在同一平面内。苯氯乙酮分子中,在同一平面内的碳原子最多可能有 个。
(2)苯氯乙酮不可能具有的性质 (用序号填空)。
A.难溶于水 B.能与NaOH溶液反应
C.常温下呈气体 D.在一定条件下能能与Cl2、H2反应
(3)与苯氯乙酮互为同分异构体,分子中无甲基, 在一定条件下可以和新制氢氧化铜反应产生红色沉淀,符合上述条件的芳香族化合物有 种。
(4)已知: 。苯氯乙酮的一种同分异构体有如下转化关系:
。苯氯乙酮的一种同分异构体有如下转化关系:
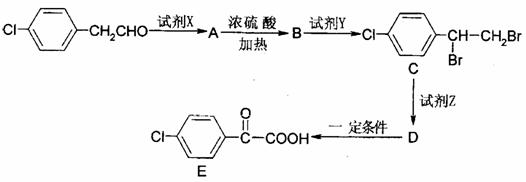
请写出:
①B的结构简式 ,试剂Y为 。
②写出实现下列转化的化学方程式:
C→D 。
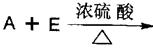 。
。
25.(19分)如题25图所示,在xOy平面内,直线MN和y轴之间存在沿y轴负方向的匀强电场,在第Ⅳ象限和第I象限的射线DC右下区域存在垂直纸面向内的匀强磁场,磁感应强度大小为B.有一质量为m,带电量为+q的质点从电场左边界上的A点沿x轴正方向射入电场,A点与原点O的距离为d,质点到达y轴上P点时,速度方向与y轴负方向的夹角为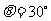 ,P点与原点O的距离为h.接着,质点进入磁场,从磁场边界OC上的Q点离开磁场之后,又从y轴上的D点垂直于y轴进入电场,最后刚好回到A点.不计质点的重力,求:
,P点与原点O的距离为h.接着,质点进入磁场,从磁场边界OC上的Q点离开磁场之后,又从y轴上的D点垂直于y轴进入电场,最后刚好回到A点.不计质点的重力,求:
 (1)D点与原点O的距离;
(1)D点与原点O的距离;
(2)匀强电场的电场强度E的大小;
(3)粒子由A点射入电场到最终回到A点所用的时间t.
24.(18分)可视为质点的小球A、B静止在光滑水平轨道上,A的左边固定有轻质弹簧,B 与弹簧左端接触但不拴接,A的右边有一垂直于水平轨道的固定挡板P.左边有一小球C沿轨道以某一未知的速度v0射向B球,如题24图所示,C与B发生碰撞并立即结成一整体D,在它们继续向右运动的过程中,当D和A的速度刚好相等时,小球A恰好与挡板P发生碰撞,碰后A立即静止并与挡板P粘连。之后D被弹簧向左弹出,D冲上左侧与水平轨道相切的竖直半圆光滑轨道,其半径为R=0.6m,D到达最高点Q时,D与轨道间弹力F=2N.已知三小球的质量分别为mA=0.2kg、mB=mC=0.1kg.取g=10m/s2,求:
(1)D到达最高点Q时的速度%的大小;
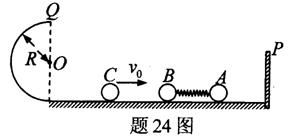 (2)C球的初速度v0的大小.
(2)C球的初速度v0的大小.
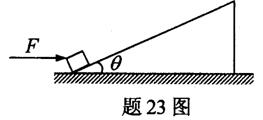
23.(16分)质量为m=6.5kg的物体在F=120N的水平推力作用下,从粗糙斜面的底端由静止开始沿斜面运动,斜面固定不动,与水平面的夹角θ=37°,如题23图所示,力F作用一段时间后撤去,物体在斜面上继续滑动了0.5s速度减为零.已知物体与斜面间的动摩擦因数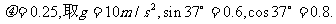 求:
求:
(1)物体在力F作用下沿斜面运动的加速度a的大小;
 (2)物体沿斜面向上运动的最大距离
(2)物体沿斜面向上运动的最大距离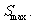
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com