
7.若能适当选择常数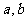 ,使得
,使得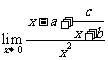 存在,则常数
存在,则常数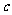 是( )
是( )
A.正数 B.零 C.负数 D.不能确定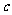 的符号
的符号
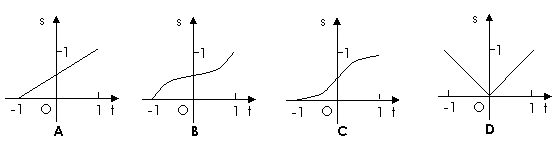
6.设D是由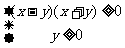 所确定的平面区域,记D被夹在直线
所确定的平面区域,记D被夹在直线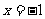 和
和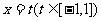 间的部分的面积为S,则函数
间的部分的面积为S,则函数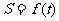 的大致图象为( )
的大致图象为( )
5.在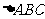 中,若对任意的实数
中,若对任意的实数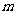 ,都有
,都有 ,则
,则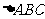 为( )
为( )
A.直角三角形 B.锐角三角形 C.钝角三角形 D.不能确定其形状
4.曲线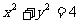 与曲线
与曲线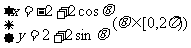 关于直线
关于直线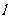 对称,则
对称,则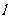 的方程为( )
的方程为( )
A.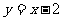 B.
B.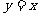 C.
C.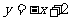 D.
D.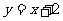
3.一高三学生计划报名参加某7所高校中的4所学校的自主招生考试,其中仅甲、乙两所学校的考试时间相同,因此该学生不能同时报考这两所学校,那么该学生不同的报考方法有( )种.
A.20 B.25 C.30 D.35
2.设向量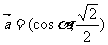 的模为
的模为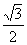 ,则
,则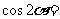 ( )
( )
A.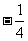 B.
B. C.
C.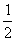 D.
D.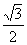
1.设集合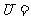 {小于7的正整数},
{小于7的正整数},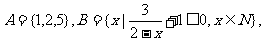 则
则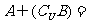 ( )
( )
A.{1} B.{2} C.{1,2} D.{1,2,5}
22. 以下两题任选一题:
a.(物质结构与性质)(14分)有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p亚层的电子数等于次外层的电子总数,C原子最外层中有2个不成对的电子。已知C、D、E原子核内的质子数均与中子数相等,且C元素可分别与A、B、D、E生成RC2型化合物,在DC2中,D与C的质量比为7︰8, 在EC2中,E与C的质量比为1︰1。请回答下列问题:
(1)写出A、B、C、D、E五种元素的元素符号:A 、E 。
(2)写出D原子的电子排布式 。
(3)指出E在元素周期表中的位置 。
(4)比较A、B、C三种元素的第一电离能的大小顺序 。
(5)比较D和E元素的电负性的相对大小 。
(6)用电子表示AC2的形成过程 。
b.(有机化学)注意:作有机化学的必须把I和II两部分全部做完
I. (8分)某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,
称取该试样0.352 g,置于铂舟并放入燃烧管中,不断通入氧气流。
用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,
两者分别增重0.144 g和0.528 g,生成物完全被吸收。
试回答以下问题:(用百分数表示,保留到小数点后两位)
(1) 维生素C中碳的质量分数是_____________,氢的质量分数____________
(2) 维生素C中是否含氧元素 。
(3) 如果需要你确定维生素C的分子式,你还需要哪些信息?
II.(6分)有机物的结构可用“键线式”简化表示。
CH3-CH=CH-CH3可简写为 。
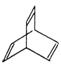
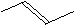
有机物X的键线式为:
(4) 有机物Y是X的同分异构体,且属于芳香烃,
写出Y的结构简式。
(5) Y与乙烯在一定条件下发生等物质的量聚合反应,
写出其反应的化学方程式:
(6) X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种。
2009-2010学年上学期三校期末联考
21.(18分)
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。
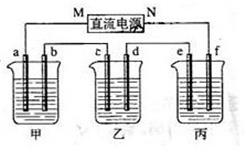
(1) 接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;
②电极b上发生的电极反应为 ;
③电极b上生成的气体在标准状态下的体积: ;
④电极c的质量变化是 g;
⑤电解后甲溶液PH (填增大、减小或不变);
简述其原因: 。
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
,
。
20.(8分)
选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn + CuSO4 = ZnSO4 + Cu
(1)在右边方框内画出装置图,
并标明各部分材料名称
(2)负极材料 ,
电解质溶液是 。
(3)写出电极反应式:
正极: ;
负极: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com