
1.[南京市2009届高三化学考前专题]四种常见元素的性质或结构信息如下表,试根据信息回答有关问题。
|
元素 |
A |
B |
C |
D |
|
性质 结构 信息 |
原子核外有两个电子层,最外层有3个未成对的电子 |
原子的M层有1对成对的p电子 |
原子核外电子排布为[Ar]3d104sx, 有+1、+2两种常见化合价 |
有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
⑴写出B原子的电子排布式 ▲ 。
⑵A元素的氢化物的沸点比同主族相邻元素氢化物沸点 ▲ (填“高”或“低”),其原因是 ▲ 。
⑶D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点 ▲ (填“高”或“低”),其原因是 ▲ 。
⑷往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为 ▲ ,简要描述该配合物中化学键的成键情况 ▲ 。
 ⑸下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,
⑸下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,
“ ”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
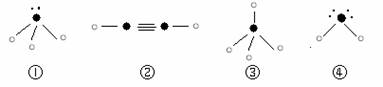
则在以上分子中,中心原子采用sp3杂化形成化学键的是 ▲ (填写序号);在②的分子中有 ▲ 个σ键和 ▲ 个π键。
19.据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。
(1)下列有关O4的说法正确的是: ▲
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,即不属于化学变化
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:
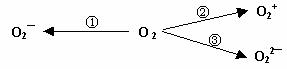
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式:
18.短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外M层电子数目比K层多1个,C―比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子。
(1)A、B、C、D四种元素的名称分别是 、 、 、 。
(2)画出C―和D原子的结构示意图
(3)向B、C两种元素形成的化合物的水溶液里逐滴滴入苛性钠溶液,现象为______________________,写出有关离子方程式________________________________;_________________________________。
17.下列分子结构:CO2、CH4、PCl5、Na2O2、MgF2,其中原子的最外层不能都满足8电子稳定结构的是 ,是离子化合物,且离子个数之比是2:1或1:2的是 。
16.由于金属锑的导电性介于导体与绝缘体之间以及它容易形成合金而具有很多重要用途。下列对锑元素(15Sb)的单质及其化合物的叙述不正确的是( )。
A.金属锑可用于制半导体材料
B.金属锑可用于制合金,以提高金属的硬度
C.金属锑及其化合物往往有毒,使用时要倍加小心
D.在火柴盒侧面涂有的三硫化二锑,用作氧化剂
15.石英玻璃是将纯石英在1600℃高温下熔化,冷却后形成的玻璃体。关于石英玻璃的结构和性质的叙述中正确的是( )
A.石英玻璃属于原子晶体
B.石英玻璃耐高温且能抵抗一切酸的腐蚀
C.石英玻璃的结构类似于液体
D.石英玻璃能经受高温剧变且能抗碱的腐蚀
14.A、B、C、D四种短周期元素,其离子A+、B2+、C-、D2-具有相同的电子层结构,下列判断正确的是( )
A.原子序数由大到小的顺序是:B>A>C>D
B.离子半径由大到小的顺序是:B2+>A+>C->D2-
C.A、B、C、D四种元素可能属于同一周期
D.A、B、C、D四种元素一定属于短周期元素
13.有M、R两种主族元素,已知M2-离子与R+离子核外电子数之和为20,则下列说法不正确的是( )
A.M与R的质子数之和一定等于19
B.M、R可能分别处于第二周期和第三周期
C.M、R可能分别处于第三周期和第二周期
D.M和R的质子数之差可能等于7
12.下列化学键中,都属于极性共价键的是( )
A.共价化合物中的化学键
B.离子化合物中的共价键
C.同种元素原子间的共价键
D.不同元素原子间的共价键
11.阴离子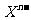 含中子N个,X的质量数为A,则a gX的氢化物中含质子的物质的量是( )
含中子N个,X的质量数为A,则a gX的氢化物中含质子的物质的量是( )
A.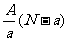 mol
B.
mol
B.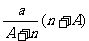 mol
mol
C.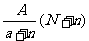 mol
D.
mol
D.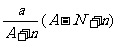 mol
mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com