
1.(2008江苏化学5)镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是 ( )
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是 ( )
A.充电时阳极反应:Ni(OH)2 -e- + OH- == NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
30.(17分)阿魏酸在医药、保健品、化妆品原料和食品添加剂等方面有着广泛的用途,其
结构简式为

⑴阿魏酸可以发生 (填选项字母)。"
a.酯化反应 b.消去反应 c.加成反应 d.氧化反应 e.银镜反应
⑵阿魏酸的一种同分异构体A 可用于制备有机玻璃(聚甲基丙烯酸甲酯),转化关系如下图所示:

己知A 和B都能与FeCl3溶液发生显色反应,B的一溴代物只有一种,A、C能发生银镜反应。
①B的结构简式为____________,C含有的官能团为____________。
②D→E的化学方程式为____________________________________。
③A的结构简式为__________________________________________。
(3)写出所有符合下列条件的阿魏酸的同分异构体的结构简式。
①苯环上有两个取代基,且苯环上的一漠代物只有2 种;
②能发生银镜反应;
③与碳酸氢钠溶液反应可放出使澄清石灰水变浑浊的气体;
④与FeCl3 溶液发生显色反应__________________________________________。
29.(16分)小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3·10H2O),为测定试样中小苏打的质量分数ω(NaHCO3),实验小组同学设计了如下装置进行实验。

[实验过程]
①按图组装仪器,检查装置的气密性;
②将m1g试样放入硬质玻璃管中,装置B、C、D 中药品如图,己知加药品后装置B的质量为m2 g装置C 的质量为m3g;
③关闭活塞a,点燃酒精灯加热试样,直到B 装置中无气泡冒出后,打开活塞a 向装置中通人N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B 的质量为m4g、装置C 的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
⑴装置A中发生反应的化学方程式为____________________________________
⑵装置B的作用为__________________________________________
装置C的作用为________________________________________________
⑶实验过程中通入N2的目的为__________________________________________
⑷用下列各项所提供的数据能计算出ω(NaHCO3)的是____________(填选项字母)。
|
序号 |
a |
b |
c |
d |
e |
|
数据 |
m1、m2、m3 |
m2、m3、 m4、m5 |
m1、m2、m4 |
m1、m4、m5 |
m1、m3、m5 |
⑸实验结束后发现装置A 中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的ω(NaHCO3),若能,则ω(NaHCO3)的计算式为:__________________;若不能,此问不作答。
28.(14 分)在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催 化剂,发生反应N2(g) + 3H2(g)  2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。
 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1 >T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。
27.(13分)X、Y、W、Q都是短周期元素,已知Y、X、W、Q的原子半径依次增大,X、Y 同周期,X、W 同主族,W 原子核内的质子数等于X、Y 原子核内的质子数之和,W 原子最外层电子数是Q 原子最外层电子数的3 倍。
(l)写出下列元素符号:X______,Y______,W______,Q________。
(2)W元素的单质有广泛用途,工业上制备该单质的化学方程式为:
______________________________________________________________________。
(3)Y元素的某种单质通大酸性淀粉碘化钾溶液中,溶液变蓝,同时生成Y元素的另一种单质,该反应的离子方程式为:
______________________________________________________________________。
(4)Y、W、Q三种元素可组成一种盐,其溶液中各离子的浓度从大到小的顺序为
______________________________________________________________________。
13. CuO和Fe2O3混合粉末中加入200 mL 0.5mol/L HNO3溶液,恰好完全反应(忽略溶液体积变化),所得溶液中c(Cu2+) = c(Fe3+)。下列说法中不正确的是
A.混合粉末的质量为3.2g
B.混合粉末中CuO和Fe2O3的物质的量相等
C.混合粉末中CuO 和Fe2O3的质量相等
D.混合粉末溶于硝酸所得溶液中c( NO3-)为0.5 mo/L
12.反应CO(g)+2H2(g)  CH3OH(g)过程中的能量变化
情况如右图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程中的能量变化
情况如右图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
A.该反应的△H= +91kJ/mol
B.加入催化剂,该反应的△H 变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则△H变大
11.甲、乙为短周期元素的单质,丙、丁为氧化物,它们存在如下转化关系:

则甲和乙可以是
 A.钠和氢气 B.镁和碳
A.钠和氢气 B.镁和碳
C.氧气和硫 D.铝和铁
10.用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是
A.20mL 2mol/L FeCl3溶液
B.40mL 1mol/L NaHCO3溶液
C. 20mL 1mol/L Na2SO3溶液
D. 40mL 2mol/L NH4HCO3溶液
9.如下图所示,X、Y、Q、W 都是惰性电极,将电源接通后,W极附近颜色逐渐加深。下列说法中不正确的是
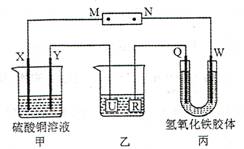
A.电源的M 极为正极
B.甲装置中溶液的pH 减小
C.甲装置的两个电极上都有单质生成且物质的量之比为1︰1
D.欲用乙装置给铜镀银,U 极应该是Ag,电镀液选择AgNO3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com