
7.为下面短文的空缺处选择一个贴切的比喻。
四面是柳枝篱笆,篱笆上爬满豆角秧,豆角秧里还夹杂着喇叭花藤萝,像________,墙里是一棵又一棵的桃树、杏树、山桂树、花红果子树,墙外是一些杨、柳、榆、槐、梨树,就像是墙上的两道铁箍。
A.童年的五彩梦。 B.绣着红花的蓝布裙。
C.二姐出嫁时坐的彩轿。 D.密封的四堵墙。
6.填入下面横线处的句子,与上下文衔接最恰当的一组是
同父亲的关系则完全不同。_______。_______。_______。_______:______。父亲是教育孩子,向孩子指出通往世界之路的人。
①而父亲不体现任何一种自然渊源 ②即代表思想的世界,人所创造的法律、秩序和纪律等事物的世界 ③父亲虽然不代表自然世界,却代表人类生存的另一个极端 ④母亲是我们的故乡,是大自然、大地和海洋 ⑤在最初几年内孩子同父亲几乎没有什么联系,在这个阶段父亲的作用几乎无法同母亲相比
A.②⑤③①④ B.①④②⑤③ C.④①⑤③② D.①④②⑤③
5.依次填入下面一段文字横线处的语句,衔接最恰当的一组是
不过不瓷盘大的一轮弱照,怎么有了它便犹如画龙点睛般让夜景熠熠生辉了。值夜深花睡之际, ;濒临水气氤氲之地, ; , ;
, 。
①它又“荷风摆露,秋月生凉” ②待到金风起兮
③它“长河若带,新月如钩” ④它“花荫寂寂,月色溶溶”
⑤孤照塞外关河隘口 ⑥它“湖波荡漾,月色迷离”
A.①③⑤⑥②④ B.④①②③⑤⑥
C.④⑥⑤③②① D.⑥③②①⑤④
3.依次填入下面一段文字横线处的语句,衔接最恰当的一组是
生活中,没有什么比茅塞顿开更令人激动、更令人受用。 ,茅塞顿开有时来自书本,有时来自别人的言说,有时来自一句诗,有时来自朋友之口。
①当然,这样的时刻并不多见 ②不只是改变,而且使之变得更好 ③但仍然会发生在我们所有人身上 ④茅塞顿开能够改变一个人的人生
A.③①④② B.④①③② C.①③④② D.④②①③
2.依次填入下面一段文字横线处的语句,与上下文衔接最恰当的一组是
阴山以南的沃野不仅是游牧民族的苑囿, 。 ,他们就可以强渡黄河, 。 ,就失去了生存的依据。史载“匈奴失阴山之后,过之未尝不哭也”, 。
①进入汾河或黄河河谷
②如果他们失去了这个沃野
③也是他们进入中原地区的跳板。
④就是这个原因
⑤只要占领了这个沃野
A.③②①⑤④ B.③⑤①②④ C.⑤④①②③ D.②①③⑤④
1.将下面标有序号的六句话依次填到空白处,使之构成衔接连贯的一段话。
遍布华夏的古村落,作为乡土建筑的精华, , , , 。 , ,承载着丰富的历史文化信息,对中国人的价值观念、生活方式的形成产生过深刻的影响。
①却辉映着过辉煌的过去
②鲜明地折射出中国悠久的历史
③具有很高的文物价值
④它们看似陈旧
⑤生动地展现着民族文化的丰富多样
⑥成为了解中国文化和历史的一种重要窗口
14.(12分)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
取25mL甲溶液,向其中缓慢滴入乙溶液15mL,共收集到224mL(标准状况)气体。
取15mL乙溶液,向其中缓慢滴入甲溶液25mL,共收集到112mL(标准状况)气体。
(1)判断:甲是 溶液,乙是 溶液;
(2)实验中所发生反应的离子方程式为: ;
(3)甲溶液的物质的量浓度为 ,乙溶液的物质的量浓度为 ;
(4)将n mL甲溶液与等体积乙溶液按上述两种实验方式进行反应,所产生气体体积为VmL(标准状况下),则V的取值范围是 。
13.(18分)纯净的过氧化钙(CaO2)是白色的结晶粉末,难溶于水,不溶于乙醇、乙醚,常温下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。
已知:①在潮湿空气中CaO2能够分解:CaO2+2H2O== Ca(OH)2+H2O2,
2CaO2+2CO2==2CaCO3+ O2
②CaO2与稀酸反应生成盐和H2O2:CaO2+2H+== Ca2++ H2O2
在实验室可用钙盐制取CaO2·8H2O,再经脱水制得CaO2。CaO2·8H2O在0℃时稳定,在室温时经过几天就分解,加热至130℃时逐渐变为无水CaO2。
其制备过程如下:
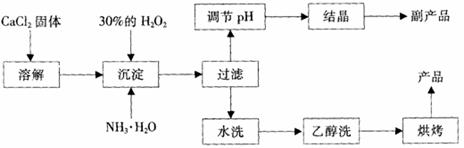
根据以上信息,回答下列问题:
(1)用上述方法制取过氧化钙的化学方程式是 ;
(2)为了控制沉淀温度为0℃左右,在实验室宜采取的方法是 ;
(3)该制法的副产品为 (填化学式),为了提高副产品的产率,结晶前要将溶液的pH调整到合适范围,可加入的试剂是 。
A、盐酸 B、氨水
(4)为了检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加 。
(5)测定产品中CaO2的含量的实验步骤是:
第一步,准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应。
第二步,向上述锥形瓶中加入几滴淀粉溶液。
第三步,逐滴加入浓度为c mol/L的Na2SO3溶液至反应完全,消耗Na2S2O3溶液VmL。(已知:I2 + 2S2O32– = 2I– + S4O62-(无色))
①第三步中说明反应恰好完全的现象是 ;
②CaO2的质量分数为 (用字母表示);
③某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能 (填“不受影响”、“偏低”或“偏高”),原因是
。
12.(12分)根据侯德榜制碱法原理并参考下表的数据,实验室制备纯碱Na2CO3的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得Na2CO3固体。
四种盐在不同温度下的溶解度(g/100g水)表
 |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
100℃ |
|
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
39.8 |
|
NH4HCO3 |
11.9 |
15.8 |
21.0 |
27.0 |
-① |
- |
- |
- |
|
NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
16.4 |
- |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.3 |
77.3 |
注:>35℃ ,NH4HCO3会分解
请回答:
(1)反应温度控制在30-35℃,是因为若高于35℃,则 ;若低于30℃,则 ;为控制此温度范围,采取的加热方法为 。
(2)加料完毕后,继续保温30分钟,目的是 。静置后只析出NaHCO3晶体的原因是 。用蒸馏水洗涤NaHCO3晶体的目的是除去 等杂质(用化学式表示)。
(3)过滤所得的母液中含有 等,需加入
,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1-2滴酚酞指示剂,用物质的量浓度为c(mol∙L-1 )的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点),所用HCl溶液体积为V1 mL;再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V2 mL。写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com