
第一节单项填空(共15小题;每小题1分,共15分)
从每题所给的A、B、C、D四个选项中,选出可以填入空白处的最佳选项,并在答题
卡上将该项涂黑。
21. Jack had feeling of excitement when hearing his article had been published in
school magazine.
A.the;a B.a;the C./;the D the;/
31.(18分)
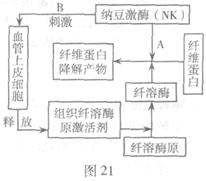 血栓主要由不溶性的纤维蛋白等物质组成。纳豆激酶(NK)是一种在纳豆发酵过程中由纳豆菌产生的蛋白酶,它不但能直接作于纤维蛋白(A过程),还能间接激活体内纤溶酶原(B过程)。图21是有关纳豆激酶溶栓机理简图,请据图回答问题:
血栓主要由不溶性的纤维蛋白等物质组成。纳豆激酶(NK)是一种在纳豆发酵过程中由纳豆菌产生的蛋白酶,它不但能直接作于纤维蛋白(A过程),还能间接激活体内纤溶酶原(B过程)。图21是有关纳豆激酶溶栓机理简图,请据图回答问题:
(1)研究NK直接水解作用:给定纤维蛋白平板,将 滴加其上,若出现相应的溶解圈,则可说明
。
(2)NK的间接作用是通过 激活体内纤溶酶原,增加纤溶酶的量和作用,溶解血栓。
(3)清根据下列出示的实验材料,比较NK与内源性纤溶酶溶栓效果,并在下面横线位置上,补全相应内容。
实验材料:NK溶液、内源性纤溶酶溶液、纤维蛋白块、缓冲液、量筒、试管和秒表。
实验步骤:
|
|
加入物质的成分 |
试管1 |
试管2 |
|
1 |
纤维蛋白块 |
1g |
1g |
|
2 |
缓冲液 |
1mL |
1mL |
|
3 |
纳豆激酶(NK)溶液 |
1mL |
/ |
|
4 |
|
/ |
1mL |
观察记录:观察纤维蛋白块分解情况,并记录分解的 。
请预测一种实验结果并分析:
(4)继续研究NK的化学组成:因为纳豆激酶存在于 ,可直接利用纳豆菌发酵液的上清液,进一步 ,鉴定其化学组成。
(5)由于NK在60℃时迅速失活,可通过 (现代生物技术)提高其热稳定性。





30. (16分)
(16分)
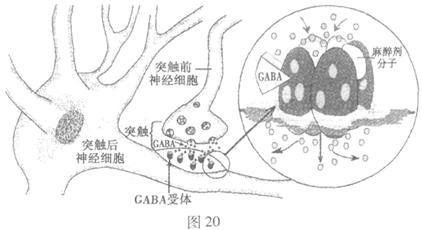
 氨基丁酸(GA-BA)作为哺乳动物中枢神经系统中广泛分布的神经递质,在控制疼痛方面的作用不容忽视,其作用机理如图20所示。请回答有关问题:
氨基丁酸(GA-BA)作为哺乳动物中枢神经系统中广泛分布的神经递质,在控制疼痛方面的作用不容忽视,其作用机理如图20所示。请回答有关问题:
(1)GABA在突触前神经细胞内合成后,贮存在 内,以防止被胞浆内其它酶系所破坏。当兴奋抵达神经末梢时,GABA释放,并与位于图中 上的GABA受体结合。该受体是膜上某些离子的通道。当GABA与受体结合后,通道开启,使 离子内流,从而抑制突触后神经细胞动作电位的产生。上述过程体现出细胞膜具有 功能。如果用电生理微电泳方法将GABA离子施加到离体神经细胞旁,可引起相同的生理效应,从而进一步证明GABA是一种 性的神经递质。
(2)释放的GABA可被体内氨基丁酸转氨酶降解而失活。研究发现癫痫病人体内GABA的量不正常,若将氨基丁酸转氨酶的抑制剂作为药物施用于病人,可缓解病情。这是由于
,从而可抑制癫痫病人异常兴奋的形成。
(3)图中麻醉剂分子嵌入的结构是 ,它的嵌入起到了与GABA一样的功能,从而可 (缩短/延长)该离子通道打开的时间,产生麻醉效果。
29.(16分)
科学家们用长穗偃麦草(二倍体)与普通小麦(六倍体)杂交培育小麦新品种--小偃麦。相关的实验如下,请回答有关问题:
 (1)长穗偃麦草与普通小麦杂交,F1体细胞中的染色体组数为
。长穗偃麦草与普通小麦杂交所得的F1不育,其原因是 ,可用 处理F1幼苗,获得可育的小偃麦。
(1)长穗偃麦草与普通小麦杂交,F1体细胞中的染色体组数为
。长穗偃麦草与普通小麦杂交所得的F1不育,其原因是 ,可用 处理F1幼苗,获得可育的小偃麦。
(2)小偃麦中有个品种为蓝粒小麦(40W+2E),40W表示来自普通小麦的染色体,2E表示携带有控制蓝色色素合成基因的1对长穗偃麦草染色体。若丢失了长穗偃麦草的一个染色体则成为蓝粒单体小麦(40W+1E),这属于 变异。为了获得白粒小偃麦(1对长穗偃麦草染色体缺失),可将蓝粒单体小麦自交,在减数分裂过程中,产生两种配子,其染色体组成分别为 ,这两种配子自由结合,产生的后代中自粒小偃麦的染色体组成是 。
(3)为了确定白粒小偃麦的染色体组成,需要做细胞学实验进行鉴定。取该小偃麦的
作实验材料,制成临时装片进行观察,其中 期的细胞染色体最清晰。
28.(16分)
I.某校化学实验小组探究浓度对化学反应速率的影响,并测定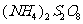 和KI反应的化学反应速率。进行如下实验探究:
和KI反应的化学反应速率。进行如下实验探究:
[实验原理]
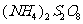 和KI反应的离子方程式为:
和KI反应的离子方程式为:
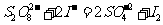 (1)
(1)
平均反应速率的计算式为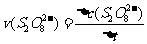 。
。
实验时,向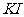 、
、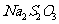 和淀粉指示剂混合溶液中加入
和淀粉指示剂混合溶液中加入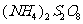 溶液,不断搅拌。
溶液,不断搅拌。
在反应(1)进行的同时,发生反应:
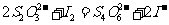 (2)
(2)
反应(1)生成的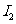 立即与
立即与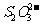 反应,生成无色的
反应,生成无色的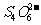 和
和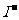 。
。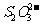 耗尽时,反应(1)继续生成的
耗尽时,反应(1)继续生成的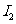 才与淀粉作用呈现蓝色。从加入
才与淀粉作用呈现蓝色。从加入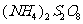 溶液到出现蓝色的时间为
溶液到出现蓝色的时间为 。
。
[实验内容]
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
|
实验编号 |
① |
② |
③ |
④ |
⑤ |
|
|
试剂 用量 (mL) |
0.20 mol·L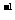 (NH4)2S2O8 溶液 (NH4)2S2O8 溶液 |
20.0 |
10.0 |
b |
20.0 |
20.0 |
0.20 mol·L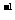 KI溶液 KI溶液 |
20.0 |
20.0 |
20.0 |
10.0 |
5.0 |
|
0.010 mol·L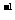 Na2S2O3溶液 Na2S2O3溶液 |
a |
8.0 |
8.0 |
8.0 |
8.0 |
|
|
0.2%淀粉溶液 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
|
0.20 mol·L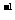 KNO3溶液 KNO3溶液 |
0 |
0 |
0 |
10.0 |
c |
|
0.20 mol·L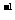 (NH4)2SO4 溶液 (NH4)2SO4 溶液 |
0 |
10.0 |
15.0 |
0 |
0 |
|
20℃时,反应时间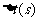 |
32 |
67 |
130 |
66 |
135 |
|
|
为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 |
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是 。
(3)第①组实验的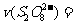 mol·(L·s)
mol·(L·s)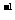 。
。
(4)根据上表数据分析,可以得到的结论有(写出一条即可) 。
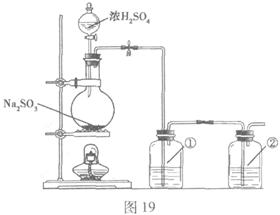
II.实验小组查资料得知,向含有NaCO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:
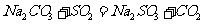
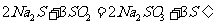
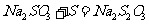
该小组根据上述原理设计如图19所示装置制备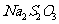 。
。
(1)实验应避免有害气体排放到空气中。装置①、②中盛放的试剂依次是① ;② 。
(2)实验过程中,随着气体的通入,装置①中有大量黄色固体析出,继续通入气体,可以观察到的现象是 。
(3)反应结束后,从制得的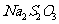 稀溶液中得到
稀溶液中得到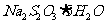 晶体的主要操作包括: 。
晶体的主要操作包括: 。
27.(14分)
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0-6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
某科研小组用电浮选凝聚法处理污水,设计装置如图18所示:
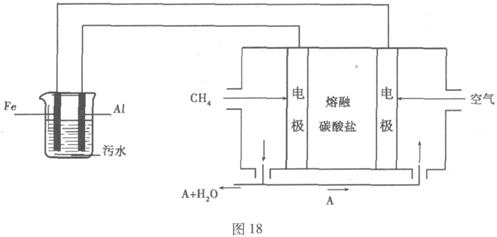
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。
a.H2SO4 b.BaSO4 c.N2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极的电极反应分别是① ;
②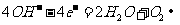 。
。
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。
已知负极的电极反应是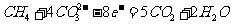 。
。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况) L。
26. (12分)
(12分)
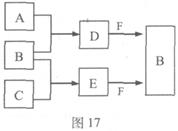
A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图17 (反应条件和部分产物略去)。试回答:
(1)E的电子式是 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是 。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是 。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+) 。
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是 。
(已知甲醇的燃烧热 ,氢气的燃烧热
,氢气的燃烧热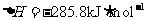 )
)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com