
2.原子晶体:
(1)概念: 。
(2)性质特征: 。
(3)重要判断依据: 。
(4)影响熔沸点高低的因素: 。
晶体: 。
1.离子晶体:
(1)概念: 。
(2)性质特征: 。
(3)重要判断依据: 。
(4)影响熔沸点高低的因素: 。
14.已知一个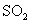 分子的质量为nkg,一个
分子的质量为nkg,一个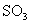 分子的质量为mkg(假设两种分子中硫原子、氧原子分别具有相同的中子数)。若以硫原子质量的
分子的质量为mkg(假设两种分子中硫原子、氧原子分别具有相同的中子数)。若以硫原子质量的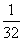 作为标准,试计算
作为标准,试计算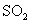 的式量为多少?
的式量为多少?
13、在下列原子(或离子)结构简图上表示的微粒中(用元素符号填空)
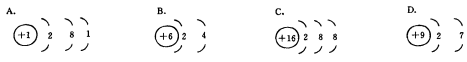
(1)半径最小的是 ;(2)具有最低负化合价的是 ;(3)只有还原性的是 ;(4)只有氧化性的是 ;(5)得失电子能力均最弱的是 .
12.在1911年前后,新西兰出生的物理学家--卢瑟福把一束变速运动的a-粒子(质量数为4的带2个正电荷的质子粒),射向一片极薄的金箔。他惊奇地发现,过去一直认为原子是“实心球”,而由这种“实心球”紧密排列而成的金箔竟被大多数a-粒子畅通无阻地通过,就像金箔不在那儿似的,但也有极少数的a-粒子发生偏转,或被笔直地弹回。根据以上实验现象能得出关于金箔中Au原子结构的一些结论,试写出其中的三点:
(1)___________________ (2)___________________ (3)__________________
11.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图为________ 。
10.结构示意图为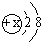 的微粒,其x值可能为________
、________、________、________、________、________,相应的微粒符号分别为________、________、________、________、________、________。
的微粒,其x值可能为________
、________、________、________、________、________,相应的微粒符号分别为________、________、________、________、________、________。
9.与氖原子核外电子数相同的双原子分子是________;与氖原子核外电子数相同的三原子分子是________;与氖原子核外电子数相同的四原子分子是________ ;与氖原子核外电子数相同的五原子分子是________。
8.19世纪末,人类开始揭开原子内部结构的秘密,最先发现电子的科学家是( )。
A.法国化学家拉瓦锡 B.英国物理学家汤姆逊
C.意大利物理学家阿伏加德罗 D.英国化学家道尔顿
7.X、Y两种元素组成的两种化合物甲和乙,已知:甲的化学式为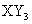 ,甲中X的质量分数为80%,乙中Y的质量分数为25%,则乙的化学式是( )。
,甲中X的质量分数为80%,乙中Y的质量分数为25%,则乙的化学式是( )。
A.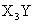 B.
B.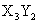 C.
C.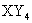 D.
D.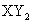
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com