
4.调味剂是日常生活中离不开的食品添加剂,有关其说法正确的是( )
A.食盐是咸味剂,食盐属于离子晶体,它的溶液是强电解质,
B.食醋的主要成分是醋酸,将一定量的醋酸溶液稀释,溶液中各离子的浓度都减小
C.味精的主要成分是谷氨酸钠,向其中加入盐酸可得谷氨酸,谷氨酸既能与NaOH反应,又能与HCl反应
D.木糖醇(C5H12O5)是一种甜味剂,它属于多羟基化合物,与葡萄糖互为同系物
3.下列黄色不属于因化学反应而产生的现象的是( )
A.无色试剂瓶中的浓HNO3呈黄色 B.久置的KI溶液呈黄色
C.鸡蛋白遇浓HNO3 呈黄色 D.在普通玻璃导管口点燃纯净H2时,火焰呈黄色
2.现有两种高聚物A、B,A能溶于氯仿等有机溶剂,B不溶于任何溶剂,加热不会变软或熔融,则下列叙述中不正确的是( )
A.高聚物A具有热塑性 B.高聚物B具有热固性
C.高聚物A一定是体型高分子化合物材料 D.高聚物B一定是体型高分子化合物材料
1.1997年,英国的“克隆羊”备受世界关注。“克隆羊”的关键技术之一是找到一些特殊的酶,这些酶能激活普通体细胞使像生殖细胞一样发育成个体。有关酶的叙述错误的是( )
A.酶是具有催化作用的蛋白质 B.酶的催化作用具有选择性和专一性
C.高温或重金属盐能降低酶的活性 D.酶只有在强酸性或强碱性条件下才能发挥作用
30.(18分)香豌豆是雌雄同花植物,有多种性状,各种性状的遗传方式各有差别。
(1)如果基因型RR的植株呈深绿色,基因型Rr的植株呈浅绿色,基因型rr的植株呈白色。深绿色和浅绿色植株的繁殖和生存能力相似,而白色植株会在幼苗阶段死亡。基因型为RR的植株在遮光条件下茎叶为黄白色,这是因为光照影响了 ▲ 合成,说明生物性状的表现是 ▲ 的结果。现有一株浅绿色的植株作亲本进行自花授粉得到F1,F1自花授粉得到F2,F2的成熟植株中浅绿色植株所占的比例为 ▲ 。
(2)如果该植株的花有红色、紫色和白色,该性状受两对基因控制,同时有E和F基因的植株开红花,无E和F基因的植株开白花,只有E基因或F基因时开紫花。有两株开紫花的植株杂交,后代出现开红花:紫花:白花=1:2:1,请你对这个现象用遗传图解作出解释。
(3)若上述基因型为EEFF的红花豌豆具有更强的抗逆性,且种子中蛋白质含量相对高,如何利用紫花豌豆快速培育此品种,写出简单的育种方案。(要求叙述简洁,条理清楚)

 台州市2010年高三年级第一次调考试题
台州市2010年高三年级第一次调考试题
29.(26分)回答下列Ⅰ、Ⅱ小题
Ⅰ.(14分)右图为某一森林生态系统中红松的种群密度
的变化示意图。据图回答:
(1)图甲中A→B的种群密度变化率为 ▲ 株/(100m2·a)
(以“+”代表增强,以“-”代表减少)。从图甲中B
→C的变化可以看出,在该年份中红松种群的年龄组成
的特点用图乙哪项曲线可以表示 ▲
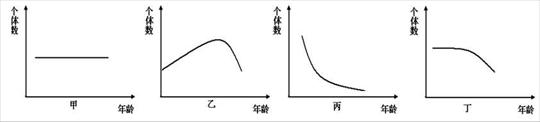
第29题I(1)乙图
(2)分布型是指种群中个体的空间配置格局。由于红枫植株间争夺树冠空间和根部空间所进行的竞争,往往出现 ▲ 分布。森林生态系统中两个物种利用同一资源就会发生生态位重叠,但生态位重叠本身并不一定伴随竞争,只有当 ▲ 时才会发生竞争。
(3)由于一场大火破坏了原有生态系统,但经过一段时间后又会蔚然成林,这一过程称为▲ 。该过程中,生产者单位时间内固定太阳能的变化为 ▲ ,当群落发展到一定平衡状态,演替不再进行,这个最终平衡状态就叫 ▲ 。
Ⅱ(12分)低温和高温都会导致植物细胞受到伤害。某研究小组的同学欲设计实验方案研究高温和低温对小麦的伤害,假设你是该小组中的一员,请完善下列实验方案并回答相关问题。
(1)实验原理:
当植物组织受到不良条件如高温、低温的影响时,细胞内含物会有不同程度的外渗,使外部溶液的电导度增大,电导度的大小可以用电导仪进行检测(电导仪非常灵敏,各种杂质以及温度都会影响测量结果,从而带来实验误差),透性变化愈大,表示受伤害愈重,抗逆性愈弱。
(2)实验材料:长势相同的小麦幼苗
(3)仪器用具:电导仪、冰水、水浴锅、烧杯、量筒、蒸馏水
(4)实验步骤:
第一步:取小麦幼苗30株,去除残留胚乳,用蒸馏水反复冲洗三次;
第二步:取四只小烧杯,分别加入20mL蒸馏水,编号为1、2、3、4;
第三步:
…
(5)实验分析:
①高温和低温导致外部溶液电导度增大的最可能原因是 ▲ 。
②实验的第一步中要去除残留胚乳,并用蒸馏水冲洗的目的是 ▲ 。
28.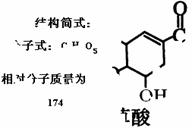 (15分)实验室一试剂瓶标签严重破损,只能隐约看到一部分:
(15分)实验室一试剂瓶标签严重破损,只能隐约看到一部分:
(1)该物质(M)分子式为: ▲
(2)A与M互为同分异构体,B无支链,B与羧酸和醇都能发生酯化反应,A在一定条件下能发生如下转化:
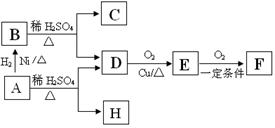
C与F互为同系物,H能使Br2/CCl4溶液褪色,H物质得到的1H-NMR谱中有5个吸收峰。
①A的结构简式为 ▲ 。
②写出一个证明E中官能团的化学方程式 ▲ ,反应类型 ▲ ;写出C与D反应形成高聚物的化学方程式 ▲ ,反应类型 ▲ 。
③写出与H官能团种类和数目都相同的所有同分异构体 ▲ 。
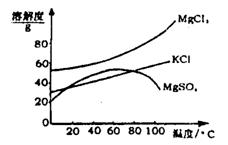
27.(15分)我国柴达木盆地拥有丰富的盐矿资源,其中的液体矿床以钾矿为主,伴生着镁、溴等多种成分。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
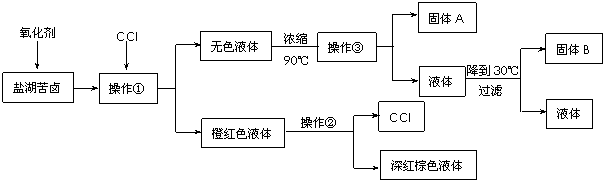
 请根据以上流程,回答相关问题:
请根据以上流程,回答相关问题:
(1)操作①需要的玻璃仪器有 ▲ ;固体A名称是 ▲ 。检验操作①得到的无色溶液中Cl-的方案是: ▲ 。
(2)工业上以浓缩海水为原料提取溴的部分过程如下:
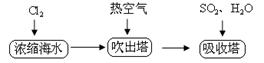
该研究小组在参观了溴的生产流程后,准备以盐湖苦卤为原料设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
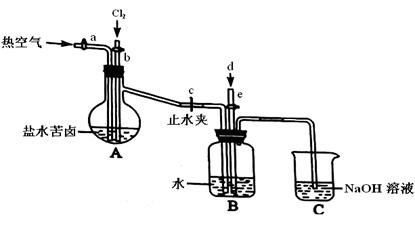
①检验装置A气密性的方法是 ▲ 。
②该装置中的橡胶制品均要用特定的材料保护,其原因是 ▲ 。
(3)某同学提出一种新的方案,对上述操作①后无色溶液进行除杂提纯,其方案流程如下:

有关资料:
|
化学式 |
Ca(OH)2 |
CaSO4 |
BaCO3 |
BaSO4 |
MgCO3 |
Mg(OH)2 |
|
Ksp |
1.0×10一4 |
7.1×10一5 |
8.1×10一9 |
1.08×10一10 |
3.5×10一5 |
1.6×10一11 |
1试剂B的化学式为 ▲ 。
2有同学提出从经济上考虑可以用石灰乳代替试剂A进行实验,经讨论,其他同学一致认为该提议不可行,他们的理由是 ▲ 。
3实验过程中,若要确保Mg2+完全除尽,用广泛pH试纸测定溶液的pH应≥ ▲ 。(若离子浓度小于10-5mol·L-1可视作已被完全除尽)
26.(14分)DME(二甲醚、CH3OCH3)是一种重要的清洁能源,可作为柴油的理想替代燃料和民用燃料,被誉为“二十一世纪的新能源”。另外,二甲醚还被广泛用作致冷剂、气雾剂以及有机化工中间体。
(1)工业上一步法制二甲醚的生产流程如下:
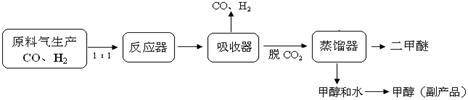
在一定的温度(230-2800C)、压强(2-10MPa)和催化剂作用下,反应器中进行下列一些反应:
CO(g)+2H2(g) CH3OH(g) △H= -90.7kJ·mol-1
CH3OH(g) △H= -90.7kJ·mol-1
2CH3OH(g) CH3OCH3(g)+H2O(g) △H= -23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H= -23.5kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2(g)
△H= -41.2kJ·mol-1
CO2(g)+H2(g)
△H= -41.2kJ·mol-1
①反应器中总反应式可表示为:3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),则该反应的△H = ▲ 。
CH3OCH3(g)+CO2(g),则该反应的△H = ▲ 。
②在生产过程中反应器必须要进行换热,以保证反应器的温度控制在230-2800C,其原因是 ▲ 。
(2)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H>0。判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是 ▲ 。
CH3OCH3(g)+3H2O(g) △H>0。判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是 ▲ 。
A.容器中密度不变 B.容器内压强保持不变
C.v(CO2)︰v(H2)=1︰3 D.单位时间内消耗2molCO2,同时消耗1mol二甲醚
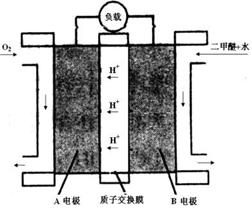 (3)右图为二甲醚燃料电池的工作原理示意图。请回答下列问题:
(3)右图为二甲醚燃料电池的工作原理示意图。请回答下列问题:
①A电极是 ▲ 极。
②B电极上发生的电极反应式是 ▲ 。
③若燃料电池中通入二甲醚(沸点为-24.9 ℃)的速率为1.12L/min(标准状况),以该燃料电池作为电源电解2 mol·L-1CuSO4溶液500mL,则通电30秒钟后理论上在阴极可析出金属铜 ▲ g(假设整个过程中,能量利用率为75%)。
25.(14分)元素A、B、C、D、E、F的原子序数依次增大,前五种元素为短周期元素,F元素为第四周期元素,且D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g·L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):
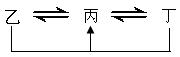
其中,均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;无论是含有D元素还是含有F元素,相邻的乙与丙或丙与丁两两间互不发生化学反应。请回答下列问题:
(1)写出化合物甲的电子式: ▲ 。
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式 ▲ ;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式 ▲ 。
 (3)复盐是指由2种或2种以上阳离子和一种阴离子组成的盐。请写出由A、B、C、E、F元素组成的一种具有还原性的复盐戊的化学式 ▲ 。化合物己是制备复盐戊的必须物质之一,工业上常用氧气、水和FE2来制取,并得到E的高价态化合物,请写出工业上由FE2制取化合物己的化学方程式 ▲ 。
(3)复盐是指由2种或2种以上阳离子和一种阴离子组成的盐。请写出由A、B、C、E、F元素组成的一种具有还原性的复盐戊的化学式 ▲ 。化合物己是制备复盐戊的必须物质之一,工业上常用氧气、水和FE2来制取,并得到E的高价态化合物,请写出工业上由FE2制取化合物己的化学方程式 ▲ 。
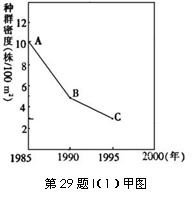
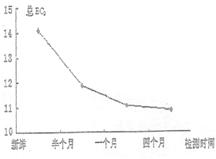
(4)EC2是啤酒中含量较低而又重要的组分,大部分是在发酵过程中产生的,是啤酒内源抗氧化物的一种,它的存在量与啤酒的抗氧化性有很大的关系。右图是某啤酒样品不同时间段总EC2的变化情况,请运用所学的知识解释啤酒样品中总EC2随时间变化的主要原因是 ▲ 。
(5)由A、C元素组成化合物庚和A、E元素组成的化合物辛,式量均为34。其中庚的熔沸点高于辛,其原因是: ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com