
25.(5分)将一块质量为8.5g的铁合金(成分为铁和碳)放入烧杯中,再向烧杯中加入91.9g稀H2SO4,恰好与铁合金中的铁完全反应(碳不溶于稀H2SO4),所得氢气的质量为0.3g。已知含碳量高于2%的铁合金为生铁,含碳量低于2%的铁合金为钢,试根据计算回答:
(1)该铁合金是生铁还是钢?
(2)反应后所得溶液中溶质的质量分数是多少?
24.(4分)实验室中盛装还未使用的浓硫酸试剂瓶上的
标签如右图所示,根据有关信息计算:
(1)该试剂瓶中含硫酸的质量是 g;
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,
需要这种浓硫酸 g。
23.(12分)小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
[查阅资料]市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”[platinum]------元素符号Pt。小红结合化学课上学习的金属活动性顺序,展开了下列实验活动。
(1)鉴别两种白金,她的方法可能是 ;
(2)探究Zn、Ni(镍)、铜的活动性顺序。
[作出假设]对三种金属的活动性顺序提出可能的假设①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③ …………
[查阅资料]小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应。
|
|
OH- |
NO3- |
SO42- |
Cl- |
|
Ni2+ |
不 |
溶 |
溶 |
溶 |
[设计实验]同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象。
[记录现象]请帮助小红把实验现象填写完整
|
金属 |
Ni |
Zn |
Cu |
|
与盐酸反应的现象 |
气体产生缓慢 金属逐渐溶解 |
气体产生激烈 金属迅速溶解 |
|
[得出结论]原假设中正确对待的是 (填序号)
写出镍与盐酸反应的化学方程式 。
[结论应用]
①根据探究结果,请你预测镍与硫酸铜溶液 (填“能”或“不能”)反应,
理由是 。
②除小红的实验设计外,你能否象小红一样,设计另一组实验,也这样一次验证上述假设的正确与否,你的设计所用的一组物质的化学式是 (只写出一组即可)。
22.(6分)下图是配制50g质量分数为5% 的氯化钠溶液的相关操作过程示意图:

① ② ③ ④ ⑤
试回答:
(1)配制该氯化钠溶液的正确的操作顺序是 ( )
A.④⑤①②③ B.①②③④⑤ C.③④①②⑤ D.②①④③⑤
(1)⑤操作中应称量氯化钠的质量是 g 。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 。
(2)②操作应选用 mL 的量筒(从10 mL、100 mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的 处保持水平。
(3)③操作的作用是 。
21.(7分)联合钢铁工业的基本生产流程示意图如下:
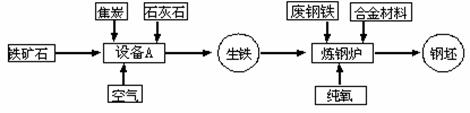
请回答下列问题:
(1)写出设备A 的名称: ;
(2)写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:
;
(3)应用化学原理分析,工业炼钢时用纯氧而不用空气的原因是:
;
(4)铁粉与生石灰都是常用的干燥剂,现欲用化学方法检验某食品袋中的干燥剂究竟是其中的哪一种?请你简述方法和现象:
(5))某赤铁矿石中含Fe2O380%,用3000 t这种矿石,可炼出含杂质4%的生铁质量 。
20.(4分)下面的表格中列出了氯化铵在不同温度下的溶解度:
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度/g |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
(1)从表中可得到的一条信息是___________________________________。
(2)在20℃时,向100g水中加入50g氯化铵,形成氯化铵的______(填“饱和”或“不饱和“)溶液,将其温度升高至60℃时,溶液的质量为________g,该溶液中溶质与溶剂的质量比为______________。
19.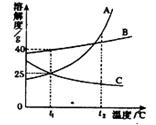 (3分)右图是A、B、C三种物质的溶解度曲线,请据图回答:
(3分)右图是A、B、C三种物质的溶解度曲线,请据图回答:
(1)t1℃时,A物质的溶解度为 ;
(2)t2℃时,将A、B、C三种物质的饱和溶液,
①均恒温蒸发等质量的水,析出晶体由多到少的顺序为 ;
②均降温致t1℃时,欲使A和C的溶液中溶质的质量分数相等,则可以采取的一种措施是 。
18.(6分)设计除去杂质的实验方案,填写在下表(括号中为杂质)
除杂质的实验方案
|
混合物 |
除去杂质的化学方程式 |
主要操作步骤 |
|
铜粉(锌粉) |
|
|
|
FeSO4溶液(CuSO4) |
|
|
17.(5分)某学生在探究活动中,把少量的生铁放入烧杯中并注入一定量的稀硫酸中,能观察到的现象有: ①生铁表面有 产生,②溶液逐渐变 ,完全反应后烧杯底部
有 出现。请写出有关化学方程式 。
16. 向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加人一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
A .滤液中一定含Ag+、Cu2+、Zn2+、Fe2+ B .滤液中一定含Fe2+ ,可能含Zn2+ C .滤液中一定含Fe2+ ,Zn2+,不含Cu2+,Ag+ D .滤液中一定含Zn2+、Fe2+,可能含Cu2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com