
8.(2009·理综辽宁、宁夏卷,13)在一定温度下,反应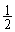 H2(g)+
H2(g)+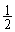 X2(g)
X2(g) HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
A.5% B.17%
C.25% D.33%
7.(2008江苏化学17)(10分)工业上制备BaCl2的工艺流程图如下:
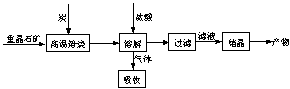
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s) 4CO(g) + BaS(s)
△H1 = 571.2 kJ·mol-1 ①
4CO(g) + BaS(s)
△H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
。
=
。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s) + CO2(g) 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
6.(2007年高考广东化学卷·26) (12分)羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料,其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
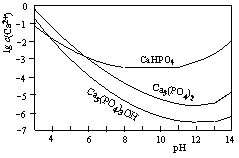
3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
⑴完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O=Ca5(PO4)3OH↓+________+_______,
②5Ca(OH)2+3H3PO4=__________________________。
⑵与方法A相比,方法B的优点是_________________。
⑶方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是__________。
⑷图中所示3种钙盐在人体中最稳定的存在形式是_____________(填化学式)。
⑸糖黏附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因________________。
5.(2008广东化学9)已知Ag2SO4的KW 为2.0×10-3,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO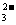 浓度随时间变化关系如右图(饱和Ag2SO4溶液中c(Ag+)=0.034mol·L-1)。若t1时刻在上述体系中加入100 mL. 0.020 mol·L-1 Na2SO4 溶液,下列示意图中,能正确表示t1时刻后Ag+和SO
浓度随时间变化关系如右图(饱和Ag2SO4溶液中c(Ag+)=0.034mol·L-1)。若t1时刻在上述体系中加入100 mL. 0.020 mol·L-1 Na2SO4 溶液,下列示意图中,能正确表示t1时刻后Ag+和SO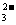 浓度随时间变化关系的是
浓度随时间变化关系的是
4.(2008·山东理综卷,15,)某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是 ( )

提示:BaSO4(s) Ba2+(aq)+SO42 -(aq)的平衡常数:Ksp = c(Ba2+)·c(SO42 -),称为溶度积常数。
Ba2+(aq)+SO42 -(aq)的平衡常数:Ksp = c(Ba2+)·c(SO42 -),称为溶度积常数。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
3.(2007广东化学15)下列各溶液中,微粒的物质的量浓度关系正确的是 ( )
A.0.1mol·L-1Na2CO3溶液:c(OH-)= c(HCO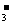 )+ c(H+)+2 c(H2CO3)
)+ c(H+)+2 c(H2CO3)
B.0.1mol·L-1NH4Cl溶液:c(NH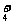 )= c(Cl-)
)= c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)> c(CH3COO-)> c(H+)+ c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)= c(NO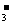 )
)
2.(2007山东理综10)物质的量浓度相同时,下列既能跟NaOH溶液反应、又能跟盐酸溶液中pH最大的是 ( )
A.Na2CO3溶液 B.NH4HCO3溶液
C.NaHCO3溶液 D.NaHSO4溶液
1.(2008海南化学9)下列离子方程式中,属于水解反应的是 ( )
A.HCOOH+H2O HCOO-+H3O+
HCOO-+H3O+
B.CO2+H2O HCO
HCO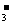 +H+
+H+
|
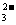 +H2O
+H2O HCO
HCO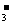 +OH-
+OH-
D.HS-+H2O S2-+H3O+
S2-+H3O+
34.(10分)图甲为测定光合作用速率的装置(CO2缓冲液能维持装置内CO2浓度恒定),在不同强度的光照条件下测得的单位时间内气体体积的变化量如乙图所示,请据图回答:
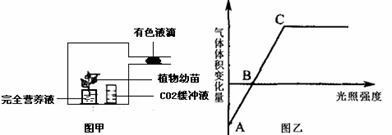
(1)图乙中的气体是在叶绿体内的________上生成的,可以在线粒体中与______结合。
(2)若将图甲中的CO2缓冲液换成1%的NaOH溶液,则植物幼苗叶绿体中C5含量将_____,产生NADPH的速率将_________。
(3)若将图甲中完全培养液换成换成钙元素不足的培养液,植物的新叶是否表现缺钙症状?_____________,理由是_____________________________。
(4)改变光照强度,直至液滴不再移动,保持此光照强度下,将图甲中的阳生植物换成阴生植物,如果其他条件不变,则有色液滴将如何移动?_______,理由是__________。
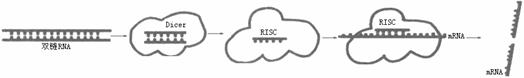
33.(11分)美国科学家安德鲁·法尔和克雷格·梅洛因为发现“RNA干扰机制--双链RNA沉默基因”而获得2006年诺贝尔生理学或医学奖。RNA干扰的机制如下:双链RNA一旦进入细胞内就会被一个称为Dicer的特定的酶切割成2l-23个核苷酸长的小分子干涉RNA(SiRNA)。SiRNA片断与一系列酶结合组成诱导沉默复合体(RISC)。激活的RISC通过碱基配对结合到与SiRNA同源的mRNA上,并切割该mRNA,造成蛋白质无法合成(如下图所示)。回答下列问题:



|





(1)RNA干扰技术具有广泛的应用前景。如用于乙型肝炎的治疗时,可以根据乙肝病毒基因中的碱基(脱氧核苷酸)序列,人工合成与之相应的_______________,注人被乙肝病毒感染的细胞,达到抑制乙肝病毒繁殖的目的。
(2)根据RNA干扰机理,RNA干扰能使相关基因“沉默”,其实质是遗传信息传递中______过程受阻。有科学家将能引起RNA干扰的双链RNA的两条单链分别注入细胞,结果却没有引起RNA干扰现象,请据图分析最可能的原因是______________________________。
(3)基因突变属于可遗传的变异,如果有一亲本的DNA上某个碱基对发生改变,而其子代的性状却没有发生改变。请给出4种可能的原因:
①_________________________________________________________________
②_________________________________________________________________
③_________________________________________________________________
④_________________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com