
6.为了除去酸性AlCl3溶液中的Cu2+,下列实验步骤顺序和试剂都正确的是( ) ①通CO2 ②加盐酸 ③加过量NaOH溶液 ④加AlCl3溶液 ⑤过滤
A.③⑤② B.③⑤①⑤② C.③⑤④⑤② D.以上都不正确
课外作业
5.下列有关实验所选用的试剂能达到目的是( ) A.证明NaHCO3溶液中混有苏打用澄清石灰水 B.证明SO2中混有CO2用澄清石灰水 C.证明AgNO3溶液中混有Al(NO3)3用氨水 D.除掉C2H6中的C2H4用酸性KMnO4溶液
4.下列实验能成功的是( ) A.用食盐、MnO2和浓H2SO4共热制Cl2 B.将白P放在敞口试管内加热,冷却得红P C.足量Cl2通入FeCl2 溶液后,将溶液蒸干得到FeCl3 D.将Cu丝伸入热的硫蒸气中得到CuS
3.都能用4mol/L NaOH溶液进行喷泉实验的一组气体是 A.HCl和CO2 B.NH3和CH4 C.SO2和CO D.NO和HBr
2.一瓶气体,可能含有H2S、CO2、HCl、HBr、SO2中的几种,将其通入氯水中,
得无色透明液,将此溶液分成两份,向一份中加入盐酸酸化的BaCl2溶液有白色沉
淀;另一份中加入HNO3酸化的AgNO3溶液有白色沉淀,则下列结论正确的是( ) A.肯定有CO2和SO2 B.可能有HBr、CO2 C.肯定没有HBr、H2S、HCl D.以上结论均不正确
1.某工厂排放的酸性废液里含有游离氯。Cl2可氧化Na2SO3,要除去游离氯并中
和其酸性,正确的方法是 A.先加适量的Na2SO3溶液,再加适量Na2CO3溶液 B.先加适量的Na2CO3溶液,再加适量Na2SO3溶液 C.先加过量的Na2SO3溶液,再加适量Na2CO3溶液 D.先加过量的Na2CO3溶液,再加适量Na2SO3溶液
2.(04年广东20)海水的综合利用可以制备金属镁,其流程如下图所示:
水,重结晶


 粗盐
精盐
粗盐
精盐
海水 蒸发
盐酸,浓缩 脱水 电解
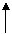




 母液 Mg(OH)2
MgCl2•6H2O MgCl2 Mg
母液 Mg(OH)2
MgCl2•6H2O MgCl2 Mg
煅烧 水

 贝壳
CaO
石灰乳
贝壳
CaO
石灰乳
(1) 若在空气中加热MgCl6•6H2O,生成的是Mg(OH)Cl或MgO,写出相应
反应的化学方程式: ,
用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热
MgCl6•6H2O时,能得到无水MgCl6,其原因是 。
(2)Mg(OH)2中混有的Ca(OH)2应怎样除去?写出实验步骤:
。
(3)实验室中将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作
中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的目的:
 溶解时:
;
溶解时:
;
过滤时: ;
蒸发时: 。
思维方法: 。
展望高考:
[巩固练习]
课堂反馈
.[例题解析]
[例1] 下图虚线框中的装置可用来检验浓硫酸与木炭粉的加热条件下反应产
生的所有气体产物,填写下列空白:
(1)
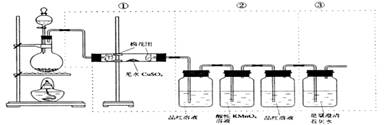 如果装装置中①、②、③三部分仪器的连接顺序改为②、①、③,则可
如果装装置中①、②、③三部分仪器的连接顺序改为②、①、③,则可
以检出的物质是____________;不能检出的物质是____________。
(2) 如果将仪器的连接顺序变为①、③、②,则可以检出的物质是_______;
不能检出的物质是____________。
(3) 如果将仪器的连接顺序变为②、③、①,则可以检出的物质是_______;
不能检出的物质是____________。
解题思路: 。
易错点: 。
[例2] 水蒸气通过灼热的煤所产生的混和气,其主要成份是CO、H2还含有CO2
和水蒸气.请用下列装置设计一个实验,以确认上述混和气中含有CO和H2。
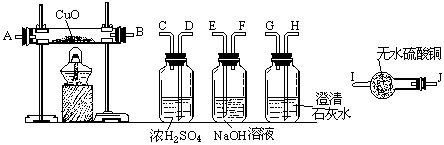

(1) 连接上述装置的正确顺序是:(填各接口的代码字母)
混和气→( )( )接( )( )接( )( )接( )( )接( )( ).
(2)确认混和气中含有H2的实验现象是 其理由是 .
解题思路: 。
易错点: 。
[考题再现]
1.(04年江苏20)有两个实验小组的同学为探究过氧化钠和二氧化硫的反应,
都将纯净干燥的二氧化硫通过盛有过氧化钠的反应管,用氢氧化钠溶液将余气
吸收后,放出的气体可使带余烬的木条复燃。请回答下列问题:
(1)第一小组同学认为过氧化钠与二氧化硫反应生成了亚硫酸钠和氧气,
该反应的化学方程式为: 。
(2)请设计一种实验方案证明该反应生成的白色固体中含有亚硫酸钠:
。
(3)第二小组同学反应除生成了亚硫酸钠外,还有硫酸钠生成。为检验是否有
硫酸钠生成,他们将所得固体溶解于水,加入氯化钡溶液,生成白色沉淀,加
入稀硝酸,还有部分白色沉淀不溶解,证明有硫酸钠生成。请你评价上述方案
是否合理? 。并简要说明两点理由:
① ;② 。
思维方法: 。
展望高考:
6.未知物的检验思路:
(1)先物理后化学:如 ;
(2)先常温后加热:如 ;
(3)先分组后逐一:如 。
5.进行物质检验时对反应的一般要求:
(1) 反应要有明显的外部特征:
常见阳离子在溶液中的特殊颜色: ;
常见阴离子在溶液中的特殊颜色: 。
溶液中的沉淀物常呈现的特殊颜色:
白色 ;
 黑色
;
黑色
;
红褐色 ;砖红色 ;黄色 ;浅黄色 ;
蓝色 。
常温下常见气体的颜色和气味:
无色无味气体: ;
无色有刺激性气味的气体: ;
红色有刺激性气味的气体: ;黄绿色有刺激性气味的气体: ;
无色有腐蛋气味的气体: ;无色有果香味的气体: 。
(2) 反应要在适宜的酸碱度、浓度和温度下进行:
①溶液酸碱度对检验反应的影响:如检验Fe3+、Al3+、Cu2+、Ag+、Zn2+等离
子都应在 性溶液中进行;检验醛基时应在 性溶液中进行。
②溶液浓度对检验反应的影响:根据检验反应的灵敏度的高低不同,对被检
离子浓度大小的要求不同。
③溶液温度对检验反应的影响:对室温下速率较慢的反应,常需加热;
而有的物质溶解度会随温度升高而增大,此时不能在热溶液中进行反应。
(3)检验反应常需排除干扰物质的影响,如:
①用Ba2+检验SO42-时,要排除 等的干扰,方法是 ;
②用Ag+检验Cl-、Br-、I-时,要先加入 以排除 的干扰;
③用SO42-检验Ba2+时,要先加入 以排除 的干扰。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com