
27.如图所示,进行中和反应实验:
(1)在A的实验中,滴入酚酞试液后,溶液由无色变为 色。
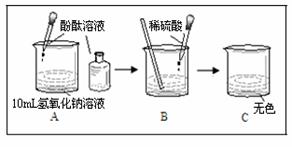 (2)B中发生中和反应的化学方程式是:
(2)B中发生中和反应的化学方程式是:
_______________________________ _____。
(3)写出C的溶液中溶质可能存在的几组情况 _________________________ 。(用化学式表示)
(4)使100g氢氧化钠恰好中和,需滴加50g20%硫酸的稀硫酸溶液,求该氢氧化钠溶液中溶质的质量分数?(列式计算)
26.根据实验回答:(1)写出图中a、b仪器名称:a_______________ ; b_________________。
(2)图A中的操作错误是 __________________________________ 。
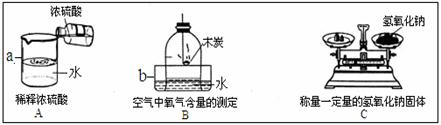
(3)用图B的方法测定空气中氧气的体积分数结果偏低,改进的措施是 。
(4)图C称量氢氧化钠固体的方法有 处错误。
25.某化工厂为综合利用生产过程中的副产品CaSO4,与相邻化肥厂联合设计了制备(NH4)2SO4的工艺流程(如图所示)
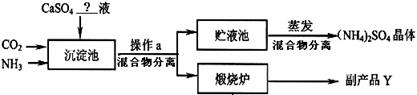 已知:上述流程中,沉淀池中发生的主要化学反应为:
已知:上述流程中,沉淀池中发生的主要化学反应为:
 CO2+2NH3+CaSO4+H2O→ +(NH4)2SO4,
CO2+2NH3+CaSO4+H2O→ +(NH4)2SO4,
 (1)根据质量守恒定律,,可以推测 内的物质是_________。
(1)根据质量守恒定律,,可以推测 内的物质是_________。
(2)根据实验室制取CO2不能使用硫酸的原理,判断该厂得到的副产品CaSO4固体溶于少量水中易形成_______________液。(填“悬浊液、乳浊液或溶液”)。
(3)制得(NH4)2SO4是一种常用化肥,请任意列举一种与这种物质具有相同肥效的物质是______。
(4)通过操作a将沉淀池中反应产物进行分离,其中操作a的名称是____________。
(5)煅烧炉中发生的化学反应方程式为_______ __。该反应产生可循环使用的物质是_______。
24.某同学在化学课外兴趣活动中得知:金属钾能与水发生剧烈反应,反应的化学方程式为:
2K + 2H2O=2KOH + H2↑,请分析:
(1)该反应属于___________基本反应类型。反应中_________作还原剂。
(2)反应后的溶液中加入硫酸铜溶液会出现________现象。
23.某品牌牙膏中的主要活性成分是单氟磷酸钠(Na2PO3F)。它是由_______种元素组成。单氟磷酸钠(Na2PO3F)相对分子质量是____________,单氟磷酸钠中含氧元素的质量分数为_________%。
22.根据右图信息,按要求回答:
 (1)A、B两瓶溶液溶质的化学式分别是__________;________,它们分别属于_______、________类别。(填写“酸、碱、盐、氧化物或单质”)
(1)A、B两瓶溶液溶质的化学式分别是__________;________,它们分别属于_______、________类别。(填写“酸、碱、盐、氧化物或单质”)
(2)取少量A瓶中的溶液于试管中,滴加 溶液和 溶液,若白色沉淀不消失,则A瓶中的溶液一定含有 (用符号表示)。
(3)B瓶溶液长期放置后浓度会变稀,这是因为该物质具有______性,若用量筒量取50mL密度为ρg/mL该硫酸溶液,则量筒内溶液的溶质质量为__________________克(只要求列式)。
21.用序号填空:①CH4 ② H2 ③ Na2CO3 ④ NaCl ⑤发出蓝紫色火焰 ⑥火星四射
(1)厨房中调味品之一食盐的化学式是_______(2)我国“西气东输”的气体是______。
(3)细铁丝在氧气中燃烧的现象是:______,生成一种黑色固体。
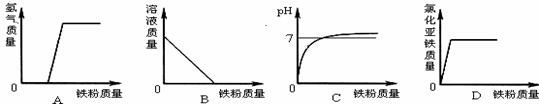
20.能正确表示在一定量的稀盐酸中加入过量的铁粉反应的图像是( )
19.甲、乙、丙三种物质在不同温度下的溶解度见下表:
|
温度 物质 |
0 |
30 |
60 |
90 |
|
甲 |
13.3 |
45.8 |
110 |
202 |
|
乙 |
35.5 |
36.0 |
37.1 |
38.1 |
|
丙 |
0.18 |
0.16 |
0.12 |
0.08 |
根据表中数据可推出的结论是( )
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.30℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙
C.降低温度可使丙的不饱和溶液变为饱和溶液
D.使甲物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法
18.现有一杯20℃的饱和硝酸钾溶液,欲改变其溶质质量分数,可采用的方法是( )
A.加入一定量的硝酸钾 B.恒温蒸发部分水 C.升温到60℃ D. 加入一定量的水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com