
19.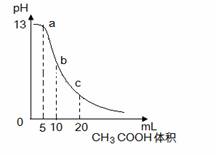 25℃时,向体积为10mL
0.1mol/L NaOH溶液中逐滴加入0.1mol/L的CH3COOH溶液,曲线如右图所示,有关离子浓度关系的比较中,错误的是
25℃时,向体积为10mL
0.1mol/L NaOH溶液中逐滴加入0.1mol/L的CH3COOH溶液,曲线如右图所示,有关离子浓度关系的比较中,错误的是
A.a点处: c(Na+)> c(CH3COO-)> c(OH-)>c(H+)
B.b点处:c(CH3COOH)+c(H+)=c(OH-)
C.c点处: c(CH3COOH)+ c(CH3COO-)=2 c(Na+)
D.NaOH溶液和CH3COOH溶液任意比混合时:
c(Na+)+c(H+)=c(OH-)+ c(CH3COO-)
18.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是

A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B.加热时,②、③溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅
D.四个“封管实验”中所发生的化学反应都是可逆反应
17.被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2十H2O = ZnO + 2MnO (OH)。下列说法正确的是
A.电池正极反应式为: 2MnO2 + 2e-+ 2H2O = 2MnO (OH)十2OH-
B.该电池的正极为锌
C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023
D.该电池反应中二氧化锰起催化作用
16.关于下列装置说法正确的是
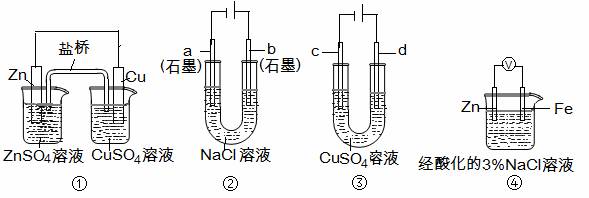
A.装置①中,盐桥中的K+移向ZnSO4溶液
B.装置②工作一段时间后,a极附近溶液的pH增大
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,装置中有Fe2+生成
15.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
 2N2O5(g)
4NO2(g)+ O2(g) △H >0
2N2O5(g)
4NO2(g)+ O2(g) △H >0
T1温度下的部分实验数据为:
|
t/s |
0 |
500 |
1000 |
1500 |
|
c(N2O5)mol/L |
5.00 |
3.52 |
2.50 |
2.50 |
下列说法不正确的是
A.500s内N2O5分解速率为2.96×10-3 mol/(L· s)
B.T1温度下的平衡常数为K1 =125,1000s时转化率为50%
C.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1 <T2
D.T1温度下的平衡常数为K1 ,T3温度下的平衡常数为K3,若K1> K3,则T1 >T3
14.下列相关实验不能达到预期目的的是
|
|
相关实验 |
预期目的 |
|
A |
相同温度下,等质量的大理石块、大理石粉分别与等体积、等浓度的盐酸反应 |
探究接触面积对化学反应速率的影响 |
|
B |
把装有颜色相同的NO2和N2O4混合气的两支试管(密封)分别浸入冷水和热水中 |
探究温度对化学平衡的影响 |
|
C |
在蔗糖中加入稀硫酸,水浴加热,再加入新制的氢氧化铜并加热 |
探究蔗糖水解产物具有还原性 |
|
D |
两支试管中装有等体积、等浓度H2O2溶液,向其中一支试管中加入MnO2固体 |
探究MnO2固体对H2O2分解速率的影响 |
13.三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3 NF3 + 5 H2O = 2 NO + HNO3 + 9 HF。下列有关该反应的说法正确的是
A. NF3是氧化剂,H2O是还原剂
B. 还原剂与氧化剂的物质的量之比为2:1
C. 若生成0.2 mol HNO3,则转移0.2 mol电子
D. NF3在潮湿的空气中泄漏会产生红棕色气体
12.短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
A. 元素非金属性:Z> Y > X B. 最高价氧化物水化物酸性:Z > Y
C. 原子半径:Z < Y < X D. 气态氢化物的稳定性:Z < Y < X
11.设NA代表阿伏加德罗常数的数值,下列说法正确的是
A.22.4 L Cl2中含有NA个C12分子
B.28 g乙烯和丙烯的混合气体中含有2NA个碳原子
C.标准状况下,2.24 L H2O含有的分子数等于0.1 NA
D.2.9 g乙基(一C2H5)含有的电子数为1.8 NA个
10.在指定的溶液中一定可以大量共存的离子组是
A.使石蕊变红的溶液中: Na+、I-、Cl-、NO3-、C6H5O-
B.在强碱性溶液中:Na+、K+、[Al(OH)4]-、CO32-、SiO32-
C.在无色透明溶液中:NH4+、Fe3+、SO32-、NO3-
D. pH=3 的溶液:Na+、Cl-、Fe2+、ClO-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com