
1. =
=
A.-1-2i B.2+i C.-1+2i D.-2+i
(一)夯实基础知识
1.牛顿第一定律(惯性定律)
一切物体总保持匀速直线运动状态或静止状态,直到有外力迫使它改变这种状态为止.
(1)理解要点
①运动是物体的一种属性,物体的运动不需要力来维持.
②它定性地揭示了运动与力的关系:力是改变物体运动状态的原因,是使物体产生加速度的原因.
③牛顿第一定律是牛顿第二定律的基础,不能认为它是牛顿第二定律合外力为零时的特例.牛顿第一定律定性地给出了力与运动的关系,第二定律定量地给出力与运动的关系.
(2)惯性:物体保持原来的匀速直线运动状态或静止状态的性质叫做惯性.
①惯性是物体的固有属性,与物体的受力情况及运动状态无关.
②质量是物体惯性大小的量度.
2.牛顿第三定律
(1)两个物体之间的作用力和反作用力总是大小相等,方向相反,作用在一条直线上,可用公式表示为F=-F′.
(2)作用力与反作用力一定是同种性质的力,作用效果不能抵消.
31、Ⅰ(8分)下图表示人体特异性免疫反应的某个阶段。请据图回答问题:
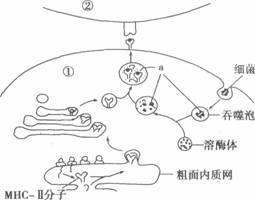
(1)图①表示 细胞,判断依据是 。
此时正处于特异性免疫的 阶段。
(2)图中a表示 ,通过MHC一Ⅱ型分子的作用,该物质暴露在细胞膜表面。
(3)由图可知,MHC一Ⅱ型分子的化学本质是 ,细胞中有 种细胞器参与MHC一Ⅱ分子的合成、加工、运输的过程,其中 没有在图中表示出来。
(4)若人体受到HIV病毒的感染, (①、②)细胞最容易受到攻击,从而导致患者几乎丧失一切免疫功能。
Ⅱ.(12分)
现有某XY型性别决定的多年生观赏植物,发现其抗除草剂对不抗除草剂为显性,由常染色体上的A 和a基因控制;花瓣单色对彩色为显性,由X染色体上的B和b基因控制;另有耐盐基因位于线粒体DNA上。
①验证花色和耐盐基因所在的位置,常用的遗传实验方法是__________________。
②现有以下纯种植株若干:
甲:不抗除草剂彩色耐盐雄株 丙:抗除草剂单色不耐盐雌株
乙:不抗除草剂彩色不耐盐雄株 丁:抗除草剂单色耐盐雌株
请利用上述四种植株(甲-丁),通过杂交育种培育抗除草剂、彩色、耐盐的雌雄植株:
第一年:可用作亲本的杂交组合是___________________________;
第二年:从子一代植株中选取表现型为__________________的植株和甲-丁中的
杂交;
第三年:从子二代植株中选出抗除草剂彩色耐盐的雌雄植株。其中选出的雄株核基因的基因型为__________________ 。
③现有水稻的纯系品种AArr(无芒易感病)和aaRR(有芒抗病),两对相对性状独立遗传。现需尽快培育出无芒抗病的品种,请用遗传图解表示从F1开始的育种程序,并作相应的文字说明。
30.Ⅰ.(10分)为了提高温室的经济效益,需要调控好温室内的光照、温度、气体和湿度。科研人员对温室栽种的作物进行了相关研究,以下是实验测得的有关数据.(甲表所示为特殊的装置内,给予不同强度的光照,测到的该植物的氧气释放量。乙图表示不同叶片的色素层析条带。丙图中曲线1、2分别表示作物的实际光合量和净光合量。)
|
光照强度 |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
O2释放量(μL/cm2叶面·min) |
-0.2 |
0 |
0.2 |
0.4 |
0.8 |
1.2 |
1.2 |
1.2 |
甲
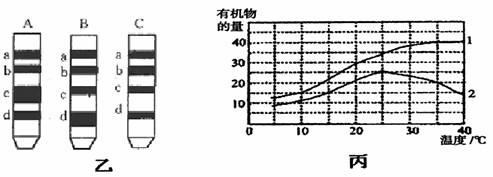
根据上述有关数据,回答下列有关问题:
(1)从甲表可知,在光照强度为4单位时,该作物光合作用的实际产氧量为
μL/cm2叶面·min。
(2)某兴趣小组同学想探究菠菜不同的叶在叶绿体色素含量上的区别,分别选择了菠菜“深绿叶”、“嫩绿叶”、 “嫩黄叶”做“绿叶中色素的提取与分离”实验。色素层析结果如乙图A、B、C三组所示,根据实验结果可知,___________组滤纸条是深绿叶的,a带所示色素的名称是_______________;b带的颜色为______________。
(3)由丙图分析:最有利于积累有机物的温度是 ;假如植物生活在12小时光照,12小时黑暗的环境中,则在环境温度达到约 时,该植物就不能正常生长。原因是 。
Ⅱ、(12分)低温和高温会伤害植物细胞,为了探究高温和低温对小麦的伤害,请完成下列实验设计方案并回答相关问题。
(1)实验原理:当植物组织受到不良条件,如高温、低温等的影响时,常能伤害细胞的结构而使膜的通透性增大,结果细胞内含物会有不同程度的外渗,使外部溶液的电导度增大,电导度的大小可以用电导仪进行检测(电导仪非常灵敏,空气中的CO2会溶解于蒸馏水中,从而给实验带来误差;各种杂质以及温度都会影响测量结果,从而带来实验误差),透性变化愈大,表示受伤愈重,抗逆性愈弱。
(2)实验材料:小麦幼苗
(3)仪器与药品:电导仪、冰水、水浴锅、烧杯、量筒、洗瓶、滤纸、蒸馏水
(4)分析变量: 自变量: 。因变量: 。
(5)实验步骤
第一步:取小麦幼苗30株,去除残留胚乳,用蒸馏水反复冲洗三次;
第二步:取四只小烧杯,分别加入20mL蒸馏水,编号为1、2、3、4号;
第三步: ____________________________________________ __。
第四步:1号小烧杯置于冰水水浴中;2号小烧杯置于室温下;3号小烧杯置于45℃的恒温水浴中;
第五步:40分钟后取出,去除小烧杯中的幼苗,并 __________
第六步: _____________________________________________
(6)回答问题:
①实验的第一步中要去除残留胚乳,并用蒸馏水冲洗的目的是
。
②空气中的CO2会溶解于蒸馏水中,从而给实验带来误差。在实验的设计中,为了校正这种因素带来的误差,本实验采用的做法是 。
29.物质之间的转化关系如下图所示,A是黄色固体,其中反应①②④⑥为常见的化工生产的反应,B、C、H、I为非金属单质。常温下D为生活中常见的无色液态化合物,X与D所含元素种类相同且X有强氧化性,可用于杀菌消毒和漂白。F为常见的红棕色防锈油漆颜料的主要成分,O是生活中常见的含氮量最高的氮肥,A、E、J、N中含有同一种元素。部分反应的部分反应物或产物没有标出。
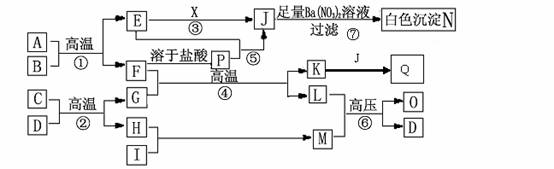
 (1)A的电子式为
,M分子的空间构型为
,O的结构式为
。
(1)A的电子式为
,M分子的空间构型为
,O的结构式为
。
(2)实验室检验Q中阳离子的一种方法
。
(3)K和D蒸汽在一定条件下能发生反应,生成2gH放出热量为akJ,该反应的热化学方程式为 。该反应生成的固体产物溶于稀硝酸的离子反应方程式为 。
(4)写出下列反应的离子反应方程式:
③ 。
Q的溶液中加入NaClO溶液 。
(5)G与O2可以组成新型燃料电池,该电池在新能源开发中有重要地位,可作未来新型汽车动力的电池,若该电池以KOH为电解质溶液,写出该燃料电池的负极反应式
。
(6)现有200T质量分数为60℅的A参加反应,若第①反应转化率为80℅,第③反应转化率为90℅,第⑦反应完全转化,则生成N的质量为 T。
高2010级高三考试理科综合试题
第Ⅱ卷(生物)
28.芳香酯类化合物A、B互为同分异构体,在一定条件下均可生成水杨酸,且均含C、H、O三种元素。相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍。
(1)A的分子式是 。
已知各有机物间存在如下转化关系:
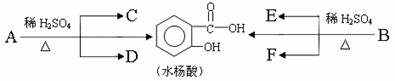
其中C能发生银镜反应,F经过连续氧化可生成C;C与D是相对分子质量相同的但不同类别的有机物。
(2)B的结构简式是__________________________。
(3)有机物C、D、E、F各mg完全燃烧,将产物全部通入Na2O2中,充分反应后Na2O2增重质量等于m g的为 ,大于m g的为 ,小于m g的为 。
(4)写出下列反应的化学反应方程式:
水杨酸与小苏打 。
C与F反应 。
A与NaOH溶液共热 。
(5)同时符合下列要求的同分异构体。即:
①与水杨酸互为同分异构体; ②可以水解;
③苯环上有两个取代基,且苯环上的一氯代物只有2种。
可能的同分异构体与新制Cu(OH)2共热的化学反应方程式为:
27.我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:
NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl;
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
Na2CO3可用于工业上制玻璃,涉及的化学反应方程式为 。
等浓度等体积的Na2CO3与NaHCO3的混合溶液中,离子浓度的大小顺序为
。
(3)某课外活动小组模拟上述制碱原理,进行碳酸氢钠的制备实验,同学们将二氧化碳气体通入含氨的饱和食盐水制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 ,该试剂的作用是 。
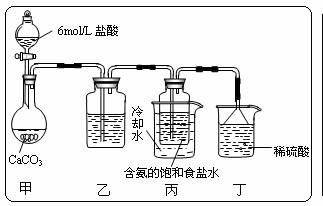 (Ⅱ)实验结束后,分离出NaHCO3 晶体的操作是
(填分离操作的名称),该操作所需要的玻璃仪器有 。
(Ⅱ)实验结束后,分离出NaHCO3 晶体的操作是
(填分离操作的名称),该操作所需要的玻璃仪器有 。
26.某校化学小组学生利用下图装置进行“氨的催化氧化及其产物验证”实验。(图中夹持装置已略去)
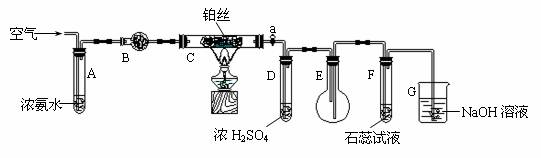
(1)装置B中盛放的试剂 (填名称),作用是 。
(2)反应开始时,将装置C中铂丝加热到红热,撤去酒精灯,铂丝变暗。此时鼓入空气,铂丝又变红热。这是因为氨的催化氧化是 反应。该反应的化学方程式为
。
(3)实验过程中,装置D中的导管容易生成无色晶体而堵塞。为了解决该问题,可以在活塞a后增加 (选填序号)。
①盛有蒸馏水的洗气瓶 ②盛有浓盐酸的洗气瓶 ③盛有碱石灰的U形管
(4)反应一段时间后,装置E中的气体颜色应为 色。此时,装置E中的含氮化合物有NO、NO2、 (填化学式)。
(5)反应一段时间后,装置F中的紫色石蕊试液变红,其原因是(写出化学方程式)
。
(6)实验结束时,应先停止加热,并继续 直至C中玻璃管冷却。
(7)工业上合成氨的反应是:N2(g) + 3H2(g) 2NH3(g);ΔH= -92.2 kJ·mol-1。
2NH3(g);ΔH= -92.2 kJ·mol-1。
①下列做法能够提高工业合成氨转化率的是 (选填字母)
a.增大压强 b.升高温度
c.使用铁触媒 d.将生成的NH3及时从混合气体中分离出去
②工业合成氨时采用500℃左右的温度,主要是因为
。
25.(20分)如图所示,MN、PQ是平行金属板,板长为L,两板间距离为d,PQ带正电,MN板带负电,在PQ板的上方有垂直纸面向里的匀强磁场。一个电荷量为q、质量为m的带负电粒子以速度v0从MN板边缘沿平行于板的方向射入两板间,结果粒子恰好从PQ板左边缘飞进磁场,然后又恰好从PQ板的右边缘飞进电场。不计粒子重力。试求:
⑴两金属板间所加电压U的大小;
⑵匀强磁场的磁感应强度B的大小;
⑶在图中正确画出粒子再次进入电场中的运动轨迹,并标出粒子再次从电场中飞出的速度方向。
高2010级高三考试理科综合试题
第Ⅱ卷(化学)
24.(19分)如图所示,A、B板并放在光滑水平面上,在A的左端有一可视为质点的物块。已知A、B与C之间的动摩擦因数μ=0.2,A、B、C质量均为m=1kg、A板长LA=1m、B板长LB=2.5m。现在C上施加一水平恒力F=5N,使C由静止开始运动,当C刚滑上B时撤去F,g=10m/s2。求:
⑴C刚滑上B时,B和C的速度;
⑵B的速度最大时A、B间的距离。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com