
1、 同位素的相对原子质量:就是某个原子质量与12C原子质量的1/12的比值。
同位素的近似相对原子质量就是相应原子的质量数。
3、 离子电荷=质子数-核外电子数
离子电荷=质子数-核外电子数
有关相对原子质量的计算
2、质量数(A)= 质子数(Z)+ 中子数(N)==近似原子量
1、核电荷数(Z) == 核内质子数 == 核外电子数 == 原子序数
3.例题讲解:
[例1]图表示的反应关系中,部分产物被略去,已知1mol白色固体粉末X完全分解后,恢复到室温,生成白色固体A,无色液体B,无色气体C各1mol,E、X、G的焰色反应均为黄色。

请回答下列问题:
(1)写出下列物质的化学式:X: E: G: D:
(2)写出G+C→X反应的化学方程式
 (3)写出X+E A的离子方程式
(3)写出X+E A的离子方程式
答案:(1)X:NaHCO3 E:NaOH;G:NaAlO2 D: Al(OH)3
(2)(3分)NaAlO2+CO2+2H2O=NaHCO3+Al(OH)3↓
(3)(3分)HCO +OH-=CO
+OH-=CO +H2O
+H2O
[例2]1 . 某单质X能从盐溶液中置换出单质Y,由此可知( )
A.当X、Y都是金属时,X一定比Y活泼
B.当X、Y都是非金属时, Y一定比X活泼
C.当X是金属时,Y可能是金属,也可能是非金属
D.当X是非金属时,Y可能是金属,也可能是非金属
[例3] A、B、C、D、E、F六种物质相互转化关系如下图所示(反应条件未标出)其中反应①是置换反应。

(1)如果A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是:
(2)若A是常见的金属单质,D、F是气体单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 ;已知1gD与F反应生成B时放出92.3KJ的热量,写出该反应的热化学反应方程式 。
(3)若B、C、F都是气态单质,且B有毒,③和④两个反应中都有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则C的电子式为 ,反应①的化学方程式是 。
(4)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,③和④两个反应中却有红棕色气体生成,则反应④的化学方程式为: 。
 答案
答案
(1)2C+SiO2 Si+2CO↑
 (2)2Fe2++Cl2 2Fe3++2Cl-
(2)2Fe2++Cl2 2Fe3++2Cl-
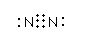
 H2(g)+Cl2 (g) 2HCl(g);△H= -184.6KJ/mol
H2(g)+Cl2 (g) 2HCl(g);△H= -184.6KJ/mol
 (3) ;3Cl2+2NH3 6HCl+N2
(3) ;3Cl2+2NH3 6HCl+N2
 (4)C+4HNO3(浓) CO2↑+4N2O↑+2H2O
(4)C+4HNO3(浓) CO2↑+4N2O↑+2H2O
[例4]甲、乙、丙、丁四种单质在点燃的条件下反应生成X、Y、Z、W四种化合物,转化关系如右图所示,又知:
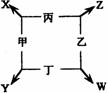 ①甲、乙、丙均为短周期元素的单质,常温下均为气态,丁是日常生
①甲、乙、丙均为短周期元素的单质,常温下均为气态,丁是日常生
活中的常见金属;
②常温下,X是无色液体,Y是黑色固体;
③丙在乙中燃烧发生苍白色火焰,丁在乙中燃烧生成棕色烟,W的
水溶液呈黄色。请填空:
(1)丁在甲和X同时存在的条件下,容易被腐蚀,写出电子反应式:
负极:__________________________ 正极:_________________________________
(2)将饱和W的溶液滴入到热的X中煮沸几分钟,反应的化学方程式为_________________________。
(3)Y与足量的稀HNO3反应的离子方程式为: ______________________________ 。
(4)在一定条件下,丁分别Y、Z反应生成等物质的量的丙时,消耗丁的物质的量之比为___________。
答案:

(4)3:4
[例5]在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:
⑴ 组成单质X和Y的元素分别属第 族和第 族;
⑵ Z与水发生水解反应方程式 ;
⑶ 每生成1mol的化合物Z,反应中转移 mol的电子。

答案:(1)(每空2分)ⅢA ⅥA
(2)(3分)Al2S3 + 6H2O === 2Al(OH)3↓+ 3H2S↑
(3)(3分)6
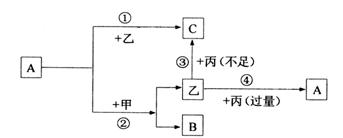 [例6]下列框图所表求援
各种物质的转化过程A、B、C、为中学化学中常见的两种组成的化合物,甲、乙、丙为单质。
[例6]下列框图所表求援
各种物质的转化过程A、B、C、为中学化学中常见的两种组成的化合物,甲、乙、丙为单质。
请回答下列问题:
(1) 上述框图所示变化过程属于化合反应的
有 ,属于置换反应的有
(2)甲、C的化学式为 ,
A与甲反应的化学方程式为
答案:(1)①③④;② (2)Mg,CO;2Mg+C02 点燃2MgO+C
[例7]A、B、C是常见单质,X、Y、Z是氧化物,它们之间有如下转化关系:
请写出符合下列要求的化学方程式:
(1)若X为CO2,则: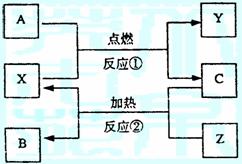
反应① 。
(2)若X为Fe3O4,则:
反应① ;
反应② 。
答案:(1)2Mg+CO2 2MgO+C
(2)①8Al+3Fe3O4 4Al2O3+9Fe
②3Fe+4H2O(g) Fe2O4+4H2
[例8]如图所示:
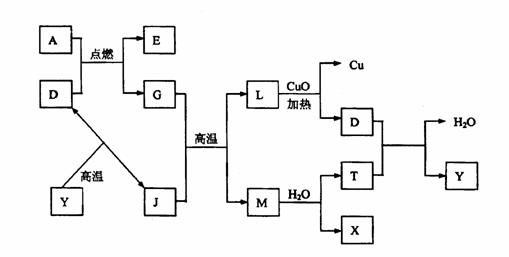
其中A、G是固体单质,其余是化合物。X是常用于切割和焊接金属的可燃性气体;Y是一种难溶于水的白色固体,它的式量是100。
请填空:
(1)D的电子式是 。
|
 。
。
答案:(1)
|
(2)2Mg+CO2=====2MgO+C, < (3) CaO+3C=====CaC2+CO↑
[例9]有 A、B、C、D四种单质,在一定条件下,A、B、C分别跟 D发生化合反应相应生成甲、乙、丙(甲、乙、丙每个分子中都含有10个电子)而B跟C发生化合反应生成丁,这些单质和化合物之间发生如下反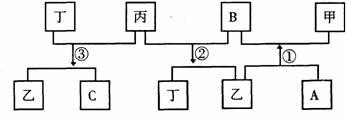 应关系:
应关系:
(1)写出下列物质的化学式
甲______________乙___________丙_____________丁_____________
(2)写出反应①②③的化学方程式
①_____________________________②______________________________③_______________________答案:(1) HF、H2O、NH3、NO (2) 2F2 + 2H2O ==4HF+ O2 4NH3+ 5O2==4NO +6H2O 4NH3+ NO==5N2 +6H2O
[例10]下图每一个方框内的字母代表一种物质,常温常压下,A、B、C、D均为主族元素形成的单质,且B为金属,其它三个为双原子分子的气体,它们在一定条件下,发生图中所示的化合反应,得到化合物E、F、G、H和J,这些化合物在常温常压下的状态及颜色已在图中注明,有关反应的化学计量数为:
①A与B按物质的量之比n(A): n(B)=1:2完全反应生成G
②B与C按物质的量之比n(B):n(C)=3:1完全反应生成F
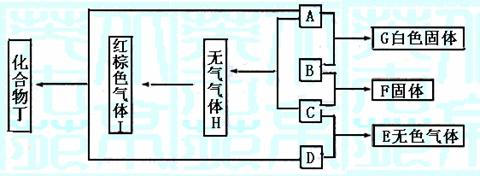
③C与D按物质的量之比n(C):n(D)=1:3完全反应生成E
请填空:
(1)物质B是 ,物质D是 。
(2)B与C反应生成F的化学方程式为: 。
(3)由H生成I的化学方程式为: 。
(4)将F溶于足量的稀盐酸中,所发生的化学反应方程式为:
(5)写出生成E的化学方程式
答案:(1)Mg(镁), H2(氢) (2)3Mg+N2 Mg3N2
(3)O2+2NO====2NO2 (4)Mg3N2+8HCl=3MgCl2+2NH4Cl
(4)Mg3N2+8HCl=3MgCl2+2NH4Cl
(5)N2+3H2 2NH3
[例11]X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见化合物。它们在一定条件下可以发生如图反应(均不是在溶液中进行的反应)(以下每个空中只需填入一种物质)
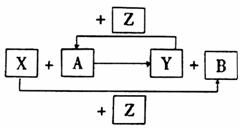
(1)当X、Y均为金属时,A为 B为
(2)当X为金属,Y为非金属时,A为 B为
(3)当X为非金属,Y为金属时,A为 B为
答案:(1)A为Fe2O3、 Fe3O4、FeO、CuO等,B为Al2O3。
(2)A为CO2,B为MgO或A为H2O(g),B为Fe3O4。
(3)A为CuO、Fe2O3等,B为H2O或CO2
[例12](08海南卷)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
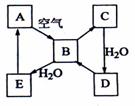 (1)写出A在加热条件下与H2反应的化学方程式
(1)写出A在加热条件下与H2反应的化学方程式
_________________________________________________________
(2)写出E与A的氢化物反应生成A的化学方程式_______________
(3)写出一个由D生成B的化学方程式___________________ ;
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式____________________________________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
③加热反应后的溶液,其pH______ (填“增大”、“不变”或“减小”),理由是___________________________。
[答案]
(1)H2+S H2S(写成可逆反应也正确)。
H2S(写成可逆反应也正确)。
(2)H2SO3 + 2H2S=3S + 3H2O。
(3)C+2H2SO4(浓) CO2 ↑+2SO2
↑+2H2O或Cu+ 2H2SO4(浓)
CO2 ↑+2SO2
↑+2H2O或Cu+ 2H2SO4(浓) CuSO4 +SO2
↑+ 2H2O等。
CuSO4 +SO2
↑+ 2H2O等。
(4)①H2SO3 +2OH- = SO32- + 2H2O。
②大于;Na2SO3溶液中SO32-发生水解使溶液显碱性。
③增大;升高温度促进Na2SO3溶液的水解。
[例13](08全国Ⅰ卷)V、W、X、Y、Z是由周期表中1-20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图:
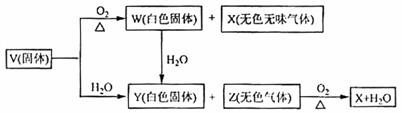
(1)5种化合物分别是V 、W 、X 、Y 、Z 。(填化学式)
 (2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 。
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 。
 (3)V的电子式是 。
(3)V的电子式是 。
[答案](1)CaC2;CaO;CO2;Ca(OH)2;C2H2。 (2)Ca(OH)2+2CO2===Ca(HCO3)2 。
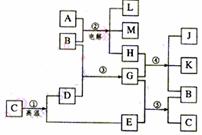
[例14]((2003年广东卷)根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是 。
(2)化合物B是 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是 和 (填代号)。
它们的化学反应方程式分别是 和 。
[答案](1)H2 (2)H2O (3)②,④
2NaCl+2H2O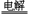 2NaOH+H2↑+Cl2↑
2Ca(OH)2+2Cl2=Ca(OCl)2+CaCl2+2H2O
2NaOH+H2↑+Cl2↑
2Ca(OH)2+2Cl2=Ca(OCl)2+CaCl2+2H2O
[例15](2005年江苏卷)右图中每一方框的字母代表一种反应物或生成物:
已知气态烃D(其密度在同温同压下是氢气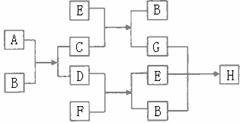 密度的13倍)跟物质F反应时产生明亮而带浓烈黑烟的火焰。请写出下列字母代表的物质的化学式(分子式):
密度的13倍)跟物质F反应时产生明亮而带浓烈黑烟的火焰。请写出下列字母代表的物质的化学式(分子式):
A 、B 、D________、E 、H__________。
[例16](2005年全国卷)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
⑴ D的化学式(分子式)是_____________,E的化学式(分子式)是_____________。
⑵ A和B反应生成C的化学方程式是______________________________。
⑶ E和F反应生成D、H和G的化学方程式是___________________________________。
1、金属单质置换其它单质
(1)金属单质之间的置换反应

 Fe+CuSO4 FeSO4+Cu
Fe+CuSO4 FeSO4+Cu
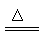 2Al+Fe2O3 2Fe+Al2O3
2Al+Fe2O3 2Fe+Al2O3
 Na+KCl NaCl+K
Na+KCl NaCl+K
 (2)金属置换氢气
(2)金属置换氢气
 Zn+H2SO4(稀) ZnSO4+H2
Zn+H2SO4(稀) ZnSO4+H2

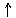

 2Na
+2H2O 2NaOH+H2
2Na
+2H2O 2NaOH+H2
 2Na+2CH3CH2OH 2CH3CH2ONa+H2
2Na+2CH3CH2OH 2CH3CH2ONa+H2

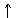
 Mg+2H2O Mg(OH)2+H2
Mg+2H2O Mg(OH)2+H2
 2Al+6H2O 2Al(OH)3+3H2
2Al+6H2O 2Al(OH)3+3H2
 (3)金属置换碳
(3)金属置换碳
2Mg+CO2 2 MgO+C
 2、非金属单质置换其它单质
2、非金属单质置换其它单质
(1)氢气置换金属
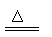 H2+CuO Cu+H2O
H2+CuO Cu+H2O
 3H2+Fe2O3 2Fe+3H2O
3H2+Fe2O3 2Fe+3H2O
(2)氢气置换非金属
2H2+SiCl4 Si+4HCl
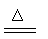 (3)碳置换金属
(3)碳置换金属
C+CuO Cu+CO(或CO2)
 (4)碳置换非金属
(4)碳置换非金属
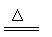
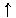 C+H2O CO+H2
C+H2O CO+H2
 2C+SiO2 Si+2CO
2C+SiO2 Si+2CO
(5)硅置换氢气
 Si+4HF SiF4 +2H2↑
Si+4HF SiF4 +2H2↑
 (6)氧气置换非金属
(6)氧气置换非金属
 O2+2H2S 2S+2H2O
O2+2H2S 2S+2H2O
3O2+4NH3 2N2+6H2O
(7)氟气置换氧气
 2F2+2H2O O2+4HF
2F2+2H2O O2+4HF
(8)氯气置换非金属

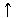 Cl2+2NaBr 2NaCl+Br2
Cl2+2NaBr 2NaCl+Br2
 Cl2+2KI 2KCl+I2
Cl2+2KI 2KCl+I2
 3Cl2+2NH3 6HCl+N2
3Cl2+2NH3 6HCl+N2
 3Cl2+8NH3 6NH4Cl+N2
3Cl2+8NH3 6NH4Cl+N2
 Cl2+H2S(Na2S) 2HCl(NaCl)+S
Cl2+H2S(Na2S) 2HCl(NaCl)+S
(9)溴置换非金属
 Br2+2KI 2KBr+I2
Br2+2KI 2KBr+I2
 Br2+H2S(Na2S) 2HBr(NaBr)+S
Br2+H2S(Na2S) 2HBr(NaBr)+S
(10)碘置换硫
 I2+H2S(Na2S) 2HI(NaI)+S
I2+H2S(Na2S) 2HI(NaI)+S
(4)复分解:
注:①通入二氧化碳气体最终能生成沉淀的物质:苯酚钠溶液、硅酸钠溶液、偏铝酸钠溶液、饱和碳酸钠溶液。
苯酚钠溶液: ;
硅酸钠溶液: ;
饱和碳酸钠溶液: ;
偏铝酸钠溶液: ;
②操作不同现象不同的反应: Na2CO3和盐酸;AlCl3和NaOH,NaAlO2和盐酸;AgNO3和氨水;FeCl3和Na2S;H3PO4和Ca(OH)2反应。
③先沉淀后澄清的反应:
AlCl3溶液中加入NaOH溶液,生成沉淀,继续滴加沉淀溶解: ;
AgNO3溶液中滴加稀氨水,先沉淀后澄清: ;
NaAlO2溶液中滴加盐酸,也是先沉淀后澄清: ;
澄清石灰水通入二氧化碳,先沉淀后澄清: ;
次氯酸钙溶液中通入二氧化碳,先沉淀后澄清: ;
KAl(SO4)2与NaOH溶液: ;
③同时生成沉淀和气体的反应:
Mg3N2+H2O-- ;
CaC2+H2O-- ;
Na2S2O3+H2SO4-- ;
Ba(OH)2+(NH4)2SO4-- ;
Al3+、Fe3+---S2-、CO32-、HCO3-间的双水解反应:
Al3++S2--- ;
Al3++HCO3--- ;
Fe3++CO32―-- ;
④制酸
2.规律总结:
(1)化合:
二合一
三合一的反应:
NH3+H2O+CO2 --
4Fe(OH)3+O2+2H2O --
4NO2+O2+2H2O --
4NO+3O2+2H2O --
CaCO3+CO2+H2O --
Na2CO3+CO2+H2O --
AlO2-+Al3++H2O --
(2)分解
①热分解反应:典型的特征是一种物质加热(1变2或1变3)。

②含有电解熔融的Al2O3来制备金属铝、电解熔融的NaCl来制备金属钠
③一种物质分解成三种物质:
2KMnO4 --
NH4HCO3 --
(NH4)2CO3 --
NaHCO3 --
Ca(HCO3)2 --
Cu2(OH)2CO3 --
HNO3--
(3)置换
1.分类:
化学用语是最重要而富有特色的化学语言,是化学试题的组成部分,是多数非选择题的设问点和赋分点。为避免由于化学用语书写不规范而造成不应有的失分,应注意三点:一要意识到化学用语是写在答题卡上呈现给阅卷教师的重要信息,书写一错(即便稿纸上的推断再正确)便不能得分,切实提高对规范书写的认识;二要熟悉各种化学用语的内涵、书写特点和要求,努力做到正确书写;三要从各次考试中发现书写错误,寻找错写原因,不断纠正,逐渐杜绝不规范书写。

[例1]1999年曾报导合成和分离了含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是(2000年全国高考题)
A.N5+共有34个核外电子 B.N5+中氮-氮原子间以共用电子对结合
C.化合物N5AsF6中As化合价为+1 D.化合物N5AsF6中F化合价为-1
[例2](2005年,天津)某粒子的结构示意图为,下列说法中不正确的是( )
A.该元素原子的原子核外有2个电子层
B.该元素是一种金属元素
C.该粒子是阳离子
D.该粒子具有稳定结构
[例3](2004·江苏)下列各项中表达正确的是( )
A.F一的结构示意图: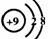 B.CO2的分子模型示意图:
B.CO2的分子模型示意图:
C.NaCl 的电子式: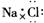 D.N2的结构式:
D.N2的结构式:
[例4]以下有些结构简式,书写得不规范、不正确。请在它们后面打一个×,并把你认为正确的写法写在后面。
1)乙醇HOCH2CH3
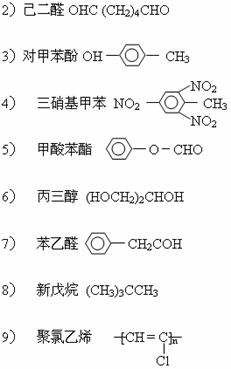
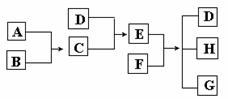
[例5]表示下列变化的化学用语正确的是( D )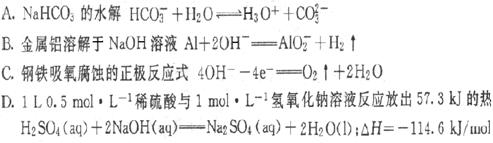
[例6]列结构图中,代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),黑点代表未用于形成共价键的最外层电子,短线代表价键。
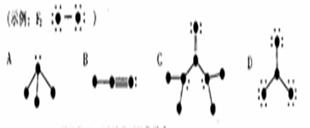
根据各图表示的结构特点,写出该分子的化学式:
A:______ B:_______ C:_______ D:_______ 答案:NH3 ;HCN ;CO(NH2)2 ;BF3
(二)有机的:天然气(又叫沼气、坑气,主要成分为CH4)
液化石油气(以丙烷、丁烷为主) 裂解气(以CH2=CH2为主) 焦炉气(H2、CH4等)
电石气(CH≡CH,常含有H2S、PH3等)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com