
4、洪特规则:电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,且自旋方向相同,这个规则是洪特规则。
洪特规则特例:当同一能级上的电子排布为全充满、半充满和全空状态时,具有较低的能量和较大的稳定性。
3、泡利不相容原理:一个原子轨道里最多只能容纳2个电子,而且自旋方向相反,这个原理成为泡利原理。
从能层、能级、原子轨道、自旋方向4个方面来说明是不可能有运动状态完全相同的两个电子的。
2、能量最低原理:原子核外电子应优先排布在能量最低的能级里,然后由里到外,依次排布在能量逐渐升高的能级里。能级的能量高低顺序如构造原理
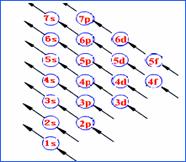
1、构造原理:多电子原子的核外电子排布总是按照能量最低原理,由低能级逐步填充到高能级。绝大数原子的核外电子的排布下图的排列顺序
构造原理中排布顺序的实质------各能级的能量高低顺序
1)相同能层的不同能级的能量高低顺序 : ns<np<nd<nf
2)英文字母相同的不同能级的能量高低顺序:1s<2s<3s<4s;2p<3p<4p; 3d<4d
3) 不同层不同能级可由下面的公式得出: ns < (n-2)f < (n-1)d < np (n为能层序数)
能级有交错现象,如E(3d)>E(4s)、E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>E(7s)、E(4f)>E(5p)、E(4f)>E(6s)等。
3、光谱:不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱(基态到激发态,亮背景,暗线)或发射光谱(激发态到基态,暗背景,亮线),总称为原子光谱。
光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
[典型例题]例5、对充有氖气的霓虹灯管通电,灯管发出红色光,产生这一现象的主要原因是( )
A、电子由激发态向基态跃迁时以光的形式释放能量 B、电子由基态向激发态跃迁时吸收除红色以外的光
C、氖原子获得电子后转化成发出红光的物质D、在电流的作用下,氖原子与构成灯管的物质发生反应
 [点击高考](07试测)下列说法中正确的是( )
[点击高考](07试测)下列说法中正确的是( )
A、处于最低能量的原子叫基态原子 B、3p2表示3p能级有两个轨道
C、同一原子中,1S、2S、3S电子的能量逐渐减小
D、同一原子中,2p、3p、4p能级的轨道数依次增多
知识点6、核外电子排布原理
2、处于最低能量的原子叫做基态原子。当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。基态原子吸收能量到激发态原子,激发态原子释放能量到基态原子。
1、能层:多电子原子的核外电子的能量是不同的,按电子的能量差异,可以将核外电子分布不同的能层。
能级:在多电子的原子中,同一能层的电子,能量也可能不同,还可以把它们分成能级。每个能层中,能级符号的顺序是ns、np、nd、nf……。任一能层的能级总是先从s 能级开始,且该能层的能级数等于该能层序数。如第一层只有一个能级(1s),第二层有两个能级(2s和2p),即能级数=能层序数。s、p、d、f…可容纳的电子数依次是1、3、5、7…的两倍
各能层所包含的能级类型及各能层、能级最多容纳的电子数见下表:
|
能
层(n) |
一 |
二 |
三 |
四 |
五 |
六 |
七 |
||||||
|
符 号 |
K |
L |
M |
N |
O |
P |
Q |
||||||
|
能
级(l) |
1s |
2s |
2p |
3s |
3p |
3d |
4s |
4p |
4d |
4f |
5s |
… |
…… |
|
最 多 电 子 数 |
2 |
2 |
6 |
2 |
6 |
10 |
2 |
6 |
10 |
14 |
2 |
… |
…… |
|
2 |
8 |
18 |
32 |
…… |
2n2 |
3、原子轨道*:90%的电子云轮廓图称为原子轨道。其中s原子轨道是球形的,p原子轨道是纺锤形的。
[典型例题]例4、下面关于多电子原子核外电子的运动规律的叙述正确的是( )
A、核外电子是沿一定轨道分层运动的 B、所有的电子在同一区域里运动
C、能量高的电子在离核近的区域运动 D、能量低的电子在离核近的区域运动
[点击高考]下列关于电子云和原子轨道的说法正确的是( )
A、原子核外的电子像云雾一样笼罩在原子核周围,故称电子云
B、s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
C、p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多
D、与s电子原子轨道相同,p电子原子轨道的平均半径随能层的增大而增大。
知识点5、能层与能级、基态与激发态、光谱
2、电子云
现代量子力学指出,核外电子的运动不能像经典力学中确定宏观物体的运动状态那样,同时用位置和速度的物理量来准确描述它的运动状态,而只能确定它在原子核外各处出现的概率。
电子在原子核外空间一定范围内出现,可以想象为一团带负电荷的云雾笼罩在原子核周围,所以,人们形象地把它叫做电子云。电子云密度大的地方,表明电子在核外空间单位体积内出现的机会多;电子云密度小的地方,表明电子在核外空间单位体积内出现的机会少。即电子云是电子在原子核外运动的概率分布图。
1、核外电子的运动特征可以概括为:
(1) 核外电子运动的能量是不连续的,分为不同的能级
(2) 核外电子运动的空间极小,运动速度极快。
(3) 核外电子运动没有确定的轨道,无法预测某时刻电子所在的位置,也不能测定电子的运动速度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com