
8.дквЛЙЬЖЈШнЛ§ЕФУмБеШнЦїжаЃЌГфШы2moI AКЭ1moI BЗЂЩњШчЯТЗДгІЃК2A(g)+B(g) XC(g)ЃЌДяЕНЦНКтКѓЃЌCЕФЬхЛ§ЗжЪ§ЮЊW%ЃЛШєЮЌГжШнЦїЬхЛ§КЭЮТЖШВЛБфЃЌвд0.6mol A ЁЂO.3mol BКЭ1.4molCЮЊЦ№ЪМЮяжЪЃЌДяЕНЦНКтКѓЃЌCЕФЬхЛ§ЗжЪ§вВЮЊW%ЃЌдђXЕФжЕЮЊ( ЁЁЁЁ)
XC(g)ЃЌДяЕНЦНКтКѓЃЌCЕФЬхЛ§ЗжЪ§ЮЊW%ЃЛШєЮЌГжШнЦїЬхЛ§КЭЮТЖШВЛБфЃЌвд0.6mol A ЁЂO.3mol BКЭ1.4molCЮЊЦ№ЪМЮяжЪЃЌДяЕНЦНКтКѓЃЌCЕФЬхЛ§ЗжЪ§вВЮЊW%ЃЌдђXЕФжЕЮЊ( ЁЁЁЁ)
ЁЁAЃЎ4ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЃЎ3ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁC. 2ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁD. l
7.НЋЬўЕФКЌбѕбмЩњЮяМгШШЗжНтЃЌШЋВПзЊЛЏЮЊЦјЬх(120Ёц ),ШєНЋЦјЬхЭЈЙ§ХЈH2SO4,ЦјЬхЬхЛ§ЫѕаЁlЃЏ3ЃЌШєНЋЪЃгрЦјЬхЭЈNaOHШмвКЃЌЪЃгрЦјЬхЬхЛ§МѕЩйlЃЏ2ЃЌдђдгаЛњЮяЕФЗжзгЪНПЩФмЪЧ( ЁЁЁЁ)
A. HCOOHЁЁ ЁЁЁЁЁЁЁЁЁЁB. H2C2O4ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.H2C2O4Љq2H2O ЁЁЁЁЁЁЁЁD. CH3COOH
6.вбжЊФГБЅКЭШмвКЕФЃКЂйШмвКЕФжЪСПЃЛЂкШмМСЕФжЪСПЃЛЂлШмвКЕФЬхЛ§ЃЛЂмШмжЪЕФФІЖћжЪСПЃЛЂнШмжЪЕФШмНтЖШЃЛЂоШмвКЕФУмЖШЃЌДгвдЩЯЬѕМўЕФзщКЯжаЃЌВЛФмгУРДМЦЫуИУБЅКЭШмвКЕФЮяжЪЕФСПХЈЖШЕФЪЧ(ЁЁЁЁ )
AЃЎЂйЂмЂоЁЁ ЁЁЁЁЁЁЁЁЁЁBЃЎЂмЂнЂоЁЁ ЁЁЁЁЁЁЁЁЁЁCЃЎЂйЂкЂлЂмЁЁ ЁЁЁЁЁЁЁЁDЃЎЂйЂкЂлЂмЂн
5.ШЫЕФбЊвКРяCa2+ХЈЖШвЛАуВЩгУgЉqcm-3БэЪОЁЃНёГщвЛбЊбљ20.00mLЃЌМгШыЪЪСПЕФВнЫсяЇ[(NH4)2C2O4]ШмвКЃЌПЩЮіГіCaC2O4ГСЕэЃЌНЋГСЕэЯДЕгКѓШмгкЧПЫсжаПЩЕУВнЫсЃЌдйгУХЈЖШЮЊO.02mol/LKMnO4ШмвКЕЮЖЈЁЃKMnO4+H2C2O4+H2SO4ЁњK2SO4+MnSO4+CO2Ёќ+H2OЕБЙлВьЕНШмвКзЯКьЩЋИеКУЯћЪЇЪБЃЌЙВЯћКФ12.0mL KMnO4ШмвКЁЃдђИУбЊвКбљЦЗCa2+ЕФХЈЖШЮЊ(ЁЁ ЁЁЁЁ)
A.0.015 gЉqcm-3ЁЁЁЁЁЁЁЁЁЁЁЁ B. 0.0012 gЉqcm-3ЁЁЁЁЁЁ ЁЁЁЁЁЁC.ЁЁ 0.0024 gЉqcm-3ЁЁЁЁ D. 0.0024 gЉqcm-3
4.Яђ2.58g KAl(SO4)2ЙЬЬхжаМгШы300 mL0.1mol/LЕФBa(OH)2ШмвКЃЌГфЗжЗДгІКѓЫљЕУГСЕэЕФжЪСПЮЊ( ЁЁЁЁЁЁ)
A. ЁЁ0.78gЁЁЁЁ ЁЁЁЁЁЁЁЁB. ЁЁ2.33g ЁЁЁЁЁЁЁЁЁЁC.ЁЁ 4.66 gЁЁЁЁ ЁЁЁЁЁЁЁЁD.ЁЁ ЁЁ5.44 g
3. вбжЊЯТСаШШЛЏбЇЗНГЬЪНЃК
вбжЊЯТСаШШЛЏбЇЗНГЬЪНЃК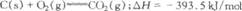
ЯжгаO.2molЕФЬПЗлКЭЧтЦјзщГЩЕФЛьКЯЮяЃЌдкбѕЦјжаЭъШЋШМЩеЃЌЙВЗХГі63.5kJШШСПЃЌдђЬПЗлгыЧтЦјЕФЮяжЪЕФСПжЎБШЮЊ(ЁЁ ЁЁЁЁ)
A. ЁЁ1:lЁЁ ЁЁЁЁЁЁЁЁЁЁB. ЁЁ1:2ЁЁ ЁЁЁЁЁЁЁЁЁЁC.ЁЁ ЁЁ2:3ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁD.ЁЁ ЁЁ3:2
2.ЯТСаЫЕЗЈжаЃЌДэЮѓЕФЪЧ(ЁЁ ЁЁЁЁ)
A. НЋФГжжЯЁЫсШмвКгУеєСѓЫЎЯЁЪЭlOБЖ,ЦфpHВЛвЛЖЈдіДѓвЛИіЕЅЮЛ
B. 100ЁцЕФNaCIШмвК,pHдМЮЊ6ЃЌЕЋШмвКГЪжаад
C. pHЯрЭЌЕФМзЫсКЭСђЫсЬхЛ§ЯрЭЌ,ЗжБ№ФмЧЁКУжаКЭЕШЮяжЪЕФСПЕФЧтбѕЛЏФЦ
D. НЋ0.lmolЃЏLМзЫсШмвКМгЫЎЯЁЪЭ10БЖЃЌШмвКжаЫљгаРызгХЈЖШОљМѕаЁ
1.Н№ЪєXЕФдзгСПЪЧН№ЪєYЕФдзгСП ЕФ2/3БЖЃЌЕШжЪСПЕФXКЭ YдкЯрЭЌЬѕМўЯТИњЙ§СПЕФЯЁСђЫсЗДгІ,ЫљВњЩњЕФЧтЦјЕФЬхЛ§ VxЪЧVyЕФвЛАыЁЃдђXЁЂYСНдЊЫиЕФЛЏКЯМлЗжБ№ЮЊ(ЁЁ ЁЁЁЁ)
A. +3ЁЂ+lЁЁ ЁЁЁЁЁЁBЃЎ+3ЁЂ+2 ЁЁЁЁЁЁЁЁC. +2ЁЂ+3ЁЁ ЁЁЁЁЁЁЁЁD. +lЁЂ+3
Р§1ЁЁ вбжЊЛЏКЯЮяAЁЂBЛЏбЇЪНЯрЫЦЃЌдкЛЏКЯЮяAжаЃЌКЌKЃКa%,SЃКb%ЃЌЦфгрЮЊбѕЃЛЛЏКЯЮяBжаКЌKЃКd%,SeЃКc%ЃЌЦфгрЮЊ,ШєSЕФЯрЖддзгжЪСПЮЊ32ЃЌдђSeЕФЯрЖддзгжЪСПЪЧ(ЁЁЁЁ ) AЃЎbd/32ac ЁЁЁЁЁЁЁЁBЃЎ32bd/ac ЁЁЁЁЁЁЁЁcЃЎ32ac/bd ЁЁЁЁЁЁЁЁDЃЎac/32bd
ЁЁ ЁЁЫМТЗЗжЮіЃКБОЬтПМВщСЫбЇЩњЖддЊЫижЪСПЗжЪ§ЕФРэНтМАжЪСПЗжЪ§ЕФМЦЫуЁЃSКЭSeдЊЫиЯрЫЦЃЌAЃЌBЛЏбЇЪНЯрЫЦЃЌЗжзгжаKдзгИіЪ§ЯрЭЌЃЌдђСНжжЮяжЪжаKЕФЯрЖддзгжЪСПзмКЭЯрЕШЁЃ
Д№АИЃКC
Р§2 (2001ФъШЋЙњ)дкБъзМзДПіЯТЃЌгУвЛЖЈСПЕФЫЎЮќЪеАБЦјКѓжЦЕУХЈЖШЮЊ12molЃЏLЃЌУмЖШЮЊ0.915 gЃЏcm3ЕФАБЫЎЃЌЪдМЦЫу1ЬхЛ§ЫЎЮќЪеЖрЩйЬхЛ§ЕФАБЦјПЩжЦЕУЩЯЪіАБЫЎ?
ЁЁЁЁ ЫМТЗЗжЮіЃКБОЬтвдЮяжЪЕФСПХЈЖШЮЊКЫаФЃЌзлКЯПМВщЦјЬхФІЖћЬхЛ§ЁЂжЪСПЁЂЬхЛ§ЕШЮяРэСПжЎМфЕФЛЛЫувдМАШмжЪШмНтЙ§ГЬжажЪСПВЛБфетвЛЙцТЩЁЃПЩДгc=n/VетвЛЛљБОЙЋЪНГіЗЂНјааЭЦЕМЃЌзЂвтВЛФмКіТдNH3ШмгкЫЎКѓШмвКЬхЛ§ЕФБфЛЏЁЃ
 Д№АИЃК378ЬхЛ§
Д№АИЃК378ЬхЛ§
Р§3(2002ФъШЋЙњ)гаШЫдјНЈвщгУAGБэЪОШмвКЕФЫсЖШЃЌAGЕФЖЈвхЮЊAG=1gЁЁЁЁ ЯТСаБэЪіе§ШЗЕФЪЧ(ЁЁЁЁ )
A.дк25ЁцЪБЃЌЦфШмвКГЪжаадЃЌдђpHЃН7ЃЌAGЃНl
B.дк25ЁцЪБЃЌЦфШмвКГЪЫсадЃЎдђPhЃМ7ЃЌAGЃМ1
C.дк25ЁцЪБЃЌЦфШмвКГЪМюадЃЎдђpHЃО7ЃЌAGЃМ1
D.дк25ЁцЪБЃЌШмвКЕФpHгыAGЕФЛЛЫуЙЋЪНЮЊAGЃН2ЁЄ(7-pH)
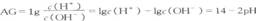 ЫМТЗЗжЮіЃКБОЬтвдpHжЕгыШмвКЕФЫсМюадЮЊвРЭа,ЭЈЙ§Ијгк AGЕФаХЯЂЃЌПМВщСЫгаЙиpHЕФЛљБОИХФюКЭЖдЯрЙижЊЪЖАбЮеЕФФмСІЁЃ
ЫМТЗЗжЮіЃКБОЬтвдpHжЕгыШмвКЕФЫсМюадЮЊвРЭа,ЭЈЙ§Ијгк AGЕФаХЯЂЃЌПМВщСЫгаЙиpHЕФЛљБОИХФюКЭЖдЯрЙижЊЪЖАбЮеЕФФмСІЁЃ
Д№АИЃКD
Р§4 (2003ФъФЯЭЈЪавЛФЃ)ЬхЛ§ЯрЭЌЃЌХЈЖШОљЮЊ0 .1 molЃЏLЕФNaOHШмвККЭАБЫЎЃЌЗжБ№МгЫЎЯЁЪЭmБЖЁЂnБЖЃЌШмвКЕФpHЖМБфГЩ9ЃЌдђmгыnЕФЙиЯЕЪЧ( ЁЁЁЁЁЁЁЁ)
AЃЎ 4mЃНnЁЁ ЁЁЁЁЁЁЁЁB.ЁЁ ЁЁmЃНnЁЁ ЁЁЁЁЁЁЁЁЁЁC.ЁЁ ЁЁmЃМnЁЁ ЁЁЁЁЁЁЁЁD.ЁЁ mЃОn
ЁЁЁЁ ЫМТЗЗжЮіЃКБОЬтПМВщСЫЧПШѕЕчНтжЪМгЫЎЯЁЪЭКѓШмвКЕФpHБфЛЏЧщПіЃЎПМВщСЫбЇЩњГщЯѓЫМЮЌФмСІКЭТпМЫМЮЌФмСІЁЃЯЁЪЭжЎЧА, NaOHКЭАБЫЎpHЪЧЗёЯрЕШ?ШчЙћЯЁЪЭЯрЭЌБЖЪ§ЃЌШмвКЕФpHЯрЕШТ№?етбљЗжЮіКѓКмШнвзЕУГіБОЬтД№АИЮЊDЁЃШєНЋЪдЬтИФГЩЬхЛ§ЯрЭЌЃЌpHОљЮЊ13ЕФNaOHКЭАБЫЎЃЌНсЙћШчКЮ?
ЁЁЁЁ Д№АИЃКD
Р§5 (2002ФъРэПЦзлКЯ)дк25ЁцЃЌ101 kPaЬѕМўЯТЃЎНЋ15LO2ЭЈШы10L COКЭH2ЕФЛьКЯЦјЬхжаЃЌЪЙЦфЭъШЋШМЩеВЂИЩдяКѓЃЌЛжИДжСдРДЕФЮТЖШКЭбЙЧПЁЃ
(1)ШєЪЃгрЦјЬхЕФЬхЛ§ЪЧ15 LЃЌдђдCOКЭH2ЕФЛьКЯЦјЬх V(CO)ЃНЁЁЁЁЁЁ LЃЌV(H2)ЃНЁЁЁЁЁЁ LЁЃ
(2)ШєЪЃгрЦјЬхЕФЬхЛ§ЮЊaL,дђдCOКЭH2ЕФЛьКЯЦјжа V(CO)ЃКV(H2)ЃНЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ШєЪЃгрЦјЬхЕФЬхЛ§ЮЊaLЃЌдђaШЁжЕЗЖЮЇЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ ЁЁЫМТЗЗжЮіЃКДЫЬтдкЩшМЦЪБгЩОпЬхЕНГщЯѓВуВуЕнНјЃЌНЯКУЕиПМВщбЇЩњЕФМЦЫуММФмКЭЫМЮЌФмСІЁЃБОЬтЪЙгУВюСПЗЈМЦЫуБШНЯЗНБуЁЃ
ЁЁЁЁ Д№АИЃК(1)5 ЁЁ5ЁЁ (2)(aЃ10):(20Ѓa)ЃЛ(3)10ЃМaЃМ20
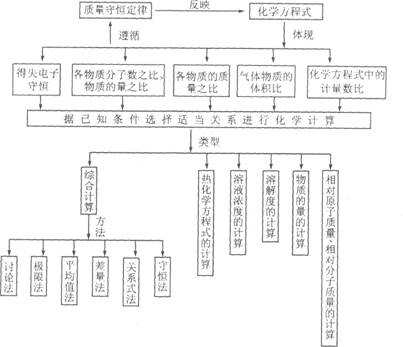
4.гаЙиЛЏбЇЗДгІЗНГЬЪНЕФМЦЫу
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com