
8.下列各组史实中,能够体现中央政府尊重少数民族文化、“因俗而治”的是 ( )
①唐朝在东突厥故地设立都督府 ②明朝在西南实施“改土归流”
③明朝在西藏建立僧官制度 ④清康熙皇帝平定“三藩之乱”
A.①③ B.②④ C.①③④ D.②③④
7.农历七月初七是中国传统的“乞巧节”(学习纺织工艺的节日)。它起源于我国古代“牛郎织女”的美丽传说。导致这一节日形成的根本原因是 ( )
A.古代人民对美好爱情的向往 B.人们对神话传说的钟爱
C.自然经济长期占据主导地位 D.人们对牛郎织女遭遇的同情
6.北宋沈括在《梦溪笔谈》中写道:“若止印三二张,未为简
易;若印数十百千本,是极为神速”。这主要得益于( )
A.造纸术的重大改进 B.雕版印刷技术的推广
C.活字印刷术的发明 D.文化市场的迅速扩大
4.美国学者伊佩霞指出:“20世纪前中国历史上任何其他时代相比(除了20世纪),初唐和中唐时的中国人自信心最强,最愿意接受不同的新鲜事物。……这个时期的中国人非常愿意向世界敞开自己,希望得到其他国家优秀的东西。”可印证该观点的史实不包括
( )
A.玄奘西游 B.鉴真东渡
C.“新罗坊”的开设 D.波斯织法与图案风格的采用
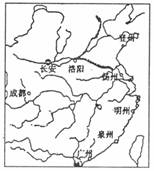 5.右图中的长安、洛阳、扬州、成都、广州、泉州、明州、登
5.右图中的长安、洛阳、扬州、成都、广州、泉州、明州、登
州被称为唐代八大城市。由此可以获取的正确历史信息有
( )
A.以工商业著称的市镇蓬勃兴起
B.扬州和成成为超越两都的政治经济中心
C.经济中心不再是政治中心
D.开放的对外政策使沿海港口城市走向兴盛
3.封建社会的污染充分体现了地主阶级的意志,下列有关我国古代法律制度的说法,不正确的是 ( )
A.秦律对后世封建律令的制订具有很大影响
B.唐朝以明确的法律条文确定了三省六部制度
C.北宋将死刑复核权力由地方收归中央
D.《大明律》采用“重其重罪,轻其轻罪”的量刑原则
2.对以下八位帝王称号归类正确的是 ( )
A.谥号:周武王、隋文帝
B.庙号:唐太宗、永乐帝
C.尊号:商纣王、秦始皇
D.年号:汉武帝、康熙帝
1.影响古希腊政治文明产生的相关因素中,最重要的客观条件是 ( )
A.古希腊的地理环境 B.东方文明的影响
C.发达的工商业经济 D.积极的殖民活动
18.(21分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
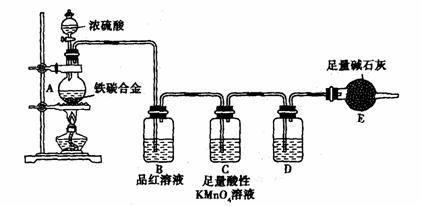
Ⅰ.探究浓硫酸的某些性质
(1) 称量E的质量;按照图示连接装置,检查装置的气密性。
(2) 将m g铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是:________________________。C中足量的酸性KMnO4溶液所起的作用
是 。D中盛放的试剂是 。
(2) 反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是___________________________________________________。
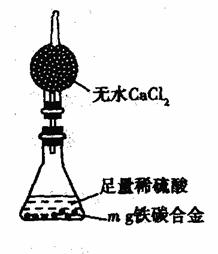 Ⅱ.测定铁的质量分数
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g,则铁碳合金中铁的质量分数为__________________________(写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是____________________________。
(5) 经过大家的讨论,决定采用下列装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是______________________(填写代号)。
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量
16.(18分)已知A、B、C、D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的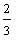 倍;A能分别与B、C、D形成电子总数相等的分子X、Y、Z。请回答下列问题:
倍;A能分别与B、C、D形成电子总数相等的分子X、Y、Z。请回答下列问题:
(1)B、D两元素的名称分别是 、 。
(2)化合物B2A2的电子式为 。
(3)Y与C的最高正价氧化物的水化物刚好完全反应时,其生成物的水溶液呈 性(填
“酸”“碱”或“中”),其原因是(用离子方程式表示) 。
(4)在(3)所得生成物的水溶液中,存在着如下关系,用粒子浓度符号填写:
① c(H+)+ =c(OH-)+ ;
② c(H+)= c(OH-)+ 。
(5)若0.2 mol液态化合物B2A8C2与液态C2D4完全反应,生成气态的C2、Z和BD2,同时放出
510 kJ热量,试写出该反应的热化学方程式:
__________________________________________________________________
(6)化合物C2A4是可燃性液体,也可用作火箭燃料。C2A4-空气燃料电池是一种碱性燃料电池,电解质溶液是20 %-30 % 的KOH溶液,放电时生成C2、Z, 则C2A4-空气燃料电池放电时,负极的电极反应式是____________ ______。
17(15分).据报道:美国海军科学家拟提取海水中溶解的二氧化碳,利用类似FT合成的方法生产短链不饱和烃,以作为汽油的替代品。研究发现,如果使用铁作催化剂,二氧化碳与氢气反应产生30%的甲烷,其余的短链烃可以被用来提炼燃料。
(1)为延缓全球温室效应,二氧化碳捕获和封存技术(CCS)是当今化学的前沿技术,下列通过化学反应捕获二氧化碳的反应,其原子利用率达100%的是 ▲ 。
(a)CO2 +CaO  CaCO3
CaCO3
(b)K2CO3+CO2+H2O=2KHCO3
(c)2Mg+CO2 2MgO+C
2MgO+C
(d)
(2)用二氧化碳合成烃,需要提供辅助原料氢气,下列制取氢气的方法可行且二氧化碳零排放的是 ▲ 。
(a)用太阳能光解海水制氢 (b)利用天然气与水高温催化制氢
(c)利用活泼金属与海水反应制氢 (d)利用核反应堆多余的电能电解海水制氢
(3)所谓FT合成,就 是CO在金属催化剂上催化氢化反应,生成以直链烷烃和烯烃为主的混合物的过程。CO2与H2合成汽油(平均组成设为C8H18)反应的化学方程式为: ▲ 。
是CO在金属催化剂上催化氢化反应,生成以直链烷烃和烯烃为主的混合物的过程。CO2与H2合成汽油(平均组成设为C8H18)反应的化学方程式为: ▲ 。
(4)某文献报道:在300℃、30MPa,以Fe、CoCl2作催化剂条件下,CO2和H2反应生成丁烷和戊烷。
①假定在一实验容器中充入一定量的CO2和H2,加入 催化剂,若CO2和H2转化率均为100%,产物只有丁烷和戊烷, n(H2)/n(CO2)=a,a取值范围为: ▲ 。
催化剂,若CO2和H2转化率均为100%,产物只有丁烷和戊烷, n(H2)/n(CO2)=a,a取值范围为: ▲ 。
②据问题①,今有标准状况下的CO2448L, n(丁烷)/n(戊烷) =x,消耗H2的物质的量为y,则y= ▲ (用x表示)。
15. (10分)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。请就“三大酸”与金属铜的反应情况,回答下列问题:
(1)在100mL 18mol/L的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B.30.24L C.20.16L D.6.72L
有同学提出,若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,请判断该方案是否可行?若不可行,请说明原因。若可行,请写出反应的离子方程式 。
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是 。则反应中所消耗的硝酸的物质的量可能为
A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)①甲同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com