
5、已知各项均为正数的数列{an}前n项和为Sn,首项为a1,且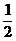 ,an,Sn成等差数列.
,an,Sn成等差数列.
(1)求数列{an}的通项公式;
(2)若an2=(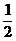 )bn,设cn=
)bn,设cn=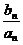 ,求数列{cn}的前n项和Tn.
,求数列{cn}的前n项和Tn.
4、若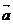 =
=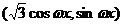 ,
,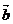 =
=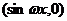 ,其中
,其中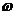 >0,记函数f(x)=(
>0,记函数f(x)=(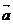 +
+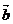 )·
)·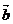 +k.
+k.
(1)若f(x)图象中相邻两条对称轴间的距离不小于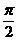 ,求
,求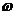 的取值范围.
的取值范围.
(2)若f(x)的最小正周期为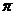 ,且当x
,且当x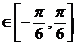 时,f(x)的最大值是
时,f(x)的最大值是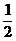 ,求f(x)的解析式,并说明如何由y=sinx的图象变换得到y=f(x)的图象.
,求f(x)的解析式,并说明如何由y=sinx的图象变换得到y=f(x)的图象.
3.已知a>0,b>0,a、b的等差中项是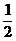 ,且α=a+
,且α=a+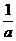 , β=b+
, β=b+ ,则α+β的最小值是__
______.
,则α+β的最小值是__
______.
2.已知O为坐标原点,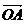 =(-3,1),
=(-3,1), =(0,5),且
=(0,5),且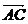 ∥
∥ ,
, ⊥
⊥ ,则点C的坐标为
.
,则点C的坐标为
.
1.等差数列{an}中,a3+3a8+a13=120,则2a9-a10的值为 .
35.(4分)同学探究镀铜的铁画中铁元素在生铁中的含量进行如下实验:取一定质量含96%生铁的镀铜铁画边角料。将该边角料磨成粉末,放入足量的稀盐酸中,待反应结束后过滤,将残渣洗涤、烘干、在空气中充分灼烧,最终得到0.3 g黑色固体,该固体比灼烧前减少了0.1 g(已知金属在灼烧过程中生成相应的氧化物)。求铁在生铁中的质量分数。
宣武区2009-2010学年度第一学期期末质量检测
34.(2分)工业上常用电解饱和氯化钠水溶液的方法制备氢氧化钠,化学方程式为
2NaCl+2H2O 2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
2NaOH+Cl2↑+H2↑。若制得16.0g氢氧化钠,可同时得到氯气的质量是多少?
33.(8分)某同学从《化学教育》杂志中得知:冶金工业可用金属单质与某种金属氧化物反应的原理来制备另一种金属单质。
[提出假设]金属都能用上述原理进行相互间制备。
[查阅资料]
(1)大多数金属氧化物都能与盐酸反应。
(2)下表列出的是一些物质溶于水后的水溶液的颜色。
|
物质名称 |
氯化铝 |
氯化铁 |
氯化铜 |
|
水溶液颜色 |
无色 |
黄色 |
蓝绿色 |
[实验过程及现象](以下各组物质均能恰好完全反应)
|
实验组别 |
I |
II |
III |
IV |
Ⅴ |
VI |
VII |
|
|
药品 |
金属单质 |
Al |
Mg |
Zn |
Fe |
Zn |
Al |
Cu |
|
氧化物 |
CuO |
CuO |
CuO |
CuO |
Fe2O3 |
Fe2O3 |
Fe2O3 |
|
|
实 验 现 象 |
取上述粉末状的混合物于密闭试管中高温 加热 |
爆炸 |
爆炸 |
变红 |
变红 |
变黑 |
变黑 |
无变化 |
|
冷却后,向上述反应后的固体中加入足量的稀盐酸 |
|
|
固体部分溶解,水溶液呈无色 |
固体部分溶解,水溶液呈黄色 |
固体全部溶解,有气体放出,水溶液呈浅绿色 |
? |
|
根据表格内容,回答下列问题:
(1)写出VI中画“?”的实验现象 。
(2)结合V中的所有实验现象,写出其中的两个反应的化学方程式
。
(3)从I-IV的实验中,可发现的规律是 。
(4)冶炼金属除需要“高温”外,还需遵循的规律是
。
32.(6分)老师用下图所示装置为同学们做了两个兴趣实验。

(1)检验装置Ⅰ气密性的方法是关闭K1和K2,向长颈漏斗中注液体至液面高出漏斗的下端管口,静置片刻,若 ,即可证明装置不漏气。
(2)若关闭K1、K3,打开K2,装置Ⅳ可以收集到一种在标准状况下密度最小的气体。装置Ⅰ中的固体物质可能是 。
(3)若打开K1、K3,关闭K2,装置Ⅰ和装置Ⅲ中可得到两种不同的气体,此时在装置Ⅱ中可以观察到的现象是 。若装置Ⅰ中得到的气体不同于(2)中的气体、装置Ⅳ中收集到的气体可使紫色的石蕊溶液变红,装置Ⅰ和装置Ⅲ中发生反应的化学方程式分别是 ; 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com