
33.(8分)某同学利用下图所示装置对植物新陈代谢中某些生理活动进行相关研究,请回答下列问题:
(1)在培养液中加入HO,一段时间后在植物体周围的空气中检测到放射性的物质有18O2、HO、C18O2,它们分别是由光合作用、__▲__、__▲__产生的。
(2)用此装置培养某植物时,第一周长势正常,第二周出现缺素症,原因是矿质元素吸收需要消耗__▲__,而此装置中根系一直浸在水中,导致__▲__。
 (3)若用此装置来探究CO2是否是光合作用的原料,则还需要增加一个实验装置,做法是__▲__,其他条件同此装置。
(3)若用此装置来探究CO2是否是光合作用的原料,则还需要增加一个实验装置,做法是__▲__,其他条件同此装置。
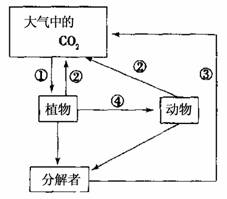 (4)若用此装置来探究元素X是否为植物的必需矿质元素,则还需再增加一个实验装置,做法是__▲__,其他条件同此装置。若研究的化学元素是镁元素和铁元素,则缺素症状表现在__▲__部位可判断为缺镁元素。
(4)若用此装置来探究元素X是否为植物的必需矿质元素,则还需再增加一个实验装置,做法是__▲__,其他条件同此装置。若研究的化学元素是镁元素和铁元素,则缺素症状表现在__▲__部位可判断为缺镁元素。
(5)若去掉此装置中的NaHCO3溶液后,同时培养长势良好的一株菠菜(C3植物)和一株苋菜(C4植物),给予充足的光照。一星期后,菠菜死亡而苋菜依旧存活,其原因可能是__▲__。
32.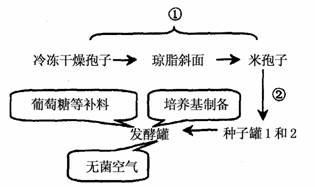 (10分)青霉素作为治疗细菌感染的药物,是20世纪医学上的重大发现,是抗生素工业的首要产品。[注:冷冻干燥孢子,在极低温度(-70℃左右),真空干燥状态下保藏的菌种。米孢子:生长在小米或大米培养基上的孢子。]
(10分)青霉素作为治疗细菌感染的药物,是20世纪医学上的重大发现,是抗生素工业的首要产品。[注:冷冻干燥孢子,在极低温度(-70℃左右),真空干燥状态下保藏的菌种。米孢子:生长在小米或大米培养基上的孢子。]
据图回答下列问题:
(1)青霉素是青霉菌的__▲__代谢产物,目前发酵生产中常用的高产青霉素菌种是通过__▲__方法选育的。据图可以判断青霉菌的代谢类型是__▲__,生殖方式为__▲__。
(2)在生产和科研中,青霉素在__▲__期积累最多,故生产中常用__▲__的方法延长此时期。
(3)培养基的配制要满足青霉菌__▲__等营养物质的需求。若在该培养基中添加蛋白胨,从化学成分上看该培养基可称为__▲__培养基。种子罐2又叫繁殖罐,可推测②属于发酵工程中的__▲__阶段。发酵罐接种__▲__(填前或后),必须进行灭菌处理。
31.(12分)根据所学的遗传学知识回答下列问题:
(1)在鸽子中,有一伴性的复等位基因系列,包括:BA(灰红色)、B(野生型呈蓝色)、b(巧克力色),它们之间显性是完全的,次序是:BA>B>b。基因型BAb的雄鸽是灰红色的,可是有时在它们的某些羽毛上出现了巧克力色斑点,请从染色体方面和基因突变方面作出两个说明:
A.__▲__
B.__▲__
(2)己知果蝇的红眼和白眼是一对相对性状(红眼W、白眼w),且雌性果蝇均有红眼和白眼类型。现有若干红眼和白眼的雌雄果蝇,若用一次交配实验即可证明这对基因位于何种染色体上,请选择交配的亲体表现型:__▲__
(3)己知某哺乳动物棒状尾(A)对正常尾(a)为显性;直毛(B)对卷毛(b)为显性;黄色毛(Y)对白色毛(y)为显性,但是雌性个体无论基因型如何,均表现为白色毛。三对基因均位于常染色体上,并遵循基因的自由组合定律。请回答:
①如果一只黄色个体与一只白色个体交配,生出一只白色雄性个体,则父本、母本、子代个体的基因型分别是:__▲__
②现有足够的直毛棒状尾雌雄个体(纯合,杂合均有),要选育出纯合卷毛棒状尾的雌性个体,请简要写出步骤:
第一步:__▲__。
第二步:__▲__,后代不出现性状分离的即为纯合卷毛棒状尾的雌性个体。
30.(14)某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为COⅠOCH2CHOHCOOⅡ(其中I、II为未知部分的结构)
为推测X的分子结构,进行如图所示的转化:
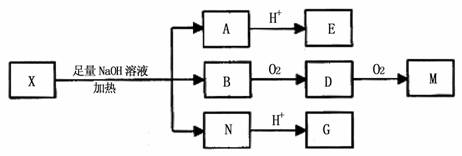
已知向E的水溶液中滴入FeCl3溶液发生显色反应;M(C2H2O4)能使蓝墨水褪色;G、M都能与NaHCO3溶液反应。
请回答:
(1)M的结构简式为 ▲ ;G分子所含官能团的名称是 ▲ ;
(2)E可以发生的反应有(选填序号)__▲__;
①加成反应 ②消去反应 ③氧化反应 ④取代反应
(3)由B转化成D的化学方程式是__▲__;
(4)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),写出G发生此反应的化学方程式__▲__;
(5)已知在X分子结构中,(I)里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是__▲__;
(6)F与G互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基。则F的分子结构有__▲__种。
29.(16分)在一定条件下(不需添加另外的反应物),经不同的化学反应,可实现如下图的各种变化。其中,反应①、②属于非氧化还原反应。正盐A分解得到三种气体。X、F和Y为单质,其余为化合物。在高科技领域中常用液态F制造低温环境。Y常用来制取漂白粉。
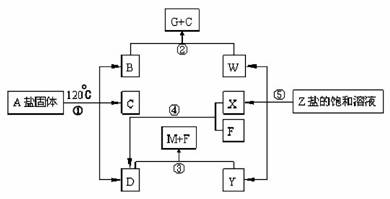
请填空:
(1)写出下列物质的化学式:A ▲ F ▲ X ▲ 。
(2)反应⑤的阴极产物为 ▲ 。
(3)写出实际工业生产中X+F→D的反应条件 ▲ 。
(4)当B过量时,写出B与W反应的离子方程式 ▲ 。
(5)当D过量时,写出D与Y的反应的化学方程式 ▲ 。
28.(15分)以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4·7H2O
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液,同时有CO2气体放出。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
Ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是__▲__。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用__▲__。
(3)Ⅲ中,生成FeCO3的离子方程式是__▲__。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是__▲__。
(4)Ⅳ中,通过检验SO来判断沉淀是否洗涤干净。检验SO的操作是__▲__。
(5)已知锻炼FeCO3的化学方程式是4FeCO3+O22Fe2O3+4CO2。现锻炼464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是__▲__kg。
27.(15分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(1)笑气是人类最早应用于医疗的麻醉剂之一,它可由NH4NO3在微热条件下分解产生,产物除N2O外还有一种,写出此反应的化学方程式:__▲__。生成1molN2O时反应中转移的电子数为__▲__mol。
(2)另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒物质--光气(COCl2):2CHCl3+O2===2HCl+2COCl2,写出光气的电子式:__▲__。为了防止发生事故,使用前要先检验氯仿是否变质,写出检验所用的试剂__▲__。
(3)氙气(54Xe)作为麻醉剂之一,在医学上也很受重视。人们曾用体积分数为80%的氙气和20%的氧气组成的混合气体作为无副作用的麻醉剂。氙在元素周期表中位置为__▲__此麻醉剂的平均式量为__▲__。
(4)氙的化学性质不活泼,但它的确可在一定条件下生成化合物。现取1mol氙气和3.5mol氟气于密闭容器中,后来余下了0.5mol氟气同时有白色固体形成,此白色固体的化学式为__▲__。
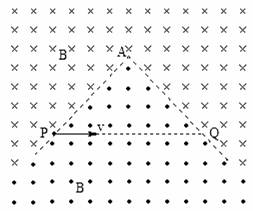
26.(21分)如图所示,空间某平面内有一条折线是磁场的分界线,在折线的两侧分布着方向相反、与平面垂直的匀强磁场,磁感应强度大小都为B。折线的顶角∠A=90°,P、Q是折线上的两点,AP=AQ=L。现有一质量为m、电荷量为q的带负电微粒从P点沿PQ方向射出,不计微粒的重力。
(1)若P、Q间外加一与磁场方向垂直的匀强电场,能使速度为v0射出的微粒沿PQ直线运动到Q点,则场强为多大?
(2)撤去电场,为使微粒从P点射出后,途经折线的顶点A而到达Q点,求初速度v应满足什么条件?
(3)求第(2)中微粒从P点到达Q点所用的时间。
25.(18分)如图,是固定在水平面上的横截面为“ ”形的光滑长直导轨槽,槽口向上,槽内放置一金属滑块,滑块上有半径为R的半圆柱形光滑凹槽,金属滑块的宽度为2R,比“
”形的光滑长直导轨槽,槽口向上,槽内放置一金属滑块,滑块上有半径为R的半圆柱形光滑凹槽,金属滑块的宽度为2R,比“ ”形槽的宽度略小。现有半径为r(r?R)的金属小球以水平初速度v0冲向滑块,从滑块上的半圆形槽口边缘进入。已知金属小球的质量为m,金属滑块的质量为3m,全过程中无机械能损失。求:
”形槽的宽度略小。现有半径为r(r?R)的金属小球以水平初速度v0冲向滑块,从滑块上的半圆形槽口边缘进入。已知金属小球的质量为m,金属滑块的质量为3m,全过程中无机械能损失。求:
(1)当金属小球滑离金属滑块时,金属小球和金属滑块的速度各是多大;
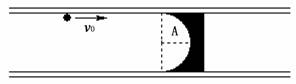 (2)当金属小球经过金属滑块上的半圆柱形槽的底部A点时,对金属滑块的作用力是多大。
(2)当金属小球经过金属滑块上的半圆柱形槽的底部A点时,对金属滑块的作用力是多大。
24.(15分)起跳摸高是学生常进行的一项活动。某中学生身高1.80m,质量70kg。他站立举臂,手指摸到的高度为2.10m。在一次摸高测试中,如果他先下蹲,再用力蹬地向上跳起,同时举臂,离地后手指摸到的高度为2.25m。设他从蹬地到离开地面所用的时间为0.7s。不计空气阻力,(取g=10m/s2)。求:
(1)他跳起刚离地时的速度大小;
(2)上跳过程中他对地面平均压力的大小。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com