
31.(22分)柴油树是一种单性花、雌雄同株的二倍体植物,其种子榨出的油稍加提炼可作为生物柴油。柴油树的产油途径如下面甲图所示(两对基因自由组合,A对a、B对b为显性)。有人设想通过基因工程培育抗病高产的柴油树,其操作过程中的一部分如下面乙图所示。请回答:
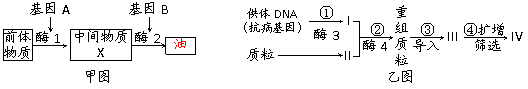
(1)从甲图所示过程可以看出,基因A、B之间及其与性状之间的关系是:____________。
(2)在乙图中,酶3的名称是______,在①-④过程中,不需要遵循碱基互补配对原则的步骤有_________。
(3)从某种细菌中获得的抗病基因导入到柴油树体细胞内后,不仅能够正常表达,而且不会影响其他基因的正常表达,其主要原因有:__________________________________。
(4)有人采用乙图所示方法得到柴油树的基因A和基因B,并成功导入大肠杆菌体内,通过发酵工程来实现高效产油,但是导入的基因却不能正常表达,最可能的原因是基因A和基因B的结构中都含有___________。要解决这一问题,可采用______________的方法获得柴油树的基因A和基因B。
(5)如果选用两种不产油的植株进行杂交,则F1代全部为产油的植株;F1自交产生的F2中,不产油的植株占_______。选用F2中某种产油的植株与另一种不产油的植株杂交,所得后代中的3种表现型及比例是,产油类型 :中间物质X含量高 :既不产油又不含中间物质X = 3 :3∶2 ,则从F2中选作亲本的植株基因型是___________和____________。
(6)现有不产油的植株甲(基因型为Aabb)和植株乙(基因型为aaBb),要在最短时间内获得能稳定遗传的产油植株的种子,请你帮助完成下列相关育种设计:
①育种原理:_________________________________________。
②育种方案设计的思路及注意事项:
根据题中所提供的实验材料,首先需要获得基因型为___________的植株。在育种过程中,需要与传统育种方法相结合进行的操作有______________。
在采用花药离体培养的方法获得单倍体植株后,要用秋水仙素溶液处理___________,才能获得染色体数目加倍的纯合植株。由于秋水仙素有剧毒,进行处理时应当注意的问题有_______________________以及减少对实验者的伤害。
整个育种过程中需要两次从所获得的_________中进行选择。
绵阳市高中2010级第二次诊断性考试
30.(20分) Ⅰ(7分)下图表示正常人体内的部分物质代谢过程,请回答:

(1)图中①过程的完成需要多种酶的参与,这是因为酶的催化作用具有__________。
(2)当人在较长时间的饥饿状态下,肝细胞中主要由________转化成物质B释放到血液中,此时起着主要调节作用的激素是_______。
(3)在肝细胞中,某些种类的物质A不能由物质B等通过______作用形成,原因是在物质B代谢的过程中不能产生相对应的______________。
(4)图中的物质C能够作用于垂体,请你简要说出理由:①____________________;②________________________。

 Ⅱ (13分)右图是研究玉米在适宜的培养条件下光合作用与呼吸作用关系的实验装置示意图。请回答:
Ⅱ (13分)右图是研究玉米在适宜的培养条件下光合作用与呼吸作用关系的实验装置示意图。请回答:
(1)该实验目的是研究光合作用____________。
(2)如果密闭装置内提供的是C18O2,那么在玉米
的________细胞中可检测到含18 O的淀粉。培养一段
时间后,下列有关18O的转移途径正确的是________。
A.C18O2→C4→C6H1218O6 B. C18O2→C3→C4→C5
C. C18O2→C3→C6H1218O6 D. C18O2→C4→C3→C5
E. C18O2→C3→C4→C6H1218O6 F. C18O2→C4→C3→C6H1218O6
(3)若要验证植物呼吸作用产生了CO2,应对上图中的实验装置进行的操作是: 。
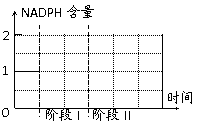 (4)如果在植物叶绿体中的NADPH与NADP+含量大致相等的情况下,依次进行下面两项实验研究:
(4)如果在植物叶绿体中的NADPH与NADP+含量大致相等的情况下,依次进行下面两项实验研究:
阶段Ⅰ 将上述实验装置放在极弱的光照下。
阶段Ⅱ 将实验装置图中的CO2缓冲液换成
浓NaOH溶液,并给予充足的光照。
请你在右面坐标图中画出叶绿体中NADPH
含量的变化曲线。
29.(13分)水处理技术在工业生产和日常生活中有着重要应用。
(1)水处理絮凝剂包括无机絮凝剂和有机絮凝剂。无机絮凝剂如明矾,其原理用离子方程式表示为 ;有机絮凝剂如聚丙烯酸钠,其结构简式为 。
(2)用氯气进行自来水消毒时,起消毒杀菌作用的物质是 ,但用氯气消毒的水可能有臭味,长期饮用还可能对人造成潜在危害。ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,工业上可用SO2与NaClO3溶液反应制得,该反应中氧化剂与还原剂的物质的量之比是___________。
(3)高铁酸钠(Na2FeO4)作为水处理剂兼具絮凝剂和消毒杀菌剂的作用,被科学家们公认为绿色消毒剂。
① 实验室采用次氯酸盐氧化法制高铁酸钠,在10.0 mL质量分数为8 % 的次氯酸钠溶液(密度为1.05 g·cm-3)中加入4.0 g氢氧化钠和0.70 g硫酸铁,可制备高铁酸钠的稀溶液,该反应的离子方程式是 ,所得溶液中含高铁酸钠最多只能达到________ mol。
 ② 高铁酸盐还可用于可充电电池。高铁电池与普通高能电池相比,能长时间保持稳定的放电电压。高铁电池的总反应为:
② 高铁酸盐还可用于可充电电池。高铁电池与普通高能电池相比,能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
该电池充电时,阳极的电极反应是 ;放电时,每有1 mol K2FeO4被还原,转移电子的数目为 。
28.(17分)芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1 mol H2,若1 mol C与NaHCO3完全反应,也产生1 mol气体,E可以使溴的四氯化碳溶液褪色。

(1)D分子中的含氧官能团名称是 ,A的结构简式是 。
(2)反应④的基本类型是 反应,反应⑤的化学方程式是 。
(3)与C取代基位置相同,既能与FeCl3溶液显色、又能发生水解反应的同分异构体结构简式为: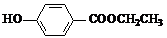 、
、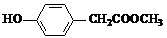 、
。
、
。
(4)现有C和E的混合物n mol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2 a L(标准状况)、H2O b g,则C、E混合物中含E的物质的量的计算式为:
。
27.(14分)如下图所示的转化关系中(部分产物省略),A是由四种短周期元素组成的正盐,X是黄绿色气体,D、F都是无色有刺激性气味的气体;气体I对H2的相对密度是13,且分子中各原子处于同一直线上;D、E分子都是10电子微粒。

请回答下列问题:
(1)J的化学式为 ,Y的电子式为 。
(2)反应③的离子方程式是 ,反应⑤的化学方程式是 。
(3)上述转化中,属于氧化还原反应的是(填编号) 。
(4)在450 ℃、催化剂存在下,4 mol F和2 mol O2反应放热353.9 kJ,此时,F的转化率为90 %,则该反应的热化学方程式为 。
26.(16分)已知,室温下存在反应3HNO2===HNO3+2NO↑+H2O;在酸性溶液中,NO-2 可将 MnO-4 还原为Mn2+且无气体生成。某化学兴趣小组设计了如下探究实验:
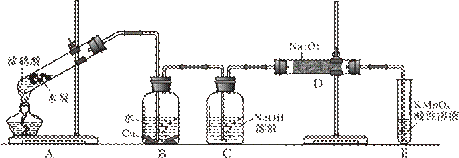
请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是 。
(2)B瓶中可以观察到的现象是 ,C瓶出来的气体是 。
(3)实验时观察到D 管内固体颜色逐渐变为白色。据此甲同学认为D管中生成物是NaNO3,而乙同学则认为D管中生成的是NaNO2,如何证明乙同学的观点正确?
|
实验方法 |
实验现象 |
反应的离子方程式 |
|
|
|
|
(4)E装置的作用是 。
(5)同学们经讨论认为上述装置仍有缺陷,为了避免D管中生成NaOH,你认为应该进行的改进是 。
25. (22分)如图所示的竖直平面内有范围足够大、水平向左的匀强电场,电场强度为E。一绝缘弯杆由两段直杆和一半径R=1.6m的四分之一圆弧杆MN组成,固定在竖直面内,两直杆与圆弧杆的连接点分别是M、N,竖直杆PM和水平杆NQ均足够长,PMN段光滑。现有一质量为m1=0.2 kg、带电荷量为+q的小环1套在PM杆上,从M点的上方的D点静止释放,恰好能达到N点。已知q=2×10-2C,E=2×102N
/ m。g取10 m / s2。
(22分)如图所示的竖直平面内有范围足够大、水平向左的匀强电场,电场强度为E。一绝缘弯杆由两段直杆和一半径R=1.6m的四分之一圆弧杆MN组成,固定在竖直面内,两直杆与圆弧杆的连接点分别是M、N,竖直杆PM和水平杆NQ均足够长,PMN段光滑。现有一质量为m1=0.2 kg、带电荷量为+q的小环1套在PM杆上,从M点的上方的D点静止释放,恰好能达到N点。已知q=2×10-2C,E=2×102N
/ m。g取10 m / s2。
(1) 求D、M间的距离h1=?
(2) 求小环1第一次通过圆弧杆上的M点时,圆弧杆对小环作用力F的大小?
(3) 在水平杆NQ上的N点套一个质量为m2=0.6 kg、不带电的小环2,小环1和2与NQ间的动摩擦因数μ=0.1。现将小环1移至距离M点上方h2=14.4 m处由静止释放,两环碰撞后,小环2在NQ上通过的最大距离是s2=8 m。两环间无电荷转移。环与杆之间的最大静摩擦力等于滑动摩擦力。问经过足够长的时间,小环1的状态?小环1在水平杆NQ上运动通过的总路程s1=?
24.(19分)如图甲所示,在一对平行光滑的金属导轨的上端连接一阻值为R=4Ω的定值电阻,两导轨在同一平面内。质量为m=0.1kg,长为L=0.1m的导体棒ab垂直于导轨,使其从靠近电阻处由静止开始下滑,已知导体棒电阻为r=1Ω,整个装置处于垂直于导轨平面的匀强磁场中,导体棒下滑过程中加速度a与速度v的关系如图乙所示。g=10 m / s2。求:
 (1)导轨平面与水平面间夹角θ;
(1)导轨平面与水平面间夹角θ;
(2)磁场的磁感应强度B;
(3)若靠近电阻处到底端距离s=20m,ab棒在下滑至底端前速度已达10m/s,求ab棒下滑整个过程中,电阻R上产生的焦耳热。
23. (14分)如图所示,在xOy坐标系y轴右侧有垂直于纸面向里的匀强磁场,磁感应强度为B,在第四象限还有沿x轴负方向的匀强电场,y轴上有一点P,坐标已知为(0,L),一电荷量为q、质量为m的粒子从P点以某一大小未知的速度沿与y轴正方向夹角为30°的方向垂直射入磁场,已知粒子能够进入第四象限,并且在其中恰好做匀速直线运动。不计重力。求:
(14分)如图所示,在xOy坐标系y轴右侧有垂直于纸面向里的匀强磁场,磁感应强度为B,在第四象限还有沿x轴负方向的匀强电场,y轴上有一点P,坐标已知为(0,L),一电荷量为q、质量为m的粒子从P点以某一大小未知的速度沿与y轴正方向夹角为30°的方向垂直射入磁场,已知粒子能够进入第四象限,并且在其中恰好做匀速直线运动。不计重力。求:
(1)粒子在第一象限中运动的时间t;
(2)电场强度E。
22.(1)(5分)在“验证机械能守恒定律”的实验中(g取9.8 m / s2):
① 所需器材有打点计时器(带导线)、纸带、复写纸、带铁夹的铁架台和带夹子的重物,此外还需 (填字母代号)中的器材。
A.直流电源 B. 交流电源 C. 游标卡尺 D.毫米刻度尺 E.天平及砝码 F.秒表
② 正确使用打点计时器,打出的某一条纸带如图,O是纸带静止时打的点,1、2、3、4、5、6是依次打的6个点,已知电源频率是50Hz。利用图中给出的数据可求出打第4点时的速度v4=_______ m/s。
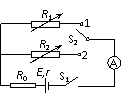

(2)(12分)用如图所示的电路测量电源的电动势E和内电阻r。
提供的器材有:保护电阻R0(准确阻值是50Ω)、电阻箱R1(0-100Ω)、电阻箱R2(0-200Ω)、电源(电动势约6V,内阻约1Ω)、单刀单掷开关S1和单刀双掷开关S2、导线若干。
供选择的器材有:电流表A1(量程6mA)、电流表A2(量程60mA)、电流表A3(量程0.6A)。①电流表应该选_________。
②实验操作步骤是:闭合开关S1,电阻箱R1选取合适的阻值,______________,读取并记录__________________;电阻箱R2选取合适的阻值,保持开关S1闭合,______________,读取并记录__________________。(明确写出读取并记录的物理量的名称和符号)
③电动势表达式E= ,内电阻表达式r = 。(用已知和②中读取并记录的物理量的符号表示)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com