
4、 强科更强,弱科不弱;强科有弱项,弱科有强项。在考试的几个科目上,一个人有强有弱,是太正常了。复习的策略,就是扬强扶弱。有的同学是只补弱的,忽视了强的;有的同学是放弃弱的专攻强的。从整体看,都未见明智。强的里面不要有“水分”,弱的里面还要有突破。
3、 勇气、心态。考试要有一个良好的心态,要有勇气。“试试争争”是一种积极的参与心态,是敢于拼搏,敢于胜利的精神状态,是一种挑战的气势。无论是复习还是在考场上,都需要情绪饱满和精神张扬,而不是情绪不振和精神萎靡,需要兴奋而不是沉闷,需要勇敢而不是怯懦。
2、 学历史,要“死”去“活”来。历史学科,有很多需要背诵的东西,人物、事件、年代、一些历史史料的要点等等。有些材料,只能“死”记。要靠多次反复强化记忆。历史课是一门机械死记量比较大的学科。但是在考试时,却要把记住的材料灵活运用,这就不仅要记得牢,记得死,还要理解,理解得活。是谓:“死”去“活”来。不单学历史,学地理,学政治,以至学理化生物,都需要“死”去“活”来。
1、 基础。什么是根本?就是基础。基础知识和基本技能技巧,是教学大纲也是考试的主要要求。在“双基”的基础上,再去把握基本的解题思路。解题思路是建立在扎实的基础知识条件上的一种分析问题解决问题的着眼点和入手点。再难的题目也无非是基础东西的综合或变式。在有限的复习时间内我们要做出明智的选择,那就是要抓基础。要记住:基础,还是基础。
31.(22分)
Ⅰ.一只雌鼠的染色体上的某基因发生突变,使得野生型性状变为突变型,请回答下列问题:
⑴假定控制突变型的基因是位于常染色体上的隐性基因,则用纯合野生型雄鼠与上述雌鼠交配,后代表现型是 。
⑵另假定上述雌鼠为杂合子,让其与野生型雄鼠交配, 代表现型有四种,分别是突变型♀、野生型♀、突变型♂、野生型♂、比例为1:1:1:1。从
代表现型有四种,分别是突变型♀、野生型♀、突变型♂、野生型♂、比例为1:1:1:1。从 代中选用野生型♀、突变型♂的个体进行交配,其下一代的表现型中所有♂的都为野生型,所有的♀都为突变型。请问:突变基因位于X染色体上还是常染色体上?说明推断理由并画出遗传图解(B表示显性基因,b表示隐性基因)。
代中选用野生型♀、突变型♂的个体进行交配,其下一代的表现型中所有♂的都为野生型,所有的♀都为突变型。请问:突变基因位于X染色体上还是常染色体上?说明推断理由并画出遗传图解(B表示显性基因,b表示隐性基因)。
推断结论:
推断理由:
遗传图解:
Ⅱ.(14分)干扰素是能够抑制多种病毒复制的抗病毒物质。科学家利用基因工程技术从人的T淋巴细胞中提取干扰素基因转入羊的DNA中,培育出羊乳腺生物发生器,使羊乳汁中含有人体干扰素。请回答:
(1)科学家将人的干扰素基因与乳腺蛋白基因的启动子等调控组件重组在一起,通过显微注射等方法,导入哺乳动物的___________细胞中,然后,将该细胞送入母体内,使其生长发育成为___________动物。
(2)在该工程中所用的基因“剪刀”是 。将人体干扰素基因“插入”并连接到羊体细胞DNA上所需要的酶是 。人体干扰素基因之所以能“插入”到羊的DNA内,原因是 。
(3)请在下框中画出某DNA片段被切割形成黏性末端的过程示意图。

(4)如何检测和鉴定人的干扰素因素已被成功导入羊体内?请写出两种方法:
、 。
(5)为了使T淋巴细胞在体外产生大量的干扰素,有人进行了实验,可是当将T淋巴细胞在体外培养繁殖了几代后,细胞分裂就停止了。请你用细胞工程的方法,以小鼠为实验对象,提出一个既能使T淋巴细胞在体外培养繁殖,又能获得大量小鼠干扰素的实验设计简单思路:
。
30.(20分)下丘脑和垂体在人体内分泌活动中起重要的调节作用。请回答下列问题:
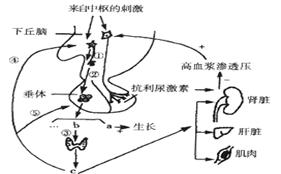
(1)图中下丘脑参与的生理调节方式有________________________。当人体突然进入寒冷环境中,下丘脑分泌的_________________________量增加,与其它激素协同作用,导致产热增加。
(2)在①-⑤过程中,属于反馈抑制作用的是____________________。
(3)下丘脑参与上述活动的神经中枢是_____________________________。
(4)甲状腺激素能提高神经系统的兴奋性,某同学由“高温能影响酶的活性”联想到“高温是否也影响甲状腺激素的活性”。该同学以小白鼠为实验对象进行探究,请你帮助完成下列问题:
实验材料和用具:正常的实验小白鼠2组、注射器、烧杯、量筒、水浴锅、试管等。
实验步骤:
①将正常的小白鼠分成A、B两组,观察并记录其生理状况。
②将这两组小白鼠的甲状腺切除,小白鼠出现精神萎靡、食欲不振等现象。
③____________________________________________________________________________。
④_____________________________________________________________________________。
一段时间后,观察并记录其生理状况。
实验结果的预测和结论:
①______________________________________________________________________________;
②____________________________________________________________________________;
③______________________________________________________________________________。
29.(16分)部分有机物之间的转化关系以及转化过程中相对分子质量的变化关系如下:
物质转化关系:RCH2OH → RCHO → RCOOH
相对分子质量: M M -2 M +14
已知:物质A中只含有C、H、O三种元素,一定条件下能发生银镜反应,物质C的相对分子质量104。A与其他物质之间的转化关系如下图所示:
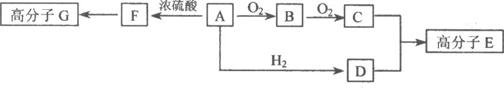 请回答下列问题:
请回答下列问题:
(1)A的结构简式为_____________________,高分子G的结构简式为_________________。
(2)F中含有的官能团有______________________。
(3)一定条件下,B与足量银氨溶液发生反应的化学方程式为:
________________________________________________________________________。
(4)由C、D在一定条件下反应还能生成环状化合物,其化学方程式为:
________________________________________________________,反应类型为__________。
(5)A的同分异构体很多,写出与A中所含官能团不同,但能与NaOH溶液反应的各种异构体的结构简式__________________________________________________________。
28.(14分)固体X是由两种常见元素组成的化合物,其中有一种为金属元素,金属元素在化合物X中的质量分数为14/15。在一定条件下X可发生如下框图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为混合气体,R是能使澄清石灰水变浑浊的无色无味气体,C为红褐色沉淀,M为常见金属单质,Q为常见非金属单质。
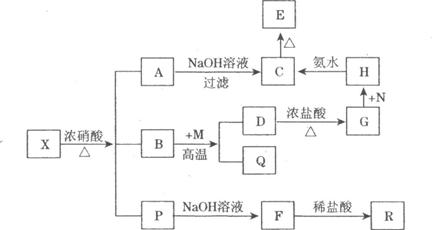
请根据以上信息,完成下列各小题:
(1)X的化学式为___________,在X与浓硝酸共热条件下反应所得的产物中,属于氧化产物的有________________________。
(2)R气体的结构式为________________。
(3)实现G→H,欲不引进新的杂质,N可以选择下列物质中的__________(填字母代号)。
a.H2O2 b.KMnO4 c.Cl2 d.HNO3 e.NaClO
(4)写出下列反应的离子方程式:
H→C______________________________________________________________;
D→G______________________________________________________________。
27.(15分) 向溴水中加入足量乙醛溶液,可以看到溴水褪色。
有如下三种猜想:①由于乙醛具有还原性,溴水将乙醛氧化成了乙酸;
②溴水与乙醛发生取代反应;
③由于乙醛分子中有双键,溴水与乙醛发生了加成反应。
为探究哪一种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性。
方案二:测定反应前溴水中Br2的物质的量和反应后Br-的物质的量。
(1)用pH试纸检验溶液酸碱性的方法是____________________________________________
_____________________。方案一是否可行?________(填“可行”或“不可行”)。理由是______
______________________________________。
(2)假设测得反应前溴水中Br2的物质的量为a mol,若测得反应后n(Br-)=______mol,则说明溴水与乙醛发生了取代反应;若测得反应后n(Br-)=_______mol,则说明溴水与乙醛发生了加成反应;若测得反应后n(Br-)=______mol,则说明溴水将乙醛氧化为乙酸。
(3)一般用KBrO3、KBr溶液在酸性条件下制取Br2,其离子方程式为____________________。为了不影响后面的实验,若取物质的量浓度为0.1 mol/L的KBrO3溶液100 mL,则需加入同浓度的KBr溶液_________ mL,将上述溶液稀释定容到1 L,取此溶液20 mL,加入足量的乙醛使其褪色后,将所得溶液稀释到100 mL,准确量取10 mL,加入过量AgNO3溶液,过滤、洗涤、干燥后称量得到AgBr固体22.56 mg,则溴水与乙醛反应的离子方程式为:
____________________________________________________。
26.(15分)Ⅰ.有原子序数依次增大的四种短周期元素A、B、C、D,已知:
①A与C、B与D分别同主族;
②A、C、D分别与B都能形成两种常见的化合物;
③B的阴离子与C的阳离子的核外电子排布相同。
试根据以上信息完成下列各小题:
(1)写出由C与B形成的化合物C2B2的电子式______________________,其中含有的化学键类型有___________________________。
(2)A与B形成的两种常见化合物属于___________(填“极性”、“非极性”)分子。
(3)写出由A、C、D三种元素组成的盐溶于水所得溶液呈碱性,其原因是(用离子方程式表示)_________________________________________________。
(4)写出均由这四种元素组成的两种化合物在水溶液中发生反应的离子方程式:
______________________________________________________。
(5)A、B两种元素的单质已被应用于宇宙飞船的燃料电池中。在燃料电池中通入A元素的单质的电极为电池的_________(填“正”或“负”)极,若以KOH溶液为介质环境,则此电极上发生的电极反应式为________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com