
26.(14)分
现有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A和D、C和E分别同主族,D、E、F同周期。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C可形成电子总数相等的分子,且A与C、A与E、A与F也可以形成电子总数相等的分子。
请回答下列问题:
(1)元素F在周期表中的位置:________________________
(2)A、C、D三种元素可组成一种常见的化合物,该化合物的化学式____________;工业生产该化合物和单质F的离子方程式:_________________________________
(3)B与F形成的化合物分子中,各原子最外层均达到8电子结构,则该分子的电子式:______________________________
(4)已知0.5mol EC2被C2氧化成为EC3,放出49.15kJ的热量,其热化学方程式为:________________________________________________________________
(5)A、B、C以原子个数比为4:2:3所形成的化合物,所含化学键类型为:______________
13.常温下将稀NaOH溶液和稀CH3COOH溶液混合,不可能出现的结果是 ( )
A.pH>7,且c(Na+)>c(OH-)>c(H+)>c(CHCOO-)
B.pH>7,且c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
C.pH<7,且c(CHCOO-)>c(H+)>c(Na+)>c(OH-)
D.pH=7,且c(CHCOO-)=c(Na+)>c(H+)=c(OH-)
第26-28为必考题,每个试题考生都必须作答。第37-39为选做题,考生根据要求作答
12.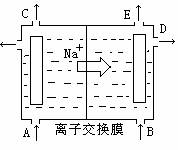 右图为阳离子交换膜法电解饱和食盐水原理
右图为阳离子交换膜法电解饱和食盐水原理
示意图。下列说法不正确的是 ( )
A.从E口逸出的气体是H2
B.从B口加入含有少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4LCl2,同时产生2mol NaOH
D.粗盐水中含有Ca2+ Mg2+ Fe3+ SO42-等离子,精
制时先加入Na2CO3溶液
11.从下列事实所得出的相应结论不正确的是( )
|
|
实验事实 |
结论 |
|
A |
将燃烧的Mg条放入CO2中能继续燃烧 |
还原性:Mg>C |
|
B |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
酸性:HCO3->Al(OH)3 |
|
C |
常温下白磷可自燃而氮气必须在放电时才与氧气反应 |
非金属性:P>N |
|
D |
向某未知溶液中加入稀硝酸和KSCN溶液,溶液变红 |
原未知溶液中不一定有Fe3+ |
10.将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果。用数轴表示下列化学知识正确的是(提示:AlO2-在水溶液中可以表示为(Al(OH)4)-)表示( )
A.分散系分类 :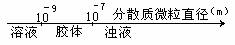
B.平衡常数与转化率关系 :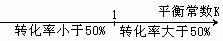
C.AlCl3与NaOH反应后铝元素的存在形式:
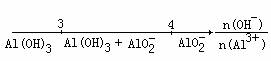
D.Na与O2反应的产物:
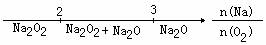
9.有关能量的判断或表示方法正确的是 ( )
A.由:H++OH-=H2O;△H=-57.3kJ/mol,可知:含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出热量大于57.3kJ
B.从C(石墨)=C(金刚石);△H=+119kJ/mol,可知:金刚石比石墨稳定
C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
D.2g H2 完全燃烧生成液态水放出285.8kJ 热量,则氢气燃烧的热化学方程式为:
2 H2(g)+O2(g) =2 H2O(l);△H=-285.8kJ/mol
8.下列说法正确的是( )
A.凡是放热反应都是自发的,由于吸热反应都是非自发的
B.自发反应一定是熵增大,非自发反应一定是熵减少或不变
C.自发反应在恰当的条件下才能实现
D.自发反应在任何条件下都能实现
7.下列表述与化学用语正确的是( )
A.CO2的比例模型  B.氢化氨的电子式:
B.氢化氨的电子式: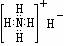
C.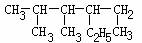 的名称:2,3-二甲基-4-乙基己烷
的名称:2,3-二甲基-4-乙基己烷
D.乙酸乙酯水解:
提示:可以从手法,人物,细节等多方面来讨论。
7.若将结尾处的“写下”改成“高呼”,可以吗?为什么?
不可以,因为这时的韩麦尔先生陷入了极大的痛苦之中,连说话的力气都没有了。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com