
1ЁЂЮЪЬтОпгажїЙладЁЃЮЪЬтЕФЩшжУЮЊПМЩњЬсЙЉСЫЬНЫїЁЂЫМПМЁЂЗЂБэЖРСЂМћНтЕФПеМфЃЌгажњгкПМЩњДДдьСІЕФЗЂЛгЃЌгажњгкеЙЪОПМЩњЕФДДаТМћНтКЭгяЮФФмСІЁЃ
Шч2007ФъИпПМЩНЖЋОэЕк22Ьт(ЮФбЇРр)ЃК
зїепЫЕШЫдкЙТОјЕФЛЗОГжаЃЌЭљЭљШнвзВЩШЁаяОЦЁЂЦђжњКЭбАЧѓСЏУѕЕШЗНЪНРДНтЭбздМКЁЃФудѕбљПДД§етжжШЫЩњЬЌЖШ?МйШєФуДІдкетбљЕФЛЗОГгжЛсШчКЮЃПЧыСЊЯЕШЋЮФЬИЬИФуЕФПДЗЈЁЃ
етРяУПИіЮЪЬтЖМЧПЕїЁАФуЁБЕФПДЗЈЃЌОЭвЊЧѓПМЩњНсКЯЮФеТЕФФкШнЁЂздМКЕФЩњЛюЛ§РлЁЂШЫЩњЙлЕШзїГіздМКЕФЫМПМгыНтД№ЁЃ
ЬНОПЃЌжИЬНЬжвЩЕуФбЕуЃЌгаЫљЗЂЯжКЭДДаТЃЌЪЧдкЪЖМЧЁЂРэНтЁЂЗжЮізлКЯЕФЛљДЁЩЯЗЂеЙСЫЕФФмСІВуМЖЁЃЬНОПМШВЛЪЧЖдаХЯЂЕФЩИбЁећКЯЃЌвВжївЊВЛЪЧЖдвеЪѕадЕФЦРЫЕМјЩЭЃЌЖјЪЧЖдзїЦЗЫМЯыФкШнЕФЗЂОђЁЂЬНЬжЁЂЬигаНтЖСКЭжЪвЩЃЌЬхЯжСЫвЛжжЫМЮЌЩЯЕФЩюЖШКЭЙуЖШЁЃ
ЬНОПЬтЃЌМђЕЅЕиЫЕОЭЪЧжИПЊЗХадЪдЬтжаДјгаЖдВФСЯЕФбаОПЁЂЬНЬжЁЂЗжЮіЁЂећКЯЃЌНјЖјЬсГіжЪвЩЁЂСэНтЁЂНЈвщЛђМјЩЭЦРМлЕФЬтФПЁЃ
7. 2007Фъ10дТЪЧЫїЖћЮЌжЦМюЗЈУќУћ140жмФъМЭФюЃЌ1867ФъдкАЭРшЪРНчВЉРРЛсЩЯЃЌНЋАБМюЗЈе§ЪНУќУћЮЊЫїЖћЮЌжЦМюЗЈЁЃИУЗЈЙуЗКЮЊЪРНчИїЙњВЩгУЃЌКѓБЛжаЙњЕФКюЪЯжЦМюЗЈЫљШЁДњЁЃЫїЖћЮЌЗЈЕФЩњВњСїГЬЪЧЃК
 ЁЁ
ЁЁ
ЫїЖћЮЌЗЈФмЪЕЯжСЌајЩњВњЃЌЕЋЪГбЮРћгУТЪжЛга70ЉЃЌЧвИБВњЦЗCaCl2УЛгагУЭОЃЌЮлШОЛЗОГЁЃ
1940ФъЮвЙњЛЏбЇМвКюЕТАёЯШЩњОЙ§ЖрДЮЪЕбщЃЌГхЦЦСЫЁАЫїЖћЮЌЗЈЁБЕФММЪѕЗтЫјЃЌВЂМгвдИФНјЃЌЪГбЮРћгУТЪДя96ЉЃЌЕУЕНСЫДПМюКЭТШЛЏяЇСНжжВњЦЗЃЌБЛГЦЮЊЁАКюЪЯжЦМюЗЈЁБЁЃЦфЛљБОдРэЪЧЃК
Ђйдк30Ёц-50ЁцЕФБЅКЭЪГбЮЫЎжаЃЌЯШЭЈШыАББЅКЭЃЌдйЭЈШыCO2ЕУЬМЫсЧтФЦГСЕэЁЃ
ЂкЙ§ТЫЃЌНЋТЫдќМгШШЖјЕУИБВњЦЗЁЃ
ЂлдкТЫвКжаМгШыЯИЪГбЮФЉЃЌдк10Ёц-15ЁцЃЌЪЙNH4ClГСЕэЃЌЙ§ТЫЃЌТЫвКЮЊБЅКЭЪГбЮЫЎЁЃ
ЧыЭъГЩЯТСаЮЪЬтЃК
ЁЁ (1)дкАБЕФБЅКЭNaClШмвКжаЭЈШыCO2ЕФСНВНЗДгІЗНГЬЪНЃК
______ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ___________ЁЃ
ЁЁ (2)ВЛФмдкNaClШмвКжаЭЈШыCO2жЦNaHCO3ЕФдвђЪЧ____________________ЁЃ
ЁЁ (3)ЮіГіаЁЫеДђЕФФИвКжаМгШыЩњЪЏЛвЕФЗДгІЗНГЬЪНЃК_______________ЁЃ
ЁЁ (4)дкЁАКюЪЯжЦМюЗЈЁБжаЃЌ_______ЮяжЪПЩвдбЛЗРћгУЃЌдкЁАЫїЖћЮЌЗЈЁБжа___________ЮяжЪПЩвдбЛЗРћгУЁЃ
ЁЁ (5)ЁАКюЪЯжЦМюЗЈЁБгыЁАЫїЖћЮЌЁБЯрБШЃЌЦфгХЕуЪЧ___________ЁЃ
6ЃЎОнЯЄЃЌАТдЫЛсЩЯЪЙгУЕФЗЂСюЧЙЫљгУЕФЁАЛ№вЉЁБГЩЗжЪЧТШЫсМиКЭКьСзЃЌОзВЛїЗЂГіЯьЩљЃЌЭЌЪБВњЩњАзЩЋбЬЮэЁЃзВЛїЪБЗЂЩњЕФЛЏбЇЗДгІЗНГЬЪНЮЊЃК5KclO3+6P=3P2O5+5KClЃЌдђЯТСагаЙиа№ЪіДэЮѓЕФЪЧ(ЁЁЁЁ )ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
AЃЎЩЯЪіЗДгІжабѕЛЏМСКЭЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ5:6
ЁЁЁЁЁЁ BЃЎВњЩњАзЩЋбЬЮэЕФдвђЪЧЩњГЩЕФP2O5АзЩЋЙЬЬхаЁПХСЃ(бЬ)ЮќЫЎадКмЧПЃЌЮќЪеПеЦјжа
ЁЁЁЁЁЁ ЕФЫЎЗжЃЌЩњГЩСзЫсаЁвКЕЮ(Юэ)
ЁЁЁЁЁЁ CЃЎЩЯЪіЗДгІжаЯћКФ3molPЪБЃЌзЊвЦЕчзгЕФЮяжЪЕФСПЮЊ15mol
ЁЁЁЁЁЁ DЃЎвђКьСзКЭАзСзЛЅЮЊЭЌЗжвьЙЙЬхЃЌЫљвдЩЯЪіЛ№вЉжаЕФКьСзПЩвдгУАзСзДњЬц
5.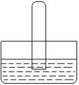 ГЃЮТЯТЃЌЯТСаИїзщЦјЬхЕШЬхЛ§ЛьКЯЃЌГфТњЪдЙмЕЙСЂдкЫЎВлжаЃЌЪдЙмФкЦјЬхЬхЛ§ВЛЛсУїЯдМѕЩйЕФвЛзщЪЧ(ЁЁЁЁ )
ГЃЮТЯТЃЌЯТСаИїзщЦјЬхЕШЬхЛ§ЛьКЯЃЌГфТњЪдЙмЕЙСЂдкЫЎВлжаЃЌЪдЙмФкЦјЬхЬхЛ§ВЛЛсУїЯдМѕЩйЕФвЛзщЪЧ(ЁЁЁЁ )
|
Ђй |
Ђк |
Ђл |
Ђм |
Ђн |
Ђо |
|
NOЁЂO2 |
C2H4ЁЂH2 |
NO2ЁЂO2 |
Cl2ЁЂSO2 |
NH3ЁЂO2 |
COЁЂO2 |
AЃЎЁЁ Ђл ЂнЁЁЁЁЁЁ BЃЎЂк ЂмЁЁЁЁЁЁ ЁЁCЃЎЁЁ Ђк Ђо ЁЁЁЁЁЁDЃЎЂй Ђл
4. ШЁxgЭКЭУОЕФКЯН№ЭъШЋШмгкХЈЯѕЫсЃЌШєЗДгІжаЯѕЫсБЛЛЙджЛВњЩњ8960mLЕФNO2ЦјЬхКЭ672mLЕФN2O4ЦјЬх(ЖМвбелЫуЕНБъзМзДПі)ЃЌдкЗДгІКѓЕФШмвКжаЃЌМгШызуСПЕФЧтбѕЛЏФЦШмвКЃЌЩњГЩГСЕэЕФжЪСПЮЊ17.02gЃЌдђxЕШгк(ЁЁЁЁ )
AЃЎ8.64gЁЁЁЁЁЁЁЁ BЃЎ9.00gЁЁЁЁЁЁ ЁЁCЃЎ9.20gЁЁ ЁЁЁЁЁЁDЃЎ9.44g
3ЃЎгЂЙњбаОПШЫдБ2007Фъ8дТ30ШеЗЂБэБЈИцШЯЮЊЃЌШЋЧђНЋга1.4вкШЫвђЮЊгУЫЎЖјЪмЕНЩщжаЖОжЎКІЃЌЕМжТИќЖрЕФШЫЛМАЉжЂКЃДјКЌЩщГЌБъЃЌОЫЎНўХн24аЁЪБКѓЃЌЦфКЌЩщСПВХФмДяЕНЪГгУАВШЋБъзМЃЌЯТСаЖдЩщ(As)ЕФгаЙиХаЖЯе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎЩщдзгађЪ§ЮЊ33ЃЌЫќгыТСЮЊЭЌжїзхЁЁЁЁЁЁ ЁЁЁЁBЃЎЩщЕФдзгАыОЖаЁгкСзЕФдзгАыОЖ
CЃЎЩщЛЏЧтЕФЮШЖЈадБШфхЛЏЧтЕФЧПЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁDЃЎЩщЫсЕФЫсадБШСђЫсЕФШѕ
2. Ш§ЗњЛЏЕЊ(NF3)ЪЧвЛжжаТаЭЕчзгВФСЯЃЌЫќдкГБЪЊЕФПеЦјжагыЫЎеєЦјФмЗЂЩњбѕЛЏЛЙдЗДгІЃЌЦфЗДгІЕФВњЮягаHFЁЂNOКЭHNO3ЁЃдђЯТСаЫЕЗЈДэЮѓЕФЪЧ
A.ЗДгІЙ§ГЬжаЃЌБЛбѕЛЏгыБЛЛЙдЕФдЊЫиЕФЮяжЪЕФСПжЎБШЮЊ1:2ЁЁ
B.NF3ЪЧвЛжжЮоЩЋЁЂЮоГєЕФЦјЬхЃЌвђДЫNF3дкПеЦјжааЙТЉЪБВЛвзБЛВьОѕ
C.вЛЕЉNF3аЙТЉЃЌПЩвдгУNaOHШмвКХчСмЕФЗНЗЈМѕЩйЮлШО
D.ШєЗДгІжаЩњГЩ1.0 mol NOЃЌзЊвЦЕФЕчзгЪ§ФПЮЊ6.02ЁС1023
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com