
36.(18分)如图所示,水平光滑地面上停放着一辆小车,左侧靠在竖直墙壁上,小车的四分之一圆弧轨道AB是光滑的,在最低点B与水平轨道BC相切,BC的长度是圆弧半径的10倍,整个轨道处于同一竖直平面内.可视为质点的物块从A点正上方某处无初速下落,恰好落入小车圆弧轨道滑动,然后沿水平轨道滑行至轨道末端C处恰好没有滑出.已知物块到达圆弧轨道最低点B时对轨道的压力是物块重力的9倍,小车的质量是物块的3倍,不考虑空气阻力和物块落入圆弧轨道时的能量损失.求:
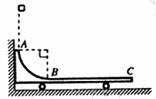 (1)物块开始下落的位置距水平轨道BC的竖直高度是圆弧半径的几倍
(1)物块开始下落的位置距水平轨道BC的竖直高度是圆弧半径的几倍
(2)物块与水平轨道BC间的动摩擦因数μ
35.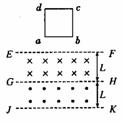 (18分)两个沿水平方向且磁感应强度大小均为B的有水平边界的匀 强磁场,如图所示,磁场高度均为L.一个框面与磁场方向垂直、质量为m,电阻为R,边长为L的正方形金属框abcd,从某一高度由静止释放,当ab边刚进入第一个磁场时,金属框恰好做匀速直线运动;当ab边下落到GH和JK之间的某位置时,又恰好开始做匀速直线运动.整个过程空气阻力不计.求:
(18分)两个沿水平方向且磁感应强度大小均为B的有水平边界的匀 强磁场,如图所示,磁场高度均为L.一个框面与磁场方向垂直、质量为m,电阻为R,边长为L的正方形金属框abcd,从某一高度由静止释放,当ab边刚进入第一个磁场时,金属框恰好做匀速直线运动;当ab边下落到GH和JK之间的某位置时,又恰好开始做匀速直线运动.整个过程空气阻力不计.求:
(1)ab边刚进入第一个磁场时的速度v
(2)ab边刚刚到达第二个磁场下边界JK时的速度v
(3)金属框从ab边开始进入第一个磁场至刚刚到达第二个磁场下边界JK过程中产生的热量Q
34. (1)在用打点计时器验证机械能守恒定律的实验中,质量m=1.00kg的重物自由下落,打点计时器在纸带上打出一
(1)在用打点计时器验证机械能守恒定律的实验中,质量m=1.00kg的重物自由下落,打点计时器在纸带上打出一
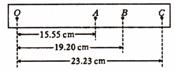
系列点. 如图所示为选取的一条符合实验要求的纸带,O
为第一个点,A、B、C为从合适位置开始选取的三个连续点(其他点未画出).已知打
点计时器每隔0.02s打一次点,当地的重力加速度g=9.80m/s2.那么:
①纸带的 端(选填“左”或“右”)与重物相连;
②根据图上所得的数据,从O点到B点,重物重力势能减少量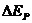 = J,动能增加量
= J,动能增加量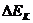 =
J;(结果取3位有效数字)
=
J;(结果取3位有效数字)
③实验的结论是 .
(2)有一阻值 在100-200Ω之间,额定功率为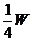 的电阻,现用伏安法较准确测定它的阻值,实验室中备有:
的电阻,现用伏安法较准确测定它的阻值,实验室中备有:
A.量程为50mA,内阻约为20Ω的电流表 B.量程为3A,内阻约为0.01Ω的电流表
C.量程为5V,内阻约为10kΩ的电压表 D.量程为10V,内阻约为20kΩ的电压表
E.值电阻为50Ω,允许通过电流2A的滑动变阻器 F.12V低压直流电源
G.电键、导线
①为保护被测电阻不至烧毁,实验中电阻两端电压应控制在 V以下,电压表应选 ;(填仪器代号)
②为了保护被测电阻,通过它的电流应控制在 A之下,应选的电流表为 ;(填仪器代号)
③根据题意要求画出实验电路图.

33.(16分)已知:环丙烷、环丁烷、环戊烷在催化剂的作用和加热条件下都能与氢气发生类似的反应,如环丁烷与氢气反应可用下列反应式表示: 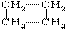
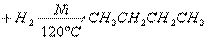 碳原子数不大于4的环烷烃可与卤素、卤化氢发生类似反应,而碳原子数大于4的环烷烃与卤素则发生取代反应。
试填空:
碳原子数不大于4的环烷烃可与卤素、卤化氢发生类似反应,而碳原子数大于4的环烷烃与卤素则发生取代反应。
试填空:
(1)环丙烷、环丁烷与Cl2的反应是 (填反应类型); (2)由环丁烷和Cl2为原料制取1,3-丁二烯的方法是:首先制取 (填结构简式),然后再由它通过 (填反应类型)即得到1,3-丁二烯;
(3)已知二甲苯充分加氢后得到烃A,A再与溴反应时发生取代反应,产物之一为B;B的相对分子质量比A大158;C分子的一取代物只有两种;F的分子式为C16H24O4。一定条件下可以它们可发生下述转化:

写出A和C物质的结构简式:A ;C ; 写出下列反应的化学方程式:
B→D: ;
E→F:__________ _________。
32.(15分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
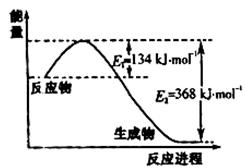 (1)右图是1molNO2和1molCO反应生成
(1)右图是1molNO2和1molCO反应生成
CO2 和NO过程中能量变化示意图,请写出NO2 和CO反应的热化学方程式 ;
 (2)在一定体积的密闭容器中,进行如下化学 反应: N2(g)+3H2(g) 2NH3(g),其化学平衡常数K与温度t的关系如下表:
(2)在一定体积的密闭容器中,进行如下化学 反应: N2(g)+3H2(g) 2NH3(g),其化学平衡常数K与温度t的关系如下表:
|
t/K |
298 |
398 |
498 |
… |
|
K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
完成下列问题:
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”);
②判断该反应达到化学平衡状态的依据是 (填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式 ;
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O] +)+c(H+)= c(H+)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)
31.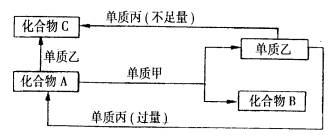 (16分)A、B、C是中学常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质。这些化合物和单质间存在如图所示的转化关系(这些转化都不需要使用催化剂)。回答下列问题:
(1)若甲在转化中为氧化剂,是常见非金属气态单质,丙是常见金属,甲、乙、丙中只有甲由短周期元素组成,乙的组成元素与甲的组成元素同主族,与丙的组成元素同周期,乙也有强氧化性,且反应都是在通常条件下的溶液中进行,则:
①甲是
(填化学式,下同);丙是
;
②A与乙反应的离子方程式是
;
③当A与甲的物质的量之比为2:3时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式是 ;(2)若甲在转化中是还原剂,是常见活泼金属单质;乙是常见非金属固态单质,且甲、乙、丙都是由短周期元素组成。则甲是 (填化学式,下同);乙是 ;丙是
。
(16分)A、B、C是中学常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质。这些化合物和单质间存在如图所示的转化关系(这些转化都不需要使用催化剂)。回答下列问题:
(1)若甲在转化中为氧化剂,是常见非金属气态单质,丙是常见金属,甲、乙、丙中只有甲由短周期元素组成,乙的组成元素与甲的组成元素同主族,与丙的组成元素同周期,乙也有强氧化性,且反应都是在通常条件下的溶液中进行,则:
①甲是
(填化学式,下同);丙是
;
②A与乙反应的离子方程式是
;
③当A与甲的物质的量之比为2:3时,A与甲恰好完全反应,且符合图中所示的转化关系,则反应的离子方程式是 ;(2)若甲在转化中是还原剂,是常见活泼金属单质;乙是常见非金属固态单质,且甲、乙、丙都是由短周期元素组成。则甲是 (填化学式,下同);乙是 ;丙是
。
30.(17分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
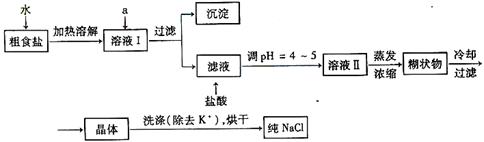
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液
Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_____________ _____(填化学式);滤液中滴加盐酸调PH=4-5的目的是 __ ____;
②选用75%乙醇洗涤除去NaCl晶体表面附带的少量KCl,检验NaCl是否洗净的方法是 ;
 (2)用提纯的NaCl配制480mL 4.00 mol·L-1NaCl溶液,需要称取的质量为 g,所用仪器除药匙、玻璃棒、烧杯外还有_____________(填仪器名称);
(2)用提纯的NaCl配制480mL 4.00 mol·L-1NaCl溶液,需要称取的质量为 g,所用仪器除药匙、玻璃棒、烧杯外还有_____________(填仪器名称);
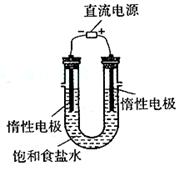
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2 _____(填“>”、“=”或“<”)2L,原因是____ __ ________。
29.(18分)现代生物技术在动植物育种工作中均发挥了巨大的作用。
(1)请根据以下材料回答相关问题。
RNA是生物体内一种重要的生物大分子,它与DNA、蛋白质一起构成了生命的框架。长期以来,科学家一直认为,RNA仅仅是细胞内传递遗传信息的信使。但近年科学家发现,一些RNA小片段能够使特定的植物基因处于关闭状态,这种现象被称作RNA干扰(简称RNAi)。近来,分子生物学家发现RNAi在老鼠和人体细胞中也存在。
①老鼠细胞中有RNA分布的结构有核糖体和 等(至少答出3个)。
 ②RNAi使基因处于关闭状态,使遗传信息传递中的
过程
②RNAi使基因处于关闭状态,使遗传信息传递中的
过程
受阻,最终遗传信息不能以 的形式表达出来。
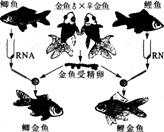
③右图实验中,鲤金鱼、鲫金鱼尾鳍不象金鱼那样是双尾鳍而是
单尾鳍,鲤金鱼、鲫金鱼的后代也是单尾鳍。结合材料一,分析原因
可能是:
。
(2)科学家们通过基因工程技术,培育出了抗软化、保鲜时间长的
番茄新品种。操作流程如下图,请回答:
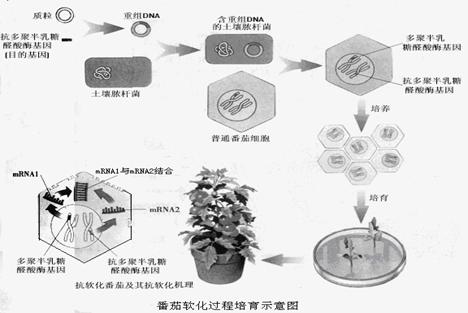
①重组DNA的建构需要的工具酶有限制性核酸内切酶和 。
②在构建基因表达载体时,除了要在重组DNA中插入目的基因外,还需要有启动子、终止子以及__ 。
③从图中可见,mRNA1和mRNA2的结合直接导致了 无法合成,最终使番茄获
得了抗软化的性状。
④普通番茄细胞导入目的基因后,先要接种到诱导培养基上培养,脱分化后得到 ,再转接到分化培养基上,诱导出试管苗,然后进一步培养成正常植株。
28.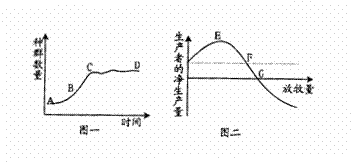 (16分)某生态学家以“保护和利用草原生态系统”为课题,对某草原进行了几项专题研究,并绘制了如下两图。图一表示一个鼠群引入一个草原生态系统后的种群增长曲线;图二表示单位面积放牧量与生产者的净生产量的关系,虚线表示未放牧时,草原中生产者的净生产量。分析回答下列问题:
(16分)某生态学家以“保护和利用草原生态系统”为课题,对某草原进行了几项专题研究,并绘制了如下两图。图一表示一个鼠群引入一个草原生态系统后的种群增长曲线;图二表示单位面积放牧量与生产者的净生产量的关系,虚线表示未放牧时,草原中生产者的净生产量。分析回答下列问题:
(1) 决定鼠群BC段数量变化的直接因素是 。
(2) 图一中的CD段表示鼠群数量不再增长,其原因是 。
(3) 适度放牧可以促进草的分蘖,增加 ,由图二可知,适度放牧可以使草原生态系统的 。
(4)图二中的____点所对应的放牧量为该草原的最大控制放牧量,原因是 。
(5)如果该草原的放牧量长期维持在G点,会引起的后果是 ,该研究结果给我们的启示为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com