
10、下列说法不符合递变规律的是
A. F2、Cl2、Br2、I2的氧化性逐渐减弱
B.HF、HCl、HBr、HI的热稳定性逐渐减弱
C. F-、Cl-、Br-、I-的还原性逐渐增强
D.HF、HCl、HBr、HI水溶液的酸性逐渐减弱
9、在一种酸性溶液中可能存在Fe3+、NO3-、Cl-、I -中的一种或几种离子,向该溶液中滴
入溴水,单质溴被还原,由此推断该溶液中
A.含Fe3+、NO3- ,无I - ,可能有Cl- B.含I -,无Fe3+、NO3-,可能有Cl-
C.含Fe3+、I - ,无NO3-,可能有Cl- D.含NO3- ,无Fe3+、I - ,可能有Cl-
8、实验室保存下列试剂,有错误的是
A. 浓盐酸易挥发,盛在无色密封的玻璃瓶中
B. 碘易升华,保存在盛有水的棕色试剂瓶中
C. 液溴易挥发,盛放在用水密封的用橡皮塞塞紧的棕色试剂瓶中
D. 溴化银保存在棕色瓶中
7、反应⑴是自海藻灰中提取碘的主要反应,反应⑵是自智利硝石中提取碘的主要反应:
2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2 …………⑴
2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2 …………⑵
下列有关说法正确的是
A.NaI 和NaIO3在一定条件下能反应生成I2
B.I2在反应⑴中是还原产物,在反应⑵中是氧化产物
C.两个反应中生成等量的I2时转移的电子数相等
D.氧化性:MnO2>IO3->I2>SO42->Mn2+
6、在密闭容器中盛有H2、O2、Cl2的混合气体通过电火花引燃,3种气体正好反应,
冷却至室温后,所得液体产物浓度为25.26%,则容器中原有H2、O2、Cl2的分子个数比是( )
A、6:3:1 B、9:6:1 C、13:6:1 D、10:6:1
5、氰气的化学式为(CN)2结构为N≡C-C≡N;其化学性质与卤素单质相似,下列叙
述中正确的是( )
A、(CN)2分子中C--C键的键长小于F--F键的键长
A、 氯化钠和氰化银均不溶于水
C、一定条件下,(CN)2可以和不饱和烃起加成反应
D、(CN)2和NaOH的反应可生成NaCN、NaOCN和H2O
4.近年来,加“碘”食盐较多的使用了碘酸钾(KIO3), 碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:
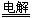 KI+3H2O KIO3+3H2↑。下列有关说法正确的是
KI+3H2O KIO3+3H2↑。下列有关说法正确的是
A.电解时,石墨作阴极,不锈钢作阳极
B.电解时,阴极反应是:I--6e- +3H2O=IO3-+6H+
C.当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g
D.电解前后溶液的pH减小
1、已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱。下列反应在水溶液中不能发生的是
A.3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 B.Cl2 + FeI2 = FeCl2 + I2
C.Co2O3 + 6 HCl = 2CoCl2 + Cl2↑+ 3H2O D.2Fe3+ + 2I- = 2Fe2+ + I2
2同温同压下,下列各组热化学方程式中,△H1<△H2是
A.S(g)+O2(g)=SO2(g); △H1 S(s)+O2(g)=SO2(g);△H2
B.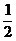 H2(g)+
H2(g)+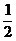 Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g); △H2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g); △H2
C.2H2(g)+O2(g)=2H2O(g); △H1 2H2(g)+O2(g)=2H2O(l);△H2
D.C(s)+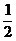 O2(g)=CO(g); △H1
C(s)+O2(g)=CO2(g); △H2
O2(g)=CO(g); △H1
C(s)+O2(g)=CO2(g); △H2
3阿伏加德罗常数约为6.02×1023 mol-1。下列叙述中正确的是
A.1L 0.1 mol·L-1的FeCl3溶液中,Fe3+的数目约为6.02×1022
B.在标准状况下,2.24 L的CCl4中含有C-Cl键的数目约为0.4×6.02×1023
C.7.8 g Na2O2中含有的阴离子数目约为6.02×1022
D.0.1 mol NH2- 离子中所含的电子数约为6.02×1023
13.(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
|
(2)双氧水或过氧化氢;2KClO3====2KCl+3O2↑
14答案:(1)排除锌的颗粒大小、纯度等因素对化学反应速率的影响,使影响反应快慢的唯一因素是c(H+) 比较收集相同体积的H2所需时间(或比较相同时间内收集H2的体积)
15答案:⑴H2O Al(OH)3 (4分)
⑵Fe2++2ClO-+2H2O=Fe(OH)3↓+Cl-+HClO或2Fe2++2ClO-+2H2O+4OH-=2Fe(OH)3↓+Cl- 3ClO-+3H2O=Fe(OH)3↓+3HClO或Fe3++ 3OH-=Fe(OH)3↓)
课后练习
12.(1)2NaBr+Cl2=2NaCl+Br2 ;
(2)3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑
(3) 5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br2+3H2O;(4)加入NaBr溶液。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com