
9.(2008·四川理综,6)下列说法中不正确的是 ( )
A.1 mol氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L
B.1 mol臭氧和1.5 mol氧气含有相同的氧原子数
C.等体积、浓度均为1 mol/L的磷酸和盐酸,电离出的氢离子数之比为3∶1
D.等物质的量的干冰和葡萄糖中所含碳原子数之比为1∶6,氧原子数之比为1∶3
答案 C
8. 已知阿伏加德罗常数为NA,下列说法正确的是 ( )
A.2 mol重水含有NA个D2O分子
B.1 g氢气含有NA个H2分子
C.2 mol钠与过量稀盐酸反应生成NA个H2分子
D.22.4 L水含有NA个H2O分子
答案 C
7.下列有关物理量相应的单位表达错误的是 ( )
A.摩尔质量g/mol B.气体摩尔体积L/mol
C.溶解度g/100 g D.密度g/cm3
 答案 C
答案 C
6.下列选项中所涉及的两个量一定相等的是 ( )
A.11.2 L Cl2与4.25 g NH3所含有的原子数
B.18.0 g重水(D2O)与20 g Ne所含有的电子数
C.标准状况下36 g H2O与1.204×1024个O2分子所占的体积
D.等物质的量的Al分别与足量的盐酸,NaOH溶液反应转移的电子数
答案 D
5.(2008· 西安检测)设NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.32 g以任意比例混合的O2和O3,所含的原子数都为2NA
B.金刚石晶体中有NA个C,就有4NA个C-C键
C.56 g铁与足量盐酸反应,转移电子数为3NA
D.在标准状况下,2.24 L SO3的分子数为0.1NA
答案 A
4.(2009·汉沽一中高三月考)有NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.在标准状况下,V L水含有的氧原子个数为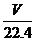 NA
NA
B.常温时,2 L 1 mol/L的甲酸溶液中,所含分子总数小于2NA
C.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
D.1 mol NH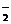 中含电子数为10NA
中含电子数为10NA
答案 D
3.20 g物质A和14 g物质B完全反应,生成8.8 g物质C、3.6 g物质D和0.2 mol物质E。则E的摩尔质量为 ( )
A.100 g·mol-1 B.108 g·mol-1 C.111 g·mol-1 D.123 g·mol-1
答案 B
2. 下列叙述正确的是
( )
下列叙述正确的是
( )
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等
C.1 L一氧化碳气体一定比1 L氧气的质量小
D.等体积、等物质的量浓度的强酸中所含的H+数目一定相等
答案 B
1.下列说法正确的是(N0表示阿伏加德罗常数的值) ( )
①在常温常压下,11.2 L N2含有的分子数为0.5N0
②在常温常压下,1 mol Ne含有的原子数为N0
③71 g Cl2所含原子数为2N0
④在同温同压时,相同体积的任何气体单质所含的原子数相同
A.①② B.②③ C.③④ D.①④
答案 B
279.7 mL。
⑩再称量冷却后试管的质量为15.55 g
(1)在操作⑦中,装置冷却时,玻璃管C的出口,一直要在烧杯的水中,不能离开水面,其理由是_________。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致?
答:______________________________________________________________________________。
(3)标准状况下,1 mol氧气所占的体积(保留小数后两位)为_________L;混合物中MnO2的质量分数为________。
答案 (1)温度降低时,烧瓶内的压强降低,这时烧杯中的水就会回流,从而可以准确地求出气体的体积
(2)如果烧瓶中的压强和外界大气压不一致,就不能准确地求出气体体积。(3)22.38 32%
[实验拓展]
(2008·沈阳模拟)某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
 ①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g。
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g。
②装好实验装置。③检查装置气密性。④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图所示,导管出口高于液面)。⑥测量收集到气体的体积。
⑦准确称量试管和残留物的质量为b g。⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。

回答下列问题:
(1)如何检查装置的气密性?____________________________。
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:________________(请填写步骤代号)。
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同?
答:___________________________________________________。
(4)如果实验中得到的氧气体积是c L(25℃、1.01×105 Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简):M(O2)=_________。
答案 (1)将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后,有少量水进入导管,表明装置不漏气 (2)②①③ (3)慢慢将量筒下移
(4)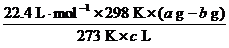
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com