
1.集合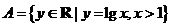 ,
,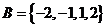 ,则下列结论正确的是
,则下列结论正确的是
A.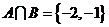 B.
B.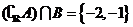
C. 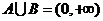 D.
D. 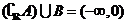
34、甲型H1N1临床实验表明,疫苗对人体安全有效的,对予防传染病有主要意义,以下问题请回答:(10分)
A、为研制甲型H1N1流感灭活病毒疫苗,研究人员设计实验方案应:
(1)制备疫苗:将纯化的甲型H1N1流感病毒在特定的 中培养增殖,收获病毒后用灭活剂杀死,但要确保灭活病毒 不被破坏,且能被免疫细胞识别。
(2)用志愿者检测疫苗刺激机体产生 能力。
(3)上述(2)实验原理为: 。
(4)实验过程:将健康的志愿者分成对照组和多个实验组,每组若干名,对照组处理:
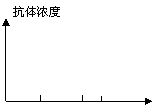

|
 ,实验组接种含
,实验组接种含
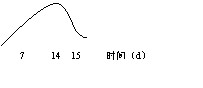 疫苗的接种物。
疫苗的接种物。
(5)右图为某健康成人注射甲型H1N1流感病毒疫苗
后机体中抗体浓度变化图,若此人在注射疫苗后第15
天又感染了该病毒,此时一般不会患病,原因:
。
B、常规疫苗制备成本高,针头注射易感染接种者,有学者提出利用现有基因工程技术,生产可食用疫苗克服常规疫苗所具弊端,其具体做法:①甲型H1N1流感病毒的抗原基因与运载体结合,一般先导入农杆菌,通过农杆菌 植物的离体叶片,可将H1N1流感病毒抗原基因导入叶片细胞的细胞核,并与细胞核的基因组合。
②将该叶片培养成转基因植株的技术是 ,检测是否成功获得转基因植物标志是 。
③基因工程获得食用疫苗与常规疫苗相比,虽然具许多优点,但也存在一些缺点,请写出一例食用疫苗的缺点:
。
33、下表为某人的尿液,原尿和血浆经化验后得到的主要数据,请据此表回答:(11分)
|
|
A液(克%) |
B液(克%) |
C液(克%) |
|
蛋白质 |
微量 |
8 |
0 |
|
葡萄糖 |
0.1 |
0.1 |
0 |
|
无机盐 |
0.75 |
0.75 |
1.25 |
|
尿素 |
0.03 |
0.03 |
1.8 |
|
尿酸 |
0.004 |
0.004 |
0.05 |
(1)表中 为尿液,依据是 。C液中全部重吸收的物质是 ,这种物质被重吸的方式是 。
(2)如果C液中出现蛋白质,表中肾脏的 部位可能发生了病变。
(3)K+也能被肾小管重吸收,但尿液中的K+浓度反而比原尿中还高,原因是 。
(4)尿素由氨基酸经 作用后主要是 部分参与形成。
(5)如果向此人血液中注射醛固酮,则原尿中Na+含量将 K+含量将会 。
(6)如果尿液化验发现有葡萄糖不可能的原因是( )
A、一次性口服大量的糖 B、肾功能障碍
C、胰岛B细胞受损 D、甲状腺激素分泌过多
32、 下图是酵母菌细胞质、核的不均等的分裂图,据图回答(10分)
下图是酵母菌细胞质、核的不均等的分裂图,据图回答(10分)
(1)这种分裂是酵母菌的 生殖。
(2)啤酒的风味主要取决于所采用的酵母菌菌株,
某酒厂的菌株使用了30年,繁殖了三千余代,
风味不减当年,其主要原因是: 。
(3)酿制甜酒时,总是先来“水”,后来酒,其原因是 ,生成
后,再造成 环境,产生 ,写出前面相应反应表达式: 。
(4)糯米饭酿制成甜酒后,其重量会 ,原因是 。
31、下图是某县城及河流的位置:(11分)

在河流的甲、乙、丙、丁地点收集了水样本经分析后:
(1)细菌种群最小的地点是 (编号),细菌种群最大的地点是 ,(编号)在乙、丙、丁菌种群大小表示为 。
(2)在分析甲和乙溶解氧浓度关系是 ,原因是 。
(3)在乙和丁处,藻类的种群大小关系为 ,原因是 。
(4)丁处溶解氧含量逐渐增加的原因是 。
(5)随着农村向城镇化发展,招商引资该县城人口急剧增多,相应工厂也不断增多,那么对该河流的生态会造成最重的威协是 ,我们应采取怎样的措施
河流本身具有
方法(至少答出2条)。
30、有一种有机物I,其合成路线如下:(15分)
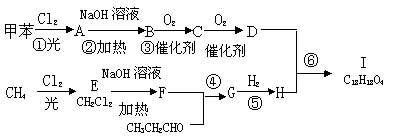
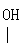

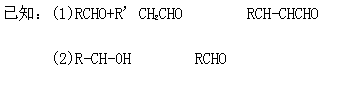



试回答:
(1)反应①-⑥中属于取代反应的有 (填编号) (3分)
(2)G中含有官能团的名称是 。(2分)
(3)F的结构简式是 。(3分)
(4)与D互为同分异物体,既有苯环又能发生银镜反应的物质的结构简式可能
是: 。(4分)
(5)写出反应⑥的化学方程式:(3分)
。
29、实验题:(15分)
定量分析的方法通常有重量法、滴定法、气体体积法等,市售小苏打常会有少量氯化钠,某学习兴趣小组为测定小苏打的纯度,设计了以下实验。
方案I:选用重量法进行测定,可用下图中的装置进行实验。
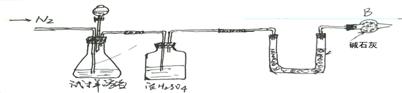
A B C D
(1)实验过程中需要通入N2 次(1分),作用是 。(1分)
(2)该方案需直接测定的物理量是 。(1分)
方案II:选用滴定法进行测定。
(3)称取mg样品,配成100mL溶液,取出20ml用cmol/L的标准HCl溶液滴定,消耗体积为VmL,则该试样中碳酸氢钠质量分数的计算式为: (2分)
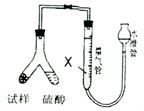
方案III: 选用气体体积法进行测定,可用右图的装置进行实验。(2分)
(4)为了减小实验误差,量气管中加入液体X为 。(2分)
(5)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象的原因可能是( ) (2分)
 A、测定主体体积时未冷却至室温
A、测定主体体积时未冷却至室温
B、测定体体积时水准管的水面高于量气管的水面
C、Y型管中留有反应生成的气体
D、气体进入量气管前未用浓硫酸干燥
方案IV:其操作流程如下:

(6)操作II的名称是 。(2分)
(7)实验中需要的仪器有电子天平、蒸发皿、玻璃棒等,还需要的玻璃仪器是 。
(2分)
(8)在转移溶液时,如溶液转移不完全,则碳酸氢钠质量分数的测定结果 (填“偏
高”、“偏低”或“无影响”) (2分)
28、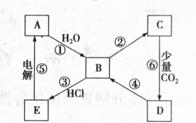 右图表示某典型金属单质A与其化合物之间的转化关系
右图表示某典型金属单质A与其化合物之间的转化关系
(某些产物和反应条件已略去)。已知:图中所示物质中的
组成元素均为短周期元素;化合物C中含有两种同周期
的金属元素;反应⑤用于工业制取A;反应⑥的产物过
滤后得到化合物D的溶液呈碱性。(15分)
(1)一步实现图中①-⑥的转化关系中一定属于复分解反应的(填序号): (3分)
(2)写出一步实一反应④中所需加入的化学试剂(填化学式):
(3分)
(3)写出反应①的离子反应方程式: 。(3分)
(4)B--C中的转化有多种途径,试写出其中两种不同反应类型的化学反应方程式:
。(6分)
27、下图是一个电化学过程的示意图,已知甲 池的总反应式为:(15分)
 2CH3OH+3O2+4KOH
2K2CO3+6H2O
2CH3OH+3O2+4KOH
2K2CO3+6H2O
请回答:
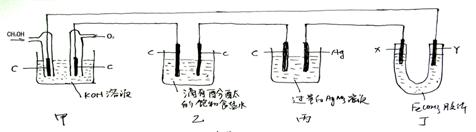
(1)写出通入CH3OH的电极的电极反应式: 。(2分)
(2)丙池中反应的化学方程式为: ,(2分)当丙池中Ag极的质量增加5.40g时,甲池中理论上消耗O2 ml(2分)(标准状况下)乙中溶液的PH是 (2分) (此时乙溶液体积为500ml)。
(3)丁装置X、Y都为惰性电极、一段时间后 极 (填X或Y) (2分)颜色逐渐变浅。原因是: ,(2分)实验室利用饱和FeCl3溶液制Fe(OH)3胶体,请写出制该胶体的化学方程式: 。(3分)
26. 质量 m=1.0kg的甲物体与竖直放置的轻弹簧的上端连接,弹簧下端固定在地面上,如图所示。质量m=1.0kg的乙物体从甲物体正上方,距离甲物体h处自由落下,撞在甲物体上在极短的时间内与甲物体粘在一起(不再分离)向下运动。它们到达最低点后又向上运动,上升的最高点比甲物体初始位置高H=0.10m。已知弹簧的劲度系数k=200N/m,且弹簧始终在弹性限度内,已知弹簧的弹性势能与弹簧的形变量有关。空气阻力可忽略不计,重力加速度g取10m/s2。求:
质量 m=1.0kg的甲物体与竖直放置的轻弹簧的上端连接,弹簧下端固定在地面上,如图所示。质量m=1.0kg的乙物体从甲物体正上方,距离甲物体h处自由落下,撞在甲物体上在极短的时间内与甲物体粘在一起(不再分离)向下运动。它们到达最低点后又向上运动,上升的最高点比甲物体初始位置高H=0.10m。已知弹簧的劲度系数k=200N/m,且弹簧始终在弹性限度内,已知弹簧的弹性势能与弹簧的形变量有关。空气阻力可忽略不计,重力加速度g取10m/s2。求:
(1)甲物体下落的高度h为多少?
(1)乙物体和甲物体碰撞过程中损失的动能;
(2)乙物体和甲物体碰撞后一起向下运动至最低点的过程中,乙物体和甲物体克服弹簧弹力所做的功。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com