
33.(12分)
大麻是XY型性别决定的植物。种植雄麻以收获麻茎纤维为目的,种雌麻以收种子为目的。
(1)雄麻的纤维产量高于雌试,所以麻农希望只种雄麻,不种雌麻。但用传统的繁殖方法获得的种子不可能全为雄麻,而单倍体育种可解决这一问题。请用简洁的文字,说明利用单倍体育种方法获得大量雄麻种子的方案。(假定YY植株可以存活并繁殖)
(2)除(1)中方法外,还可利用 作材料,采用 技术获取大量雄麻。
 34.(10分)
34.(10分)
某研究小组对农田生态系统的各种生态因素进行了
认真考察。下面是他们考察的有关内容和相关建议。请
根据题意完成填空。
(1)农田生态系统的抵抗力稳定性较低,原因是该生态
系统的 简单, 能力较小。
(2)研究人员通过分析蛇的食性,绘制了如右图的食物
关系。蛇所处的营养级是第 营养级;若蛇的食
物有4/5来自鼠,1/5来自蛙。则从理论上讲,蛇
每增加1kJ能量,至少消耗植物 kJ。
(3)建议农民经常进行除草、灭虫,从生态系统能量流动的角度看,建议这样做的目的是 。
(4)收获季节,不少农民在田里焚烧作物秸杆,其主要危害是 ,并造成物质和能量的浪费。对此现象研究人员向有关部门建议,利用秸杆生产“再生纤维共混膜”,这种膜在自然条件下被微生物产生的 酶分解,分解该膜的生物在生态系统成分中称为 。
31.(10分)在可调节温度的温室里栽培番茄,研究昼夜温差对番茄生长的影响,实验结果如下图。请据图回答:
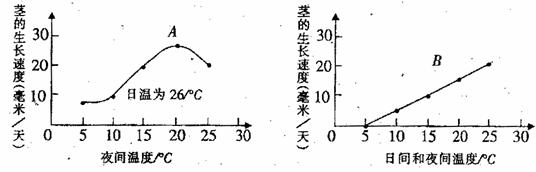
注:①曲线A是番茄植株在日温为26℃,夜温如横坐标所示的温度下测定的数据.
②曲线B是番茄植株在日夜恒定的温度下测定的数据.
(1)夜温15℃时,番茄植株生长速度较快的环境条件是 (填“有昼夜温差”或“日夜恒温”)
(2)在日夜恒定温度的情况下,番茄植株生长最快的温度是____________℃。
(3)昼夜温度差大,对番茄的生长越有利?____________;能证明观点的曲线是
。
(4)番茄植株生长速度最快的温度条件是 ;试从光合作用和细胞呼吸的关系解释其原因: 。
(5)除调控温度外,再写出能提高温室内番茄植株生长速度的两种方法。
、 。
 32.(10分)
32.(10分)
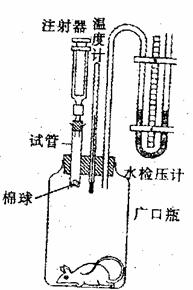
为研究甲腺激素对小鼠新陈代谢的影响,设计了
如下实验装置:500mL广口瓶的瓶差为胶塞,其上三
个小孔分别插温度计、水检压计和一支底部开口的试
管,开口边缘内翻,放一浸透液体的棉球。该装置是
通过测定动物在一定时间内的耗氧量,计算其代谢率。请回答下列问题:
(1)棉球浸透的溶液为 ,
目的是 。
(2)实验步骤:
①选日龄相同、体重相近10只健康的雄性小白鼠。
②将每只小白鼠分别放入以上装置的广口瓶中,
待动物适应测定环境和瓶内的温度稳定后,然后
用注射器(5mL)向广口瓶内注入5mL空气,记
录水检压计右侧液面下降单位刻度所需时间t1。
③给每只小白鼠注射适量的甲状腺激素溶液,在
相同的环境下,按步骤②的方法重测一次。记录
水检压计右侧液面下降单位刻度所需时间t2。
(3)实验分析:
①该实验最可能的结果是:t1 (“<”、“>”或“=”)
②注射甲状腺激素溶液后,小白鼠自身产生的甲状腺激素 (“增加”、“不变”、“减少”),原因是注射后血液中 。
③若环境温度降低,重复上述实验,水检压计右侧液面下降单位刻度所需时间
(“变长”、“不变”、“变短”)。
④该实验设计是否不够严密,缺少对照? ,理由是 。
30.(16分)
已知:

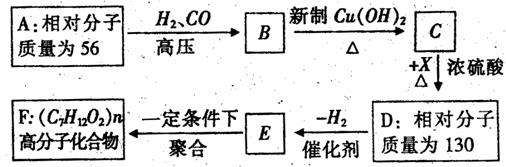 有机物A ~F中,A是链烃,A与H2加成得到烷烃,经测定,该烷烃分子中只有两个-CH3,其一卤代物有两种同分异构体,C与X反应生成D。各物质之是的转化关系如下图所示:
有机物A ~F中,A是链烃,A与H2加成得到烷烃,经测定,该烷烃分子中只有两个-CH3,其一卤代物有两种同分异构体,C与X反应生成D。各物质之是的转化关系如下图所示:
(1)写出X的名称: 。
(2)写出化合物A、E的结构简式:A ,E 。
(3)指出下列反应的类型:C→D ,E→F 。
(4)写出B与足量新制氢氧化铜悬浊液共热时发生反应的化学方程式: 。
(5)有机物G是有机物C不同类型的同分异构体,并且G能与金属钠发生反应放出无色气体,又能发生银镜反应;又知G的同一类型的同分异构体共有多种,则其中只含有一个甲基的同分异构体的结构简式有 、 。(任写两种)
29.(17分)
下图为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去,已知乙醇的沸点为78.5℃),请根据要求完成下列问题(仪器装置可任意选用,必要时可重复选择,a、b为旋钮)。
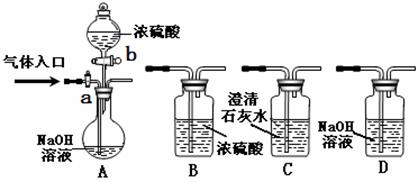

(1)若A中气体入口通入CO和CO2的混合气体,E内放置CuO,欲得到纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为___ ___ (填写装置代号)。能验证CO氧化产物的实验现象是____________ ____。
(2)完成(1)实验后,将A中a旋钮关闭,并在E内放置Na2O2,按A→E→D→B→H装置顺序,制取纯净干燥的O2,并用O2氧化乙醇。
①为获得氧气,关闭a旋钮后,首先需进行的操作是 。
②为得到平稳的乙醇蒸气流,提高反应效率,可采取的措施是(用文字简述)
__________;m中发生反应的化学方程式是____________________________。
③若想观察到试管n中有红色沉淀出现,还需要进行的操作是________ __。
28.(15分)
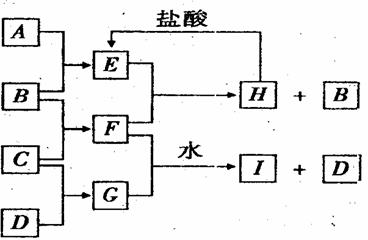 A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
请填写下列空白
(1)A是 ,F的电子式是 。
(2)H与盐酸反应生成E的化学方程式是
。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程式是 。
56.1KJ的热量,试写出硫化氢分解的热化学方
程式: 。
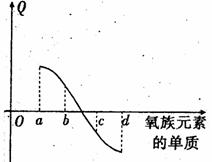
(5)右图所示为氧族元素单质与H2反应过程中的
能量变化示意图,其中a、b、c、d分另表示
氧族中某一元素的单质,Q为相同物质的量
的单质与H2反应放出的热量。则:
a代表 ,c代表
(均可单质名称)
27.(12分)下表是氧族元素的相关性质
|
性质\元素 |
8O |
16S |
34Se |
52Te |
|
单质熔点(℃) |
-218.4 |
113 |
|
450 |
|
单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
|
原子半径 |
逐渐增大 |
|||
|
单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
请根据表回答下列问题:
(1)硒的熔点范围可能是
(2)氢硒酸有较强的 (填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生在化学反应方程式为 。
 (3)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(3)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
□Al2Te3+□ ===Al(OH)3↓+□H2Te↑
(4)已知在常温下,H2和S反应生成17gH2S放出
26.(20分)
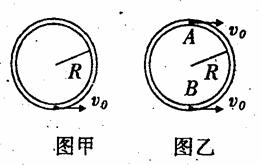
环状空心的细金属管道质量为M,不计一切摩擦。
(1)将管道竖直固定,管内底部有一可视为质点的小球(如图甲),若小球初速度为v0,小球恰能通过最高点,此时球受到管道壁的弹力大小为Mg/2,小球的质量大小为多少?环的半径R为多少(与环的半径相比,管的粗细可不计)?
(2)现将管道水平放置在光滑水平面上,管直径两端A、B处有两个与第一问完全相同的小球(如图乙),初速度仍均为v0,当两球相遇时,小球速度大小为多少?
(3)紧接上问,若两球发生完全弹性碰撞,则当两小球分别回到AB处时,管道的速度大小为多少?
25.(18分)
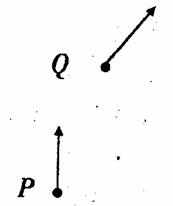
空间中存在水平向右的匀强电场,场强大小为E,一带电量为+q、质量为m的粒子,在P点以向上初速度v0开始运动,该粒子运动到图中Q点时速度方向与P点时的方向偏转了45°,若保持粒子在P点时的速度不变,而将匀强电场换成方向垂直于纸面向外的匀强磁场,在此磁场力的作用下粒子也由P点运动到Q点,不计重力。求:
 (1)P、Q间的距离l为多少?
(1)P、Q间的距离l为多少?
(2)匀强磁场的磁感应强度为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com