
29.(8分)在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:
(1) 猜想与假设
甲认为有H2. CO生成;
乙认为有H2、CO、CO2生成;
丙认为除有H2、CO、CO2外,可能还有N2生成。
探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是____________。
(2) 设计与实验
甲乙同学为了证明他们的猜想是正确的,设计了如下图所示的实验装置:
(提示:无水硫酸铜遇到水变蓝色,H2和CuO反应生成Cu和H2O,CO与CuO反应的原理与工业炼铁的反应原理相似。)

① 证明混合气体中含有H2,相应的反应现象是______________________________;
② 证明混合气体中含有CO,相应的反应现象是_____________________________;
③ 证明混合气体中含有CO2,相应的反应现象是_____________________________。
(3) 理论与思考
① 写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式___________________;
② 丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装_________溶液,才能弥补上述设计的不足。
28.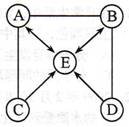 (6分)A、B、C、D、E是初中化学中常见的5种物质。其中B和E是空气中的两种气体,C是铁锈的主要成分。它们之间的转化关系如下图所示,直线表示相互间能够反应,箭头表示转化的方向。
(6分)A、B、C、D、E是初中化学中常见的5种物质。其中B和E是空气中的两种气体,C是铁锈的主要成分。它们之间的转化关系如下图所示,直线表示相互间能够反应,箭头表示转化的方向。
(1) 请写出你的推断结果(写化学式):
B__________;D__________;
(2) 写出能实现下列转化的方程式:
E转化成B的反应________________________________;
A和C的反应____________________________________。
27.(8分)某校初三学生在社会实践活动中发现鱼虾是装在铁箱中进行远距离运送的。输送途中将如何解决鱼的吸氧问题呢?经了解后知道,解决鱼的吸氧问题一般有两种方法;一种是物理方法,即通过增氧泵或直接用瓶装氧气向水中增氧。另一种是化学方法,即向水中加入增氧剂。常用的增氧剂主要有过氧化钙或者过碳酸钠。为了解增氧剂的增氧原理,同学们查阅了有关资料:
资料一:过氧化钙为白色颗粒,化学式为CaO2。干燥的过氧化钙在常温下很稳定,但在潮湿空气中或水中可缓慢反应生成氢氧化钙和氧气,以长时间维持水中的溶解氧……
资料二:过碳酸钠为白色颗粒,化学式为2Na2CO3·3H2O2。该晶体溶于水生成碳酸钠、水和氧气。能长时间维持水中的溶解氧……
根据上述信息,回答下列问题:
(1) 过氧化钙属于____________(填“碱”、“盐”、“氧化物”);
(2) 过碳酸钠晶体具有Na2CO3和H2O2的双重性质,下列物质不会使过碳酸钠晶体失效的是__________;
A.MnO2 B.稀硫酸 C.稀盐酸 D.NaCl
(3) 已知对缺氧池塘过氧化钙的用量是:水深lm,每亩用过氧化钙2kg,以后水深每增加0.5m,每亩增加过氧化钙l kg,现有水深1.5m的池塘10亩。共需加过氧化钙_______kg。
(4) 同学们欲测定所用的过氧化钙样品中过氧化钙的质量分数,现做如下实验:称取样品2.0g,加入到足量的水中,生成224mL氧气(氧气的密度为1.43g/L)。试计算所用样品中过氧化钙的质量分数。(需列式计算)
26.(6分)小亮在化学实验室发现一瓶装有无色溶液的试剂瓶,其标签破损,从残余部分只能看出其溶质的质量分数为10%,具体是什么物质无法辨认。老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠溶液中的一种。
(1)小亮根据信息立即确定该溶液不可能是氢氧化钙,理由是;_________________________
(2)小亮另取样品,滴加无色酚酞试液,试液变红色,该溶液不可能是______________,理由是________________________________________________;
(3)小亮另取样品,加入一定量的稀盐酸,没有气泡产生,该溶液不可能是理由是_________ ____________________________________;
(4)根据以上判断,小亮确定该溶液是___________________。
25.(9分)通过一年的化学学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置,根据下图回答下列问题:
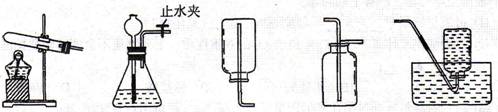
(1) 关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则B装置是否漏气?____________(填“漏气”、“不漏气”或“无法确定”);
(2) 写出实验室用B装置制取氧气的化学方程式___________________________________;
(3) 如果实验室用A装置来制取氧气,同时要收集一瓶用于做蜡烛燃烧实验的氧气,则最好的收集方法是___________;(填字母编号)
(4) 通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水。小枫同学用加热氯化铵和氢氧化钙的固体混合物来制取氨气,他应选择的发生装置是_______________,收集装置是_______________;(填字母编号)
(5) 小雯同学将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是集气瓶内的水面上升,而且水变_______________;(填一种颜色)
(6) 某校化学实验室需要配制1000g溶质质量分数为10%的盐酸用来制取二氧化碳,问需溶质质量分数为38%的盐酸(密度是1.19g/mL)________mL,需要水_________mL。(结果保留1位小数)
24.(3分)用一种试剂及相关操作就可除去下列物质中的杂质(括号内为杂质),写出该试剂的化学式(试剂是溶液的,仅需写出溶质的化学式):
(1) CaC12(CaO)________ (2) KNO3(NaCl)________ (3) NaOH(Na2CO3)________
23.(4分)根据题目要求写出下列反应的化学方程式
(1) 实验室用锌和稀硫酸反应制取氢气_____________________________________;
(2) 已知碱式碳酸铜的化学式为Cu2(OH)2CO3,可以把它看作由Cu(OH)2和CuCO3组成的物质。试写出Cu2(OH)2CO3和稀盐酸反应的方程式(用一个方程式表示)
_____________________________________________________________________。
22.(4分)化学就在我们身边,它能改善我们的生活。请从“A.氧气 B.氮气 C.生石灰 D.熟石灰 E.明矾 F.尿素”中选择适当的物质填空(填字母)。
(1) 抢救危重病人常用的物质是__________; (2) 用于农作物肥料的物质是__________;
(3) 常用作袋装食品干燥剂的是__________; (4) 净化水时可作絮凝剂的是___________。
21.(4分)用相应的化学符号填空
(1) 5个氨气分子______________; (2) 1个铜原子________________;
(3) 2个碳酸根离子____________; (4) 氢氧化铁中铁元素的化合价为+3价___________。
20.溶液的碱性强弱跟溶液中OH-的数量有关。一定体积的溶液中OH-数量越多,则溶液碱性越强。10%的NaOH溶液(密度为1.1 g/cm3)与10%的KOH溶液(密度也为1.1g/cm3)相比较,碱性更强的是( )
A.NaOH B.KOH C.一样强 D.无法比较
第1I卷(非选择题共60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com