
20.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选择其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.由徐光宪院士发起, 院士学子同创的《分子共和国》科普读物最近出版了,全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、 H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星。
(1)下列说法正确的是 ▲ 。
 (a)BF3和NH3都是含有极性键的非极性分子
(a)BF3和NH3都是含有极性键的非极性分子
(b)CO2、HCN分子中都含有两个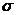 键和两个π键
键和两个π键
(c)H2S、O3分子都是直线形w ww.k s5u. co m
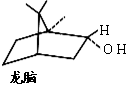
(d)一种双环单萜龙脑(如右图)分子中有4个手性碳原子
(2)NO是人体中的信号分子,有关说法正确的 ▲ 。
 (a)第一电离能N大于O (b)电负性O大于N
(a)第一电离能N大于O (b)电负性O大于N
(c)NO+的结构为:N≡O+
(d)N、O元素在周期表中都处于p区
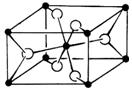
(3)TiO2的天然晶体中,最稳定的一种晶体结构如右图,白球表示: ▲ 原子。
 (4)二茂铁(C5H5)2Fe是Fe2+与环戊二烯基形成的一类配合物,其中Fe2+在基态时核外电子排布式为: ▲ ;实验室测定铁的含量可用配位剂邻二氮菲(
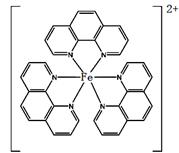
(4)二茂铁(C5H5)2Fe是Fe2+与环戊二烯基形成的一类配合物,其中Fe2+在基态时核外电子排布式为: ▲ ;实验室测定铁的含量可用配位剂邻二氮菲( ),它能与Fe2+形成红色配合物(如右图),该配离子中Fe2+配位数为 。
),它能与Fe2+形成红色配合物(如右图),该配离子中Fe2+配位数为 。
(5)乙酸熔沸点很高,是由于存在以分子间氢键缔合的二聚体(含一个环状结构),请画出这二聚体的结构: ▲ 。
B.聚合氯化铝(PAC)可以看成是AlCl3水解成为Al(OH)3的中间产物,其化学通式为[Al2(OH)nCl6-n]m(m≤10,n=3-5)。若式中,n接近于6或等于6,则可称为铝溶胶。聚合氯化铝是一种无机高分子混凝剂。某合作学习小组的同学在查阅文献资料后拟用不同的方法制备聚合氯化铝。w ww.k s5u. co m
(1)甲组用凝胶-溶胶法,它们用结晶氢氧化铝、烧碱、CO2及盐酸为试剂生产,其中涉及的氢氧化铝与烧碱反应的化学方程式为: ▲ 。
(2)乙组采用不足量酸溶法,原料主要是铝加工的下脚料铝屑、铝灰和铝渣等,反应原理为:2Al +(6-n)HCl+nH2O = Al2(OH)nCl6-n+3H2↑。该制备方法工艺简单、成本低,利用本身是放热反应,故不需要加热,可能缺点有: ▲ (列举一条)。
(3)丙组拟用高岭土(Al2O3•2SiO2•2H2O)等为原料,经焙烧、盐酸浸取、聚合、熟化、蒸发、干燥等步骤得到固体PAC。其中液体PAC蒸发时,适宜在110℃左右,你认为适宜的加热方法是 ▲ 。
(4)丁组同学对甲、乙、丙组同学制得的样品进行定性实验,请你补充下列实验报告
|
实验序号 |
实验步骤 |
实验现象 |
结论 |
|
① |
用激光笔照射甲组制得的PAC溶液 |
光亮的通路 |
▲ |
|
② |
取乙组制得的样品少许加入铝试剂阿罗明拿 |
变成玫瑰红色 |
▲ |
|
③ |
取丙组样品少许,溶于适量的水制得的淡黄色透明液体中加入氟化铵 |
▲ |
▲ |
(5)戊组同学对丙组固体样品请质检部门用27Al-NMR测试,其中的分散质主要是:Al13O4(OH)24Cl7,属于优质产品。他们另取样品mg少许放在坩埚中充分加热并灼烧,最终得到的固体产物为: ▲ ,若得到固体ng,则制得的样品中铝的质量分数为 ▲ 。



19.(10分)合成氨联产二甲醚是一项具有中国特色的化工工艺,具有节能环保,其主要工艺流程如下:


 已知造气时,主要发生的反应有:CH4+H2O→CO+3H2………①;2CH4+O2→2CO+4H2………②。
已知造气时,主要发生的反应有:CH4+H2O→CO+3H2………①;2CH4+O2→2CO+4H2………②。
CO、CO2均可与H2合成甲醇,合成甲醇后排出的醇后气中有很少量的CO、CO2,需与H2转化为甲烷,防止CO使合成氨催化剂中毒。
(1)NH3(g)→NH3(l) △H ▲ 0 (填:“>”、“<”或“=”,下同) ; △S ▲ 0。
(2)相同体积的天然气,采用“合成氨同时联产二甲醚”和直接合成氨相比,新工艺优越性有 。w ww.k s5u. co m
(a)减少二氧化硫排放 (b)适应低碳经济
(c)可提高氮肥产量 (d)资源综合利用率和经济效益高
(3)在催化剂、高温、高压下,CO2转化为甲烷的化学方程式为 ▲ 。
(4)假定造气时产生的转化气中不含CO2, H2与CO物质的量之比为2.2,空气由80%N2和20%O2组成,天然气中CH4为100%,且①和②的转化率均为100%。则同温同压下通入的空气和水蒸气的体积比,V(空气)/V(水蒸气)= ▲ 。
(5)今有224m3(已折合成标准状况)由CO、H2、N2组成的混合气体,分别合成甲醇和氨,且三种气体均完全转化,驰放气中甲烷忽略不计,若得到液氨34kg,则同时得到二甲醚多少千克? ▲ w ww.k s5u. co m
18.(12分)吲哚昔酚 (idoxifene)可用于治疗骨质疏松症,它的合成路线如下:
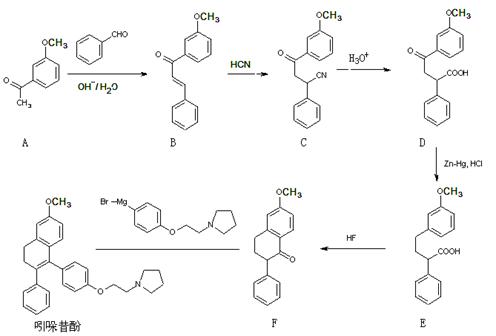
图表 1高 考 资 源 网
(1)反应类型:B→C ▲ ;D→E ▲ 。
(2)D中含氧官能团有: ▲ (写名称)。
(3)满足下列三个条件的A的同分异构体数目有 ▲ 种。
①苯的衍生物,且苯环上只有两个互为对位的取代基;②能发生银镜反应;
③与FeCl3溶液作用不显色
(4)E→F中还有一种副产物G生成,G与F互为同分异构体,且含有三个六员环,G结构简式为: ▲ 。w ww.k s5u. co m
(5)2,2-二甲基戊酸[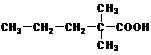 ]是有机合成中间体,请设计合理的方案以丙酮(
]是有机合成中间体,请设计合理的方案以丙酮(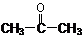 )为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件)。
)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件)。
提示:①合成过程中无机试剂任选;②丙酮分子间能发生上图合成路线中A→B的类似反应;③合成路线流程图示例如下:
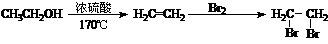
▲
17.(8分)纳米TiO2作为一种光催化剂越来越受到人们的关注,现正广泛开发运用。
(1)制取纳米TiO2的方法很多,氢氧火焰水解法是将TiCl4气体导入氢氧火焰中(700-1000℃)进行水解,其化学反应式为: ▲ 。
 (2)纳米二氧化钛可光解挥发性有机污染物(VOCs),若无水蒸气存在,三氯乙烯降解反应为:C2HCl3+2O2→2CO2+HCl+Cl2,若有足够量的降解后的尾气,实验室检验产物中有氯气的简单方法是: ▲ ;通过质谱仪发现还有多种副反物,其中之一为:
(2)纳米二氧化钛可光解挥发性有机污染物(VOCs),若无水蒸气存在,三氯乙烯降解反应为:C2HCl3+2O2→2CO2+HCl+Cl2,若有足够量的降解后的尾气,实验室检验产物中有氯气的简单方法是: ▲ ;通过质谱仪发现还有多种副反物,其中之一为: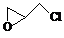 ,则该有机物核磁共振氢谱有 ▲ 个峰。
,则该有机物核磁共振氢谱有 ▲ 个峰。
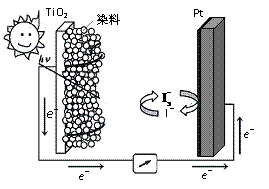
(3)利用半导材料TiO2与染料、铂电极及I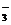 和I-的混合物作电解质(I2+I-
和I-的混合物作电解质(I2+I- I
I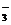 ),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为: ▲ 。
),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为: ▲ 。
(4)在不同的载体(钛片、铝片、陶瓷)表面制备二氧化钛薄膜,来考察不同载体TiO2薄膜光催化使甲基橙脱色,每次光照20min取一次样,实验结果如下。w ww.k s5u. co m
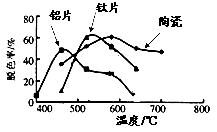 下列说法正确的是 ▲ 。
下列说法正确的是 ▲ 。
(a)不同载体,无论何种温度一定是钛片最好
(b)约在520℃时,钛片载体的光催化活性最好
(c)无论何种载体,催化活性总是随温度的升高而升高
(d)不同负载TiO2薄膜的光催化活性不同
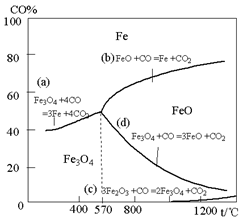
16.(10分)钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如下图:
 (1)铁在元素周期表中位于 ▲ 周期 ▲
族
(1)铁在元素周期表中位于 ▲ 周期 ▲
族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有:
▲ (选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是 ▲ 。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
|
反应序号 |
化学反应 |
反应热 |
|
① |
Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g) |
△H1= -26.7kJ·mol-1 |
|
② |
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) |
△H2= -50.8kJ·mol-1 |
|
③ |
Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g) |
△H3= -36.5kJ·mol-1 |
|
④ |
FeO(s)+CO(g)=Fe(s)+CO2(g)
|
△H4 |
反应④△H4= ▲ kJ·mol-1。
(5)1100℃时, FeO(s)+CO(g)
 Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为: ▲ 。w ww.k
s5u. co m
Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为: ▲ 。w ww.k
s5u. co m
15.(8分)汞不溶于水,易挥发,易与许多金属形成合金,汞是对人体危害较大的一种金属,据统计世界上有80多种工业以汞为原料,生产过程中产生的汞的污染越来越引起人们的重视,水体中的无机汞主要有Hg2+、Hg22+。
(1)实验时倘若不慎,将汞溅落地面时,可先用涂上X溶液的锌片去粘拾,然后再用足量的X溶液溶解锌片回收汞,X溶液可以是 ▲ (填试剂名称)。
(2)检测水体中的Hg2+可用KI及CuSO4溶液与其反应生成橙红色Cu2HgI4沉淀,用漫反射光谱直接测定汞沉淀物,该反应的离子方程式可表示为: ▲ 。
(3)冶金厂治理含汞、含硫的烟气并回收汞,中国冶金工作者在研究Hg-I-H2O系热力学的基础上,查明KI溶液能有效吸收汞,吸收总反应为:2Hg+SO2+8I一+4H+ =2HgI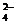 +S+2H2O,最后进行电解吸收液(K2HgI4),阴极的电极反应式为: ▲ 。
+S+2H2O,最后进行电解吸收液(K2HgI4),阴极的电极反应式为: ▲ 。
(4)国家制定的工业废水排放标准:汞的含量≤0.05 mg/L。某合作学习小组的同学拟用硫化钠法处理含汞废水,其步骤为:先将溶液pH调至8-10,然后加入稍过量的硫化钠溶液,最后加入一定量的FeSO4溶液,过滤后排放。已知:25℃HgS的Ksp= 4×10-52;Hg2S的Ksp=1.0×10-47,FeS 的Ksp=6.3×10-18;HgS+Na2S Na2HgS2(易溶)。
Na2HgS2(易溶)。
①若操作程序完全正确,且废水中只含无机汞,上述处理后的废水能否达标排放 ▲(选填:“能”或“不能”)
②加入FeSO4溶液的作用是 ▲ 。w ww.k s5u. co m
14.(8分)以天然盐湖资源中分离出来的芒硝、硫酸工业废气二氧化硫及焦炭等为原料,生产大苏打和摩尔盐,其原料的综合利用率较高。其主要流程如下:
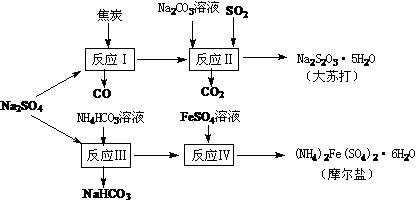
试回答下列问题:w ww.k s5u. co m
(1)已知反应Ⅰ中发生的主要反应为:Na2SO4(s)+4C(s)= Na2S(s)+4CO(g)△H=+569.99 kJ/mol,欲使该反应发生并维持该反应进行的条件是 ▲ 。
(a)常温 (b)常温,并通入少量CO2 (c)高温,并通入适量的O2
(2)配平反应Ⅱ的化学方程式: □Na2S+□Na2CO3+□SO2 =□Na2S2O3+□CO2 ▲
(3)反应Ⅲ温度需控制在35-40℃的较低温度,其主要原因是 ▲ 。
(4)在摩尔盐溶液中加入一种物质的溶液可使NH4+、Fe2+、SO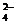 都大量减少,该物质是
都大量减少,该物质是
▲ 。
(5)反应Ⅳ中两种盐溶液混合时,需加入适量的H2SO4,将溶液pH调到1,用离子方程式说明原因: ▲ 。
13.(10分)三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化,碱性条件下能被H2O2氧化为Cr(Ⅵ)。制三氯化铬的流程如下:
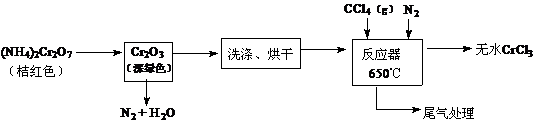
(1)重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)需用蒸馏水洗涤的原因 ▲ ,如何用简单方法判断其已洗涤干净 ▲ 。w ww.k s5u. co m
(2)已知CCl4沸点为57.6℃,为保证稳定的CCl4气流,适宜的加热方式是 ▲ 。

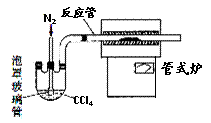 (3)用右图装置制备CrCl3时,主要步骤包括:①将产物收集到蒸发皿中;②加热反应管至400℃,开始向三颈烧瓶中通人氮气,使CCl4蒸气经氮气载人反应室进行反应,继续升温到650℃;③三颈烧瓶中装入150mLCCl4,并加热CCl4,温度控制在50-60℃之间;④反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;⑤停止加热CCl4,继续通人氮气;⑥检查装置气密性。正确的顺序为:⑥→③→ ▲ 。
(3)用右图装置制备CrCl3时,主要步骤包括:①将产物收集到蒸发皿中;②加热反应管至400℃,开始向三颈烧瓶中通人氮气,使CCl4蒸气经氮气载人反应室进行反应,继续升温到650℃;③三颈烧瓶中装入150mLCCl4,并加热CCl4,温度控制在50-60℃之间;④反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;⑤停止加热CCl4,继续通人氮气;⑥检查装置气密性。正确的顺序为:⑥→③→ ▲ 。
(4)已知反应管中发生的主要反应有:Cr2O3 + 3CCl4 → 2CrCl3 + 3COCl2,因光气剧毒,实验需在通风橱中进行,并用乙醇处理COCl2,生成一种含氧酸酯(C5H10O3),用乙醇处理尾气的化学方程式为 ▲ 。
(5)样品中三氯化铬质量分数的测定
称取样品0.3300g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O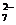 存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
已知:Cr2O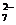 +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2===Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2===Na2S4O6+2NaI。
①该实验可选用的指示剂名称为 ▲ 。w ww.k s5u. co m
②移入碘量瓶的CrCl3溶液需加热煮沸,加入Na2O2后也要加热煮沸,其主要原因是 ▲ 。
③样品中无水三氯化铬的质量分数为 ▲ 。
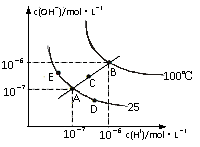
12.水的电离平衡曲线如右图所示,下列说法不正确的是
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显酸性
第Ⅱ卷(非选择题 共78分)
11.直接NaBH4/H2O2燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是
A.电极B材料中包含MnO2层,MnO2可起催化作用
B.电池负极区的电极反应为:w ww.k s5u. co m
BH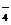 +8OH――8e-=BO
+8OH――8e-=BO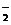 +6H2O
+6H2O
 C.放电过程中,Na+ 从正极区向负极区迁移
C.放电过程中,Na+ 从正极区向负极区迁移
D.在电池反应中,每消耗1L 6 mol/LH2O2溶液,理论
上流过电路中的电子为6NA个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com