
8.设奇函数 上是增函数,且
上是增函数,且 对所有的
对所有的 都成立,当
都成立,当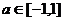 时,则t的取值范围是 ( )
时,则t的取值范围是 ( )
A. B.
B.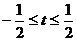
C. D.
D.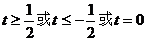
第Ⅱ卷(非选择题 共110分)
7.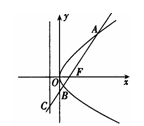 如图,过抛物线
如图,过抛物线 的焦点F的直线l交抛物线于点A、B,交其准线于点C,若
的焦点F的直线l交抛物线于点A、B,交其准线于点C,若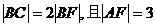 ,则此抛物线的方程为( )
,则此抛物线的方程为( )
A.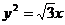 B.
B.
C. D.
D. 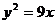
6. 若变量 满足
满足 则
则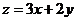 的最大值是( )
的最大值是( )
A.90 B.80 C.70 D.40
5.设向量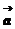 与
与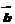 的夹角为
的夹角为 ,
,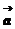 =(2,1),3
=(2,1),3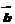 +
+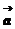 =(5,4),则
=(5,4),则 =( )
=( )
A. 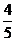 B.
B.  C.
C.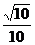 D.
D.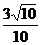
4. 如右图,一个空间几何体的主视图和左视图都是边长为1的正三角形,俯视图是一个圆,那么几何体的侧面积为( )
 A.
A.  B.
B. 
C. D.
D.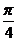
2. 已知函数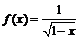 的定义域为M,g(x)=
的定义域为M,g(x)= 的定义域为N,则M∩N=( )
的定义域为N,则M∩N=( )
A.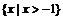 B.
B.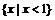 C.
C.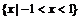 D.
D.
3  中,
中, ,
, ,
,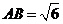 ,则
,则 ( )
( )
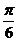 B.
B.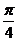 C.
C.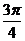 D.
D.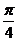 或
或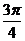
有一项是符合题目要求的)
1. 已知复数 ,则
,则 ( )
( )
A. 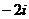 B.
B. C.
C. D.
D.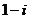
29.(15分)A、B、C、X、Y五种短同期元素,它们的原子序数依次增大。①A元素组成的单质是密度最小的物质;②B元素原子的最外层电子数是其内层电子总数的2倍;③X原子的电子层数与最外层电子数之比为3:1;④Y元素的最外层电子数是其次外层电子数的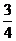 倍;A、B、X、Y四种元素,每一种均能与C元素形成原子个数比不相同的若干化合物。请回答下列问题:
倍;A、B、X、Y四种元素,每一种均能与C元素形成原子个数比不相同的若干化合物。请回答下列问题:
(1)写出B、C两种元素中,只由一种元素的原子构成的常见离子的符号: (至少两个);
(2)写出常温下Y的氢化物与其最高价氧化物对应水化物的浓溶液反应的化学方程式,并用单线桥表示电子转移情况 ;
(3)向含1 mol Na2SiO3的溶液中缓慢通入过量BC2,反应的离子方程式是
;
(4)反应快慢是化工生产考虑的重要因素。请选用以上元素组成的化合物,写出一个使用催化剂增大反应速率的工业生产实例: (用化学方程式表示);
 (5)BA4是一种重要能源物质,右图是1.01×105Pa下,1 mol BA4燃烧生成稳定化合物过程中的能量变化示意图,其热化学方程式为:
;
(5)BA4是一种重要能源物质,右图是1.01×105Pa下,1 mol BA4燃烧生成稳定化合物过程中的能量变化示意图,其热化学方程式为:
;
(6)甲、乙依次是X、Y两种元素最高价氧化物的水化物。常温,将一定浓度甲溶液逐滴加入到20.00mL 0.1mol/L的乙溶液中。
I.若反应后混合溶液的pH如下表(设溶液混合后体积不变,且lg2=0.3),请填写空白:
|
实验编号 |
甲溶液的体积(mL) |
乙溶液的体积(mL) |
混合溶液的pH |
|
1 |
10 |
20 |
|
|
2 |
25 |
20 |
7.0 |
II.若甲溶液在空气中放置时间较长,为了准确测定原甲溶液的浓度,可选试剂 。
A.酚酞 B.甲基橙 C.石蕊
28.(16分)已知:
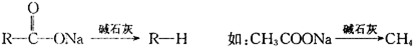
i.
ii.
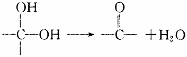
iii.有机物中,一个碳原子上若连有两个羟基不稳定。如:
从有机物X(C11H12O3)出发可发生下图所示的一系列变化(方框中字母各代表一种有机物)。
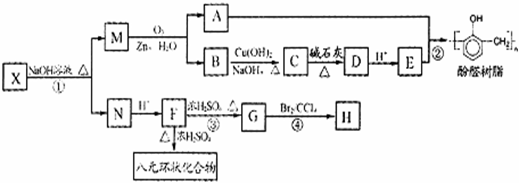
(1)F分子中碳、氢、氧的质量之比为6:1:8,其相对分子质量大于60,小于120。则F的结构简式为 ;
(2)反应③的产物除G之外,还有一些副产物,请写出其中2种类型不同的产物的结构简式
、
;


(3)M酸化后的产物Y是生产高分子光阻剂的主要原料。Y具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯取代产物只有两种。则M的结构简式为 ;
Y在一定条件下发生加聚反应的化学方程式为 ;
(4)在上述①-④变化中,属于消去反应的是 (填反应编号);
B与新制Cu(OH)2反应的化学方程式为 ;
(5)X、E的结构简式分别为: 、 ;
(6)物质A也可以用甲烷和必要的无机原料分两步制备,写出反应的化学方程式:
。
27.(13分)A、Y为常见金属单质,X为常见非金属单质。常温下X、G、H、I为气体,C为液体。B是由三种元素组成的盐,加热时发生分解生成两种气体,冷却后又可化合得到B。有关物质之间的转化关系如下图(部分反应条件及生成物略去)

 高☆考♂资♀源?网 ☆
高☆考♂资♀源?网 ☆
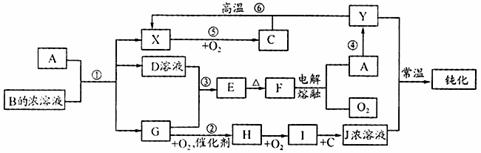
请填写下列空白:
(1)B的电子式为 ;
(2)现用A与石墨作电极,B的浓溶液作电解质溶液,构成原电池。其正极反应式为
;
(3)反应⑥的化学方程式为 ;反应④在冶金工业上属于(填金属的冶炼方法);
(4)从D的结晶水合物制备D的无水晶体的操作为 ;
(5)反应②的化学方程式为 ;
反应③的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com