
13.(东城区)下列叙述中符合历史史实的是
A.卢瑟福的α粒子散射实验揭示了原子核内部有复杂结构
B.玻尔理论成功地解释了各种原子的发光现象
C.爱因斯坦成功地解释了光电效应现象
D.牛顿提出的质量不变性是狭义相对论的基本假设之一
13.(崇文区)下列说法中不正确的是
A.在α粒子散射实验中,使少数α粒子产生大角度偏转的力是原子核对粒子的库仑斥力
B.氢原子在辐射出一个光子后,核外电子的动能增大
C.已知氦原子的质量m1、电子质量m2、质子质量m3、中子质量m4,则质子和中子在结合成氦核时的质量亏损为(2 m4+2 m3-m1)
D.爱因斯坦狭义相对论的基本结论之一是运动物体长度会收缩,即l =l0  ,它是因时空条件不同而引起的观测效应
,它是因时空条件不同而引起的观测效应
13.(朝阳区)通过α粒子散射实验 ( )
A.发现了电子 B.建立了原子的核式结构模型
C.爱因斯坦建立了质能方程 D.发现某些元素具有天然放射现象
30.(9分)研究性学习小组选择“H2O生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
[假设]H2O2发生反应生成O2的快慢与催化剂种类有关.
[实验方案]常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间.
[进行实验]下图是他们进行实验的装置图.
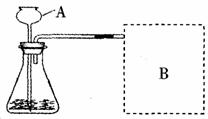
气体发生装置中A仪器名称是_________,此实验中B处宜采用的气体收集方法是_______.
[实验记录]
|
实验编号 |
1 |
2 |
|
反应物 |
5%H2O2 |
5%H2O2 |
|
催化剂 |
1g水泥块 |
1gMnO2 |
|
时间 |
165秒 |
46秒 |
[结论]该探究过程得出的结论是_____________________________________.
[反思]H2O。在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2
和水泥块是该反应的催化剂.还需要增加实验来验证它们在化学反应前后的_______是
否改变.
H2O2发生反应生成O2的快慢与哪些因素有关?请你帮助他们继续探究.(只要求提出
一种影响H2OO发生反应生成O2快慢的因素以及相关假设和实验方案)
[假设]_________________________________________________________.
[实验方案]______________________________________________________________
_____________________________________________________________________.
29.(3分)请你按下列要求填写实验室制取二氧化碳的实验步骤:
(1)按要求连接装置;
(2)检查装置_________;
(3)向广口瓶中装_________(或_________);
(4)向长颈漏斗中加入_________;
(5)用__________法收集CO 2;
(6)用__________放在_________验满.
28.(6分)课外小组的同学从某工厂收集到一些混有少量小铁片的细小铜片.
(1)为了除去混合物中的铁,同学们预想出三种方法:
方法一:用磁铁.该方法属于_________(填“物理”或“化学”)方法.
方法二:用稀硫酸.该方法还可以制得的气体是_________.
方法三:用硫酸铜溶液.请写出该方法涉及的化学方程式.____________.
(2)上述第________种方法操作最简便.
(3)在实际操作中,同学们发现“方法三”不能在短时间内将铁除净,原因是________
______________________________________________.
27.(5分)石灰石是一种重要的矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
|
实验 步骤 |
①称取烧 杯的质量 |
②将适量盐酸加 入烧杯中并称重 |
③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 |
④待反应完 全后,称重 |
|
实验 图示 |
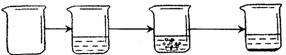 |
|||
|
实验 数据 |
烧杯的质量 为50.0g |
烧杯和盐酸的质 量为100.0g |
石灰石样品的质量为12.0g |
烧杯和其中混合物的质量为107.6g |
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)
26.(3分)(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分.)
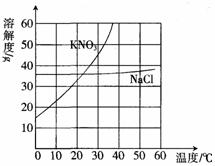
a.下图表示NaCl和KNO3的溶解度曲线,完成下列问题:
(1)_________℃时,NaCl和KNO3的溶解度相等.
(2)20℃时,40gKNO3________(选填“能”或“不能”)完全溶解在100g水中.
(3)从NaCl的饱和溶液中得到NaCl固体,最好采用的方法是___________.
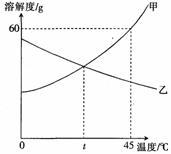
b.下图是甲、乙两种固体物质的溶解度曲线.
(1)t℃时,甲、乙两种物质的溶解度相等,此时这两种溶液中溶质的质量分数_________
(选填“是”或“不”)_________相等的.
(2)将45℃时的一定量甲溶液恒蒸发20g水,会有__________g甲固体析出.
(3)从甲的饱和溶液中得到甲固体,最好采用的方法是__________.
25.(4分)下图所示的转化关系中,A、B、C为常见的气体,其中B常温下是一种液体.D为黑色固体.

试填空.
(1)绿色固体俗称_________.
(2)A的化学式:_________.
(3)反应③的化学方程式为:____________________________.
(4)反应①的化学方程式为:___________________________.
24.(10分)完成下列反应的化学方程式,并回答有关问题.
(1)煅烧石灰石制生石灰:
__________________,该反应是__________(选填“吸热”或“放热”)反应.
(2)铝制容器表面致密氧化膜的生成:
___________________,基本反应类型是_________.
(3)酸雨中含有的极少量硫酸对桥梁、铁轨等钢铁制品的腐蚀:
___________________,基本反应类型是____________.
(4)一种可再生能源物质的燃烧反应:
___________________,它将化学能转化为_____________.
(5)用赤铁矿冶炼铁的主要化学反应原理:
_____________________,工业炼铁的主要设备是__________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com