
18、等量NaOH分别用pH=2和pH=3的醋酸中和,消耗二者的体积依次为Va和Vb,则Va和Vb的关系为
A、Va = 10Vb B、Va < 10Vb C、Va >10Vb D、 Vb >10Va
17、100℃时,Kw=10-12,将100℃时pH=10的NaOH溶液和pH=1的H2SO4混合,所得混合溶液的pH=2,则NaOH溶液和H2SO4溶液的体积比是
A、11 : 1 B、9 : 2 C、12 : 11 D、9: 1
16、 某链烃在一定条件下可和H2发生反应,取不同体积比的CnHm与H2(两者的体积和为定值V)在一定条件下反应,V与Φ(CnHm)、[CnHm的体积分数]的关系如图。则m和n的关系是:
某链烃在一定条件下可和H2发生反应,取不同体积比的CnHm与H2(两者的体积和为定值V)在一定条件下反应,V与Φ(CnHm)、[CnHm的体积分数]的关系如图。则m和n的关系是:
A.m=2n+2 B.m=2n
C.m=2n-2 D.m=2n-6
15、草酸(H2C2O4)溶液与酸性KMnO4溶液反应,在两溶液混和时看不到明显现象,但过一段时间后,混和溶液突然迅速褪色,此反应的化学方程式为:
2KMnO4 + 3H2SO4 + 5H2C2O4 === K2SO4 + 2MnSO4 + 10CO2 + 8H2O,
据你的分析,突然褪色的原因可能是:
A.溶液已混和均匀了 B.反应中溶液酸性减弱
C.生成微量的Mn2+起催化作用 D.增大了外界的压强
14、已知某饱和溶液的:①溶液的质量 ②溶剂的质量 ③溶液的体积
④溶质的摩尔质量 ⑤溶质的溶解度 ⑥溶液的密度
从以上条件的组合上,不能用来计算该饱和溶液的物质的量浓度的是:
A.①④⑥ B.④⑤⑥ C.①②③④ D.①③④⑤
13.下列物质没有固定的熔沸点的是
A.氯化钾 B.五氧化二磷 C.玻璃 D.盐酸
12. 氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生.下列叙述不正确的是
氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生.下列叙述不正确的是
B.NH4H固体投入少量水中,有两种气体产生
C.NH4H中的H-离子半径比锂离子半径大 D.NH4H溶于水后,形成的溶液显酸性
11. 下表给出几种氯化物的熔点和沸点
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
熔点(℃) |
801 |
712 |
190 |
-68 |
|
沸点(℃) |
1465 |
1418 |
|
57 |
关于表中所列四种氯化物的下列说法:①氯化铝在加热时升华,②四氯化硅晶体属于分子晶体,③1500℃时氯化钠的分子组成可用NaCl表示,④氯化铝晶体是典型的离子晶体,其中与表中数据一致的是:
A.只有③ B.只有①和② C.只有①②③ D.全都一致
10. 对于可逆反应中反应物的转化率的叙述中错误的是 BD
A.同一反应中,达到平衡时,各反应物的转化率不一定相等
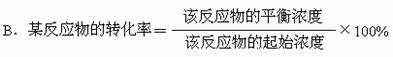
C.反应物的转化率大小可表示可逆反应进行的程度
D.在同一反应中,反应达到平衡时转化率一定大于未达到平衡时的转化率
9.铋酸钠(NaBiO3)是一种强氧化剂.NaBiO3可将MnO42-氧化为MnO4-,同时要用浓硝酸酸化,但不能用浓盐酸酸化,这是因为:
A.硝酸是氧化性酸,其参加反应有助于将MnO42-氧化为MnO4-
B.硝酸的酸性比盐酸强 C.盐酸中的Cl-能被强氧化剂BiO3-氧化
D.NO3-离子催化NaBiO3时对Mn2+有氧化作用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com