
1.线圈在匀强磁场中转动产生的交流电动势e=10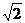 sin20πt(V),则下列说法中正确的是
sin20πt(V),则下列说法中正确的是
①t=0时,线圈平面位于中性面
②t=0时,穿过线圈的磁通量为最大
③t=0时,导线切割磁感线的有效速度最大
④t=0.4 s时,e有最大值10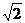 (V)
(V)
A.①② B.②③ C.③④ D.①③④
(二)选考题:共45分。请考生从给出的2道物理题.2遒化学题,2道生物题中每科任选一题作答,如果多做,则每学科按第一题计分。
35.[化学一选修3物质结构与性质](15分)
A、B、C、D、E、F六种元素的原子序数依次递增。
已知:①F的原子序数为25,其余均为短周期元素;
②元素A与元素B同周期,元素A与元素E同主族,且.A、B、E三原子p轨道上均有2个未成对电子;
③元素C、D、E在同一周期,且C原子中没有未成对电子。
请回答下列问题:
(1)元素A与元素B的电负性大小比较为 ____ > _____ ,元素C与元素D的第一电离能的大小比较为.___ _ > ______(填人相应的元素符号);
(2)F的核外电子排布式为 ,
(3)元素B与元素E形成的晶体所属的晶体类型为____晶体,在该晶体中原子间形成的共价键属于 (从下列选项中选出正确类型)
A.σ键 B.π 键 C.既有σ键,又有π键
(4)由氢元素与A、B两元素共同构成的相对分子质量为30的分子里中心原子的杂化轨道类型为_________,分子的空间构型为____________,
(5)根据等电子原理,写出由元素A与元素B构成的一种双原子极性分子的结构式___________。
36.[化学一选修5有机化学基础](15分)
已知由C、H、O三种元素组成的化合物A,其相对分子质量为60,且A能与NaHCO3反应生成CO2 。请回答下列问题:
(1)A的结构简式是_________________________ 。
(2)有机物B与A相对分子质量相同,A和B之间能发生酯化反应,生成有机物C;B烃基上的一氯取代产物有3种。C的结构简式是 ______________________
(3)有机物B在Cu作催化剂的条件下与02反应生成D,化学方程式是 。
(4)有机物E是D的氧化产物,F是E的一种同分异构体,F可发生如下图所示的转化,其中Y的分子式为C6H8O4且分子中含有一个由六个原子构成的环。
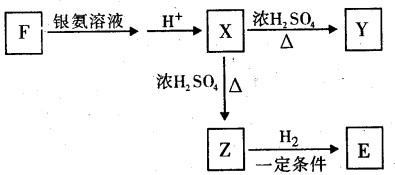
①写出F的结构简式_____________________
②写出由X生成Y的化学方程式________________________________________
③Z在一定条件下可以聚合生成高分子化合物,写出化学方程式 。
7.下列叙述正确的是( )
A.配制50g质量分数为5%KCl溶液:将45mL水加入到盛有5g KCI的烧杯中,搅拌溶解
B.鉴定SO42-向溶液中加入盐酸酸化的氯化钡溶液
C.量取液体:用50mL酸式滴定管可准确量取25.00mL 的KMnO4溶液
D.除杂质:用过量的氨水除去AICl3溶液中的少量的FeCl3
8.X、Y为短周期中的两种元素,能形成化学式X2Y3,若X的质子数为m,则Y的质子数不可能为( )
A.m+l B.m+3 C.m+ 11 D.m+6
9.能正确表示下列反应的离子方程式是( )
A.向Mg(OH)2的悬浊液中滴加FeCl3溶液:
3Mg(OH)2+2Fe3+ =2Fe( OH)3↓+ 3Mg2+
B.小苏打溶液与少量石灰水反应:HCO3-+ Ca2++ OH-= CaCO3↓ +H2O
C.单质铜与稀硝酸反应:Cu +2H+ +2NO3- =Cu2+ +2NO↑十H2O
D.氯气溶于水:Cl2+H2O=2H++ Cl-+ ClO-
10.既可以用来鉴别乙烷与乙烯,又可以用来除去 乙烷中乙烯的方法是( )
A.通过足量的NaOH溶液 B 通过足量的溴水
C.在Ni催化、加热条件下通入H2 D.通过足量的KMnO4酸性溶液
11.在一定条件下,RO3-与R-发生如下反应:RO3-+ 5R-+ 6H+ =3R2+3H2O。下列关于R元素的叙述,正确的是( )
A.R位于VA族 B.R的氢化物的水溶液是强酸
C.RO3-中的R只能被还原 D.R2在常温常压下一定是气体
12.下列叙述中正确的是( )
A.0.1moIL-1氨水中,c(OH-)=C(NH4+)
B常温下,l0mL0.02mol·L-1HCl溶液与,l0mL0.02mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH= 12
C.相同条件下,如果两种弱酸的酸性HA强于HB,则物质的量浓度相等的NaA与NaB两溶液的pH前者大于后者
D.在0.1mol·L-1Na2CO3溶液中,c(OH-)= c(H+) + C(HCO3-)+C(H2CO3)
13.等质量的CuO和MgO粉末分别溶于相同体积的硝酸中完全溶解,得到的Cu(NO3-)2和 Mg(NO3)2溶液的浓度分别为amol·L-1和bmol·L-1,则a与b的关系为( )
A.a=b B.a=2b C.2a=b D.a= 5b
第Ⅱ卷
26.(13分)我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下,发生如下反应制得:CO(g)+2H2(g)= CH3OH(g)
图I、图Ⅱ是关于该反应进行情况的图示。
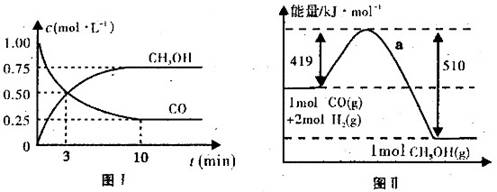
请根据图示回答下列问题:
(1)图I是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=______________________________
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b。
(3)写出该反应的热化学方程式:__________________________________________
(4)该反应的平衡常数K的表达式为_________________ ;当温度升高时,该平衡常数K将________(填“增大”、“减小”或“不变”)。
(5)恒容条件下,下列措施中能使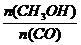 增大的有_________
增大的有_________
A.升高温度 B.充人He气
C.再充入1molCO和2molH2 D.使用催化剂
27.(15分)下列图示是学生课外活动小组设计的制取氨气并进行氨气溶于水的喷泉实验等实验的装置示意图。
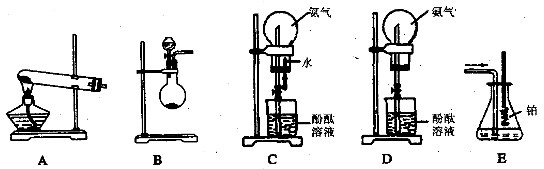
请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式______________;
制出的氨气应使用__________________ 法来收集,要得到干燥的氨气可选用 ________ 做干燥剂。
(2)学生乙用图B所示装置也制出了氨气,他选用的制取试剂可能是______ 和________。
(3)学生丙用图C所示装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是:____________________________________________________________。
(4)学生丁将装置C误装为装置D,但经同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法:________________________________
(5)学生戊用装置E吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入戊装置的锥形瓶内,看到了具有催化作用的铂丝保持红热,同时瓶内生成了红棕色的气体。写出在此过程中可能发生反应的化学方程式:_____________________________。
28.(15分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(每种电解质电离时只产生一种阳离子与阴离子,而且不重复)。
|
阳离子 |
H+ 、Na+ 、Al3+ 、Mg2+ 、Ba2+ |
|
阴离子 |
OH- 、Cl- 、CO3- 、NO3- 、SO42- |
已知:①A、B两种溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与c溶液反应只有气体产生。
③B溶液与D溶液反应时会生成两种沉淀。
试回答下列问题:
(1)写出各物质的化学式:
A. , B. _, C. ,D. .
(2)在l00mL 0.2mol.L-1 E溶液中,逐滴加入35mL 1mol·L-1B溶液,最终得到沉淀的质量为___________________ g
16.过山车是游乐场中常见的设施。下图是一种过山车的简易模型,它由水平轨道和在竖直平面内的三个圆形轨道组成,B、C、D分别是三个圆形轨道的最低点,B、C间距与C、D间距相等,半径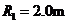 、
、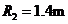 。一个质量为
。一个质量为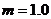 kg的小球(视为质点),从轨道的左侧A点以
kg的小球(视为质点),从轨道的左侧A点以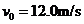 的初速度沿轨道向右运动,A、B间距
的初速度沿轨道向右运动,A、B间距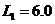 m。小球与水平轨道间的动摩擦因数
m。小球与水平轨道间的动摩擦因数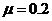 ,圆形轨道是光滑的。假设水平轨道足够长,圆形轨道间不相互重叠。重力加速度取
,圆形轨道是光滑的。假设水平轨道足够长,圆形轨道间不相互重叠。重力加速度取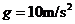 ,计算结果保留小数点后一位数字
,计算结果保留小数点后一位数字 试求
试求
(1)小球在经过第一个圆形轨道的最高点时,轨道对小球作用力的大小;
(2)如果小球恰能通过第二圆形轨道,B、C间距 应是多少;
应是多少;
(3)在满足(2)的条件下,如果要使小球不能脱离轨道,在第三个圆形轨道的设计中,半径 应满足的条件;小球最终停留点与起点
应满足的条件;小球最终停留点与起点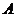 的距离。
的距离。

15. 2008年12月,天文学家们通过观测的数据确认了银河系中央的黑洞“人马座A*”的质量与太阳质量的倍数关系。研究发现,有一星体S2绕人马座A*做椭圆运动,其轨道半长轴为9.50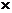 102天文单位(地球公转轨道的半径为一个天文单位),人马座A*就处在该椭圆的一个焦点上。观测得到S2星的运行周期为15.2年。
102天文单位(地球公转轨道的半径为一个天文单位),人马座A*就处在该椭圆的一个焦点上。观测得到S2星的运行周期为15.2年。
(1)
若将S2星的运行轨道视为半径r=9.50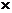 102天文单位的圆轨道,试估算人马座A*的质量MA是太阳质量Ms的多少倍(结果保留一位有效数字);
102天文单位的圆轨道,试估算人马座A*的质量MA是太阳质量Ms的多少倍(结果保留一位有效数字);
(2)
黑洞的第二宇宙速度极大,处于黑洞表面的粒子即使以光速运动,其具有的动能也不足以克服黑洞对它的引力束缚。由于引力的作用,黑洞表面处质量为m的粒子具有势能为Ep=-G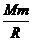 (设粒子在离黑洞无限远处的势能为零),式中M、R分别表示黑洞的质量和半径。已知引力常量G=6.7
(设粒子在离黑洞无限远处的势能为零),式中M、R分别表示黑洞的质量和半径。已知引力常量G=6.7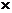 10-11N·m2/kg2,光速c=3.0
10-11N·m2/kg2,光速c=3.0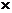 108m/s,太阳质量Ms=2.0
108m/s,太阳质量Ms=2.0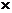 1030kg,太阳半径Rs=7.0
1030kg,太阳半径Rs=7.0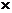 108m,不考虑相对论效应,利用上问结果,在经典力学范围内求人马座A*的半径RA与太阳半径
108m,不考虑相对论效应,利用上问结果,在经典力学范围内求人马座A*的半径RA与太阳半径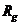 之比应小于多少(结果按四舍五入保留整数)。
之比应小于多少(结果按四舍五入保留整数)。
14.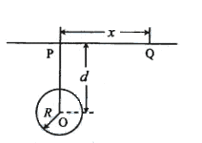 如图,P、Q为某地区水平地面上的两点,在P点正下方一球形区域内储藏有石油,假定区域周围岩石均匀分布,密度为
如图,P、Q为某地区水平地面上的两点,在P点正下方一球形区域内储藏有石油,假定区域周围岩石均匀分布,密度为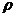 ;石油密度远小于
;石油密度远小于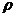 ,可将上述球形区域视为空腔。如果没有这一空腔,则该地区重力加速度(正常值)沿竖直方向;当存在空腔时,该地区重力加速度的大小和方向会与正常情况有微小偏高。重力加速度在原坚直方向(即PO方向)上的投影相对于正常值的偏离叫做“重力加速度反常”。为了探寻石油区域的位置和石油储量,常利用P点附近重力加速度反常现象。已知引力常数为G。
,可将上述球形区域视为空腔。如果没有这一空腔,则该地区重力加速度(正常值)沿竖直方向;当存在空腔时,该地区重力加速度的大小和方向会与正常情况有微小偏高。重力加速度在原坚直方向(即PO方向)上的投影相对于正常值的偏离叫做“重力加速度反常”。为了探寻石油区域的位置和石油储量,常利用P点附近重力加速度反常现象。已知引力常数为G。
(1)设球形空腔体积为V,球心深度为d(远小于地球半径),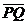 =x,求空腔所引起的Q点处的重力加速度反常
=x,求空腔所引起的Q点处的重力加速度反常
(2)若在水平地面上半径L的范围内发现:重力加速度反常值在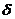 与
与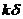 (k>1)之间变化,且重力加速度反常的最大值出现在半为L的范围的中心,如果这种反常是由于地下存在某一球形空腔造成的,试求此球形空腔球心的深度和空腔的体积。
(k>1)之间变化,且重力加速度反常的最大值出现在半为L的范围的中心,如果这种反常是由于地下存在某一球形空腔造成的,试求此球形空腔球心的深度和空腔的体积。
13. “嫦娥一号”月球探测器在环绕月球运行过程中,设探测器运行的轨道半径为r,运行速率为v,当探测器在飞越月球上一些环形山中的质量密集区上空时 (
)
(
)
A.r、v都将略为减小 B.r、v都将保持不变
C.r将略为减小,v将略为增大 D. r将略为增大,v将略为减小
12. 为纪念伽利略将望远镜用于天文观测400周年, 2009年被定为以“探索我的宇宙”为主题的国际天文年.我国发射的“嫦娥一号”卫星绕月球经过一年多的运行,完成了既定任务,于2009年3月1日16时13分成功撞月.如图为“嫦娥一号”卫星撞月的模拟图,卫星在控制点1开始进入撞月轨道.假设卫星绕月球作圆周运动的轨道半径为R,周期为T,引力常量为G.根据题中信息,以下说法正确的是
 A.可以求出月球的质量
A.可以求出月球的质量
B.可以求出月球对“嫦娥一号”卫星的引力
C.“嫦娥一号”卫星在控制点1处应减速
D.“嫦娥一号”在地面的发射速度大于11.2km/s
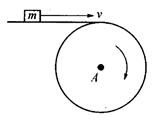
11. m为在水平传送带上被传送的小物体(可视为质点),A为终端皮带轮,如图所示,已知皮带轮半径为r,传送带与皮带轮间不会打滑。当m可被水平抛出时,A轮每秒的转数最少是 ( )
 A.
A.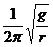 B.
B.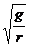
C. D.
D.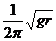
10.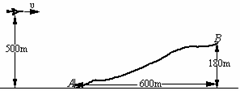 如图所示,一架在500 m高空以200 m/s的速度水平匀速飞行的轰炸机,要用两枚炸弹分别炸山脚和山顶的目标A和B。已知山高 180 m,山脚与山顶的水平距离为600 m, 若不计空气阻力,g 取10 m/s2,则投弹的时间间隔应为( )
如图所示,一架在500 m高空以200 m/s的速度水平匀速飞行的轰炸机,要用两枚炸弹分别炸山脚和山顶的目标A和B。已知山高 180 m,山脚与山顶的水平距离为600 m, 若不计空气阻力,g 取10 m/s2,则投弹的时间间隔应为( )
 A.6 S
A.6 S
 B.5 S
B.5 S
 C.3 S
C.3 S
D.2 S
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com