
19.已知A、B均是由两种元素组成的化合物,且A、B中均有某种元素质量分数为75%,C、J是同周期元素的气态氢化物,X为无色液体。反应生成的水均已略去。它们有如下图所示的关系。
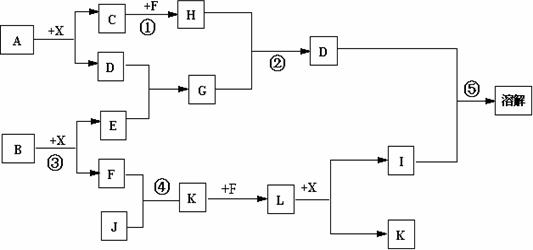
(1)写出化学式:A B J 。
(2)反应③中每生成1molF,转移电子的数目为: 。
(3)反应④的化学方程式为: 。
(4)写出离子方程式分别为:
反应② ;⑤ 。
(5)反应①中,每1.00g C与足量的F作用,恢复到25℃放出55.6kJ热量,写出反应①的热化学方程式 。
18.(8分)高纯超净特种气体主要用于制造半导体器件、化合物半导体、激光器、光导纤维、太阳能电池等。超纯硅化氢制备方法如下:(已知:常温下SiH4难溶于水,与稀硫酸不反应,乙醚沸点34.6℃)
①由下列两种方法制得SiH4
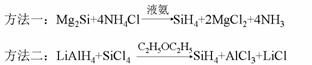
②除去SiH4中混有的杂质气体
请回答下列问题:
⑴对方法一的理解,有同学认为是NH4+水解产生H+,Mg2Si与H+反应生成SiH4,你认为该观点是否正确?并简述理由________________。
⑵将方法二的固体产物溶于水,只有一种物质能促进水的电离,则NaOH、Mg(OH)2、LiOH碱性由强到弱的顺序为_________________。
⑶两种方法制得的SiH4中均含有少量杂质,有同学提出用下列方法除去SiH4中的杂质,其中肯定不可行是____________。
a.用稀硫酸洗气 b. 高温使杂质分解 c.低温分馏
⑷甲、乙、丙三同学在讨论SiH4制备方法的化学反应类型时发表如下观点,你认为正确的是__________。
a.甲同学认为两个反应均为氧化还原反应
b.乙同学认为两个反应中只有一个属于氧化还原反应
c.丙同学认为要判断是否属于氧化还原反应,还需要知道SiH4中各元素具体的化合价
17. 按要求回答下列问题:(每空1分)
(1)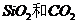 在物理性质上(如熔点、硬度)上有很大差别,这是由于________________________________。
在物理性质上(如熔点、硬度)上有很大差别,这是由于________________________________。
(2)盛烧碱溶液的试剂瓶不能用玻璃塞这是因为_______________________________。
(3)将下列天然硅酸盐改写成氧化物的形式:
(1)绿柱石  ________________(2)白云母
________________(2)白云母 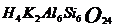 ________________
________________
(3)翡翠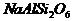 ________________
________________
|
1 |
|
2 |
|
3 |
|
4 |
|
5 |
|
6 |
|
7 |
|
8 |
|
|
9 |
|
10 |
|
11 |
|
12 |
|
13 |
 |
14 |
|
15 |
|
16 |
|
16.下列关于Na2CO3和NaHCO3的叙述中错误的是o. ( )m
A.等质量的两种盐分别与足量的盐酸反应,在相同情况下Na2CO3产生的二氧化碳多
B.等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同情况下产生的二氧化碳体积相等
C.等物质的量的Na2CO3和NaHCO3分别与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3消耗盐酸提及的2倍
D.将石灰水加入NaHCO3溶液中不产生白色沉淀,加入Na2CO3溶液中则产生白色沉
南城一中高三年碳族元素及无机非金属材料试题
班级 姓名
15.已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是 w.w.w.k.s.5.u.c.o.
( )m
w.w.w.k.s.5.u.c.o.
( )m
A.碳的燃烧热大于110.5kJ/mol
B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
14.能正确表示下列反应的离子方程式是 ( )
A.醋酸钠的水解反应CH3COO-+H3O+=CH3COOH+H2O
B.碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
C.苯酚钠溶液与二氧化碳反应C6H5O-+CO2+H2O=C6H5OH+CO32-
D.稀硝酸与过量的铁屑反应3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O
13.对下列反应①KHCO3溶液与石灰水反应、②Na2SO3溶液与稀盐酸反应、③Si与烧碱溶液反应、④Fe与稀硝酸反应,改变反应物用量,不能用同一个离子方程式表示的是 ( )
A.①②③ B.①②④ C.①③④ D.②③④
12.对相同状况下的12C18O和14N2两种气体,下列说法正确的是 ( )
A.若质量相等,则质子数相等 B.若原子数相等,则中子数相等
C.若分子数相等,则体积相等 D.若体积相等,则密度相等
11.向某密闭容器中充入1molCO和2molH2O(g),发生反应:CO+H2O (g) =CO2 +H2。
当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是 ( )w.w
A.0.5molCO+2molH2O(g)+1molCO2+1molH2 B.1molCO+1molH2O(g)+1molCO2+1molH2 .
C.0.5molCO+1.5molH2O(g)+0.4molCO2+0.4molH2
D.0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com