
16.有3份等质量的小苏打,第1份直接与过量盐酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应。假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是
A.V1>V2>V3 B. V1>V3>V2 C. V2>V3>V1 D. V1=V2=V3
15.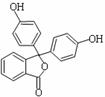 药物可以预防、诊断和治疗疾病,而中学化学中不少常用化学试剂本身就具
药物可以预防、诊断和治疗疾病,而中学化学中不少常用化学试剂本身就具
有药物的功效,如酚酞医药名为果桃, 酚酞含片是一种治疗消化系统疾病的药物,其有效成分的结构简式如图所示。 下列对该有效成分的说法正确的是
下列对该有效成分的说法正确的是
A.所有原子可能共平面
B.酚酞的水解产物中含有醇羟基
C.能发生加聚反应生成高分子化合物
D.1 mol该物质最多能与含4 molNaOH的烧碱溶液反应
14.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。
下列事实不能说明上述观点的是:
A.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B.甲苯能使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色
C.乙烯能发生加成反应,乙烷不能发生加成反应
D.苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
13.常温下将NaOH溶液与CH3COOH稀溶液混合,不可能出现的结果是
A. pH=7且c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
B. pH<7且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
C.pH>7且c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
D.pH>7且c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
12.2008年9月开始陆续有多个品牌的奶粉被检出含有危害人体的三聚氰胺,这就是轰动全国的“问题奶粉事件”。三聚氰胺的制备反应为:6CO(NH2)2[尿素]硅胶380~400℃C3N6H6+ 6NH3+3CO2。三聚氰胺和甲醛在一定条件可下制备三聚氰胺甲醛树脂。
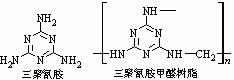 下列说法中不正确的是
下列说法中不正确的是
A.三聚氰胺与盐酸和硫酸等能形成三聚氰胺盐
B.三聚氰胺含氮的质量分数高于尿素
C.三聚氰胺分子中所有的氮原子化学环境均相同
D.三聚氰胺甲醛树脂是一种高分子材料
11.普通锌锰干电池的简图(如右下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:
Zn+2NH4++2MnO2=[Zn(NH3)2]2++Mn2O3+H2O
关于锌锰干电池的下列说法中正确的是
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池正极的电极反应式为:
2MnO2+2NH4++2e- == Mn2O3+2NH3+H2O
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5g
10. 将氨水滴加到盛有AgCl浊液的试管中,AgCl逐渐溶解,再加入NaBr溶液又产生了浅黄色沉淀。对上述过程,下列理解或解释中正确的是
A.Ksp(AgCl)<Ksp(AgBr)
B.若在AgCl浊液中直接加入NaBr溶液,也会产生浅黄色沉淀
C.上述实验说明AgCl没有NaBr稳定
 D.因为Ksp(AgCl)>Ksp(AgOH),故氨水能使AgCl溶解
D.因为Ksp(AgCl)>Ksp(AgOH),故氨水能使AgCl溶解
9. 用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,22.4L己烷中共价键数目为19NA
B.0.1mol Fe与足量硫粉充分反应,转移的电子数为0.3 NA
C.1mol/L的Na2CO3溶液中含有NA个CO2- 3
D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
8. 世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成生石灰;②在海水中加入生石灰,过滤,洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中加热晶体;⑤电解上述所得盐(熔融条件下)。 下列说法正确的是
下列说法正确的是
A.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
B. 上述变化过程中包括了分解、化合、复分解、置换等四种反应类型
C.在氯化氢热气流中干燥晶体的目的是为了加快干燥速度
D.步骤⑤也可以采用电解该盐水溶液的方法
7.下列实验操作或描述中错误的是
A.将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
B.溶剂蒸发的速度越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大
C.海带中碘元素的分离及检验时,需要向海带灰的浸取液中,加入少量稀硫酸和过氧化氢溶液
D.纸层析法分离铁离子和铜离子实验中,点样后的滤纸需晾干后,才能将其浸入展开剂中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com