
34.(15分)下图表示夏季晴朗无云的某天,温室中某种C3植物二氧化碳吸收和释放速率变化曲线,请据图回答问题:

①在24小时内,植物光合作用强度和呼吸作用强度相等的是__________点所对应时刻.
②在24小时内,植物内积累有机物速度最快的是__________点所对应时刻.
③在一天内,植物积累有机物量等于__________.(用图形面积表示,如SOABC)
④一天中,叶肉细胞叶绿体中C5含量最高的是图中的__________点所对应的时刻.此时,如果采取____________________措施,既可提高光合产量,又可降低C5含量.分别于E、G两点对应的时刻,取该植物相同部位的叶片制切片,经碘液染色,观察叶肉细胞的颜色.上述操作的缺陷是____________________.经改进,实验结果是E点比G点颜色__________(深、浅)。
⑤让光照下的玉米植株处在含适宜浓度的14CO2的环境中,14C在C3、C4、C5中出现的先后顺序是__________(用箭头表示)。
长葛市第三实验高中2009-2010学年第七次考试
33.(8分)蛙的发育为变态发育,其幼体蝌蚪有尾.为了研究甲状腺激素对蝌蚪生长发育的影响,某人做了如下实验:
①将15只同种并同时孵化的蝌蚪等分成三组,分别放在3个盛有2000mL提前晾晒3天的自来水和适量金鱼藻的烧杯中,分别标号甲、乙、丙.
 ②向甲烧杯中加入5毫克甲状腺激素,向乙烧杯中加入2.5毫克甲状腺激素,连续投药7天,每天一次,药量相同,丙中不投药作对照.
②向甲烧杯中加入5毫克甲状腺激素,向乙烧杯中加入2.5毫克甲状腺激素,连续投药7天,每天一次,药量相同,丙中不投药作对照.
③三组放在相同的适宜的环境中培养,每天按要求换水和喂食.
④每天测量蝌蚪身体的长度,并记录实验结果,绘制成曲线,如图.
回答下列问题:
(1)请指出曲线A、C分别为哪组实验的结果A:__________ C:__________
(2)曲线B绘制不完整,请补充完整.
(3)碘是合成甲状腺激素的原料,人类饮食缺碘导致甲状腺增生.请从激素的关系和作用角度简要解释_______________________________________________.
(4)甲状腺激素分泌过多,人的体温将升高,原因是____________________.另举一例能促进体温升高的激素__________.
32.(10分)下图是人体肝细胞中三大营养物质代谢部分途径示意图,回答相关问题.箭头及其旁边的数字代表过程.
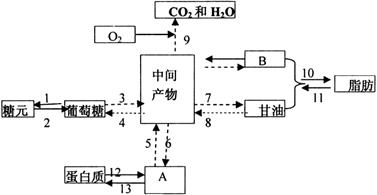
(1)图中字母代表的物质是A__________,B__________.
(2)图中能使细胞中ADP含量降低的过程是____________________(填标号).
(3)图中过程可能涉及到的细胞器除溶酶体外还有____________________.
(4)人体中糖类等其它有机物不能转化成赖氨酸,是因为__________________,由过程__________(填标号)可以得到赖氨酸,人体每天必须摄入一定量的蛋白质除与上述原因有关外还与过程__________(填三个标号)直接有关.
(5)正常人摄入商糖食物容易发胖,是因为__________分泌量增加,促进过多血糖__________,从而导致肥胖。
31.(9分)为了检测饮用水中是否含有大肠杆菌,培养基的配方如下表:
|
蛋白胨 |
乳糖 |
蔗糖 |
K2HPO4 |
蒸馏水 |
|
10g |
5g |
5g |
2g |
1000mL |
(1)表中漏掉的物质是____________________,根据培养基的物理性质,该培养基应为____________________.
(2)该培养基所含的碳源有____________________,其功能是_______________.配制培养基时,必须注意各种营养物质的__________和__________.
(3)不论何种培养基,在各种成分都溶化后分装前,要进行的是_______________
(4)当大肠杆菌体内某代谢产物X含量过高时,X会与酶Y结合,导致Y的结构__________变化,Y的活性降低.人工控制微生物代谢的措施包括改变微生物的遗传特性、__________等
30.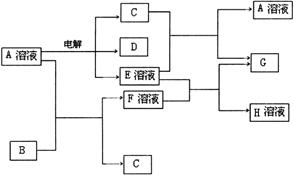 (14分)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如下图(部分反应产物已略去).
(14分)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如下图(部分反应产物已略去).
请回答下列问题:
(1)A的化学式为______________.
(2)A溶液与Na2O2反应的总化学方程式为______________________________.
(3)E的稀溶液与F溶液反应的离子方程式为_____________________________.
(4)电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为__________.(假设溶液体积不变)
(5)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体C.则滤液中溶质的物质的量浓度为__________.(假设溶液体积不变)
29. (16分)实验室制NO及验证NO的性质,可以用如图所示的装置。请根据提示完成以下问题。
(16分)实验室制NO及验证NO的性质,可以用如图所示的装置。请根据提示完成以下问题。 已知反应:2NaOH+2NO2=NaNO3+NaNO2+H2O 2NaOH+NO+NO2=2NaNO2+H2O
已知反应:2NaOH+2NO2=NaNO3+NaNO2+H2O 2NaOH+NO+NO2=2NaNO2+H2O
 I.NO的制备
I.NO的制备
 (1)在加药品之前首先应进行的操作是
(1)在加药品之前首先应进行的操作是
(填操作名称);
 (2)打开阀门K,取下活塞J向其中加入一小片铜片,装上活塞并推至底部;
(2)打开阀门K,取下活塞J向其中加入一小片铜片,装上活塞并推至底部;
 (3)用注射器吸取适量的蒸馏水,然后倒立针筒,推动活塞J至底部以排尽装置内的空气(装置内极少量的水不影响实验);
(3)用注射器吸取适量的蒸馏水,然后倒立针筒,推动活塞J至底部以排尽装置内的空气(装置内极少量的水不影响实验);
 (4)将注射器插入稀HNO3中,吸取适量的稀HNO3,然后迅速关闭阀门K,请回答此时可能观察到的实验现象:
___________,反应的离子方程式为:
,当注射器活塞上升到某一位置时,迅速打开阀门K,将反应液推入NaOH溶液中后关闭K。
(4)将注射器插入稀HNO3中,吸取适量的稀HNO3,然后迅速关闭阀门K,请回答此时可能观察到的实验现象:
___________,反应的离子方程式为:
,当注射器活塞上升到某一位置时,迅速打开阀门K,将反应液推入NaOH溶液中后关闭K。
 Ⅱ.NO性质实验
Ⅱ.NO性质实验
 (1)观察注射器内气体呈 色,然后打开K,吸取适量空气后关闭K,此时注射器内气体呈 色,反应的化学方程式为: 。
(1)观察注射器内气体呈 色,然后打开K,吸取适量空气后关闭K,此时注射器内气体呈 色,反应的化学方程式为: 。
 (2)向下快速推动活塞J,注射器内气体颜色变化情况为
(2)向下快速推动活塞J,注射器内气体颜色变化情况为 :
,原因是:__________________________________________________________
:
,原因是:__________________________________________________________
______ ________________ (结合化学方程式并配以必要的文字说明)。
 III.尾气处理
III.尾气处理
 若原注射器内NO的体积为20 mL,则至少应抽入 mL相同状况下的空气,才能保证NO完全被NaOH溶液吸收(假设空气中氧气的体积分数为20%)
若原注射器内NO的体积为20 mL,则至少应抽入 mL相同状况下的空气,才能保证NO完全被NaOH溶液吸收(假设空气中氧气的体积分数为20%)
28.(16分)某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色:J分子内有两个互为对位的取代基.在一定条件下有如下的转化关系:(无机物略去)
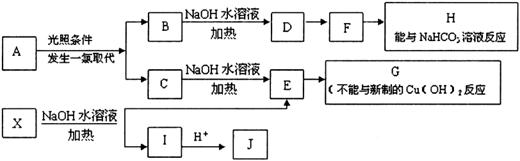
(1)属于芳香烃类的A的同分异构体中,其沸点的大小关系为________________.(不包括A,用结构简式表示)
(2)J中所含的含氧官能团的名称为____________________.
(3)E与H反应的化学方程式是____________________;反应类型是__________.
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是__________.
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式.
①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种.________________________________________
27.(14分)A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中A、D及C、F分别是同一主族元素,A、F两元素的原子核中质子数之和比C、D两元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍.又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数.请回答:
(1)1mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物发生反应,完全反应后消耗后者的物质的量为__________.
(2)A、C、F间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为__________.
(3)单质B的燃烧热a kJ/mol.由B、C二种元素组成的化合物BC14g完全燃烧放出b kJ热量,写出单质B和单质C反应生成BC的热化学方程式:____________.
(4)工业上在高温的条件下,可以用A2C和BC反应制取单质A2.在等体积的Ⅰ、Ⅱ两个密闭容器中分别充入1mol A2C和1mol BC、2mol A2C和2mol BC.一定条件下,充分反应后分别达到平衡(两容器温度相等).下列说法正确的是__________
A.达到平衡所需要的时间:Ⅰ>Ⅱ
B.达到平衡后A2C的转化率:Ⅰ=Ⅱ
C.达到平衡后BC的物质的量:Ⅰ>Ⅱ
D.达到平衡后A2的体积分数:Ⅰ<Ⅱ
E.达到平衡后吸收或放出的热量:Ⅰ=Ⅱ
F.达到平衡后体系的平均相对分子质量:Ⅰ<Ⅱ
(5)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成的化合物的溶液中构成电池,则电池负极的电极反应式是_______________.
26.(20分)如图1所示,为利用光敏电阻检测传送带上物品分布从而了解生产线运行是否运行正常的仪器.其中A是发光仪器,B是一端留有小孔用绝缘材料封装的光敏电阻.当传送带上没有物品挡住由A射向B的光信号时,光敏电阻阻值为R1=50Ω;当传送带上有物品挡住由A射向B的光信号时,光敏电阻阻值为R2=150Ω.固定电阻R3=45Ω.C为平行板电容器,虚线与两极板距离相等,极板长L1=8.0×10-2m,两极板的间距d=1.0×10-2m.D为屏,与极板垂直,D到极板的距离L2=0.16m,屏上贴有用特殊材料做成的记录纸,当电子打在记录纸上时会留下黑点,工作时屏沿图示方向匀速运动.有一细电子束沿图中虚线以速度v0=8.0×106m/s连续不断地射入电容C,v0延长线与屏交点为O.图2为一段记录纸.已知电子电量e=1.6×10-19C,电子质量m=9×10-31kg.忽略细光束的宽度、电容器的充电放电时间及电子所受的重力.求:电源的电动势E和内阻r.


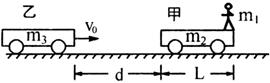
25.(18分)如图所示,质量为m1=50kg的某学生(可视为质点)站在长为L=3m、质量为m2=100kg的甲车右端,人和车均处于静止状态,地面水平光滑.一质量为m3=100kg的乙车以速度v0=3m/s向右运动.当该学生发现乙车时,两车距离为d=5m,该学生马上在甲车上向左匀加速跑动,跑到甲车车尾后从甲车跳到乙车上,假设该生跳到乙车后马上相对乙车静止.求:
(1)为了避免在学生从甲车跳出前两车相碰,该学生跑动时加速度a1至少为多少?
(2)要使两车不相碰,该学生跑动时加速度a2至少为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com