
29.(8分)
将2.3g金属钠投入足量水中,反应后溶液总体积为100mL。求:
(1)所得气体在标准状况下的体积为 L。
(2)反应后所得溶液溶质的物质的量浓度是多少?(此问写出计算过程)
28.(8分)
A、B、C、D、E、F、G各物质问的转化关系如下图所示:

已知:A为纯净物,C可使带火星的木条复燃,B、C、E为单质,G中滴入KSCN溶液早血红色。根据以上信息完成下列问题:
(1)图示①为多步反应,在该转变过程中,涉及到A与NaOH溶液的反应,该反应的化学方程式为: 。
(2)反应②能放出大量的热,用于焊接铁轨,工业上常将这类反应称为 。
(3)写出反应③的离子方程式 。
(4)写出G中溶质的电离方程式 。
27.(9分)
已知: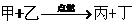 ,其中甲为金属元素单质,丙为固态非金属单质,乙是造成温窒效应的罪魁祸首。根据以上信息回答下列问题:
,其中甲为金属元素单质,丙为固态非金属单质,乙是造成温窒效应的罪魁祸首。根据以上信息回答下列问题:
(1)乙的化学式为 ,丙原子的结构示意图为
(2)工业上制取甲的化学方程式为
(3)将过量的乙通入NaAlO2溶液中,反应的离子方程式为
(4)丙与浓硫酸反应的化学方程式为
(5)写出丁在工业上的用途(只答一点用途即可)
26.(11分)
甲同学采用如图I所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体。
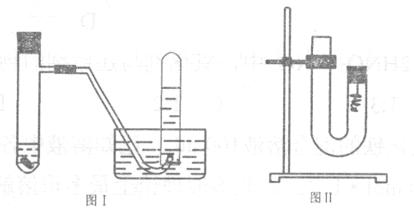
(1)反应过程中的实验现象是:①铜片逐渐溶解,铜片表面有气泡产生;②溶液由无色变成 色;③反应前具支试管内气体为无色,反应开始后气体由无色变成 色,一段时间后又变成 色;④小试管内收集到无色气体。
(2)上述变化过程中,涉及到的化学反应有三个,写出化学反应方程式
① ;② ;
③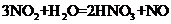 。
。
(3)乙同学用如图II所示装置进行实验,其过程如下:
①从U形管左端加入稀硝酸,直至 ,迅速用附有铜丝的胶塞塞住U形管右端,观察到的现象是:铜丝表面有气泡生成,U形管右端液面
,左端液面 ,并在右端上部有一段无色气体。
②待反应停止后,将U形管左端液体吸出一部分使之与右端液面相平,打开胶塞,观察到的现象是 。
通过以上实验,甲、乙两同学均得到了正确结论。
25.(8分)
实验室需要;480 mL 0.200 mol•L-1的Na2CO3溶液。现用Na2CO3固体配制,可供选择的仪器有:
①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤漏斗 ⑥天平 ⑦药匙 ⑧500rnL容量瓶 ⑨250mL容量瓶。请同答下列问题:
(1)上述仪器中,在配制Na2CO3溶液时必须使用的仪器除①、③、⑥、⑦外,还有
(填数字序号)。
(2)经计算,需Na2CO3固体的质量为 。
(3)将所配制的Na2CO3溶液进行测定,发现浓度小于0.200mol·L-1。请你分析配制过程中可能引起该误差的原因是(填字母代号) 。
A.定容时俯视液面 B.转移时没有洗涤烧杯和玻璃棒
C.配制时容量瓶不干燥
(4)将配好的溶液盛装于下列(填字母代号) 仪器中,贴好标签备用。
A.带玻璃塞的广口瓶 B.带玻璃塞的细口瓶
C.带胶塞的广口瓶 D.带胶塞的细口瓶
24.一定量铜投入到100mL10 mol·L-1的浓HNO3中,一段时间后硝酸恰好完全反应。若硝酸的还原产物只有NO、NO2两种气体,其标准状况下总体积为6 72L。则参加反应的铜的物质的量为
A 0. 35mnl B.0.7mol C.0. 3mol D 0.5mol
卷II(非选择题,共52分)
23.有盐酸、氯化亚铁、氯化铁的混合溶液100mL,已知溶液中各阳离子的物质的量浓度相等,氯离子的浓度为6.00mol·L-1则此溶液理论上最多可溶解铁粉的质量为
A.11.2g B.2.8g C.8.4g D.5.6g
22.在反应3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的物质的量之比为
A.3:1 B.1:3 C 1:2 D.2:1
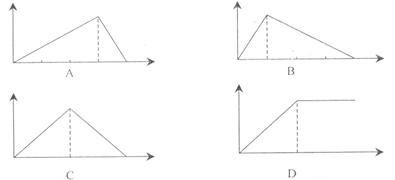
21.向AlCl3溶液中逐滴加入NaOH溶液,下列图像变化趋势正确的是
(纵坐标表示沉淀的质量,横坐标表示NaOH溶液的体积)
20.下列实验中体现浓硫酸脱水性的是
A.浓硫酸置于空气中质量增加
B.常温下,Fe、A l遇浓硫酸钝化
C.用浓硫酸作干燥剂,干燥H2、C12等气体
D.蔗糖中加入浓硫酸变黑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com