
27.(6分)(1)在下面元素周期表中全部是金属元素的区域为 。
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等
① 用元素符号将甲、乙两元素填写在下面元素周期表中对应的位置。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
② 甲、乙两元素相比较,金属性较强的是 (填化学式),可以验证该结论的实验是
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
福建省厦门六中09-10学年高一下学期3月考试
26.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
|
实验步骤 |
实验现象 |
|
①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
|
②向新制得的Na2S溶液中满加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
③将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体. |
|
④将镁条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
|
⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
|
⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。(16分)
(1)实验目的:研究 元素性质递变规律
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器:① ,② ,③ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等
(3)实验内容:(填写与实验步骤对应的实验现象的编号)
|
实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
|
实验现象(填A-F) |
|
|
|
|
|
|
步骤①的化学方程式: ,
步骤②的离子方程式 ,
此实验的结论: 。
25.短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:(18分)(1)元素名称: A B C D
(2)E的原子结构示意图:___________________________;
E在周期表中的位置: __________________________________
(3)F离子的符号:_________________ F离子结构示意图: __________________
(4)A、B组成的最简单化合物的名称是___________。
(5)写出BC2与过量氢氧化钠反应的离子方程式
(6)C单质与D单质发生反应的产物有_______________________(填化学式)。
C、D组成的一种化合物与水发生化合反应的化学方程式为:
_______________________________________________________________________
(7)能说明E的非金属性比F的非金属性____(填“强”或“弱”)的事实是:
___________________________________________________________ (举一例)。
24.按要求填空(13分) 在原子序数1-18号元素中:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质的化学式是_____________。
(3)气态氢化物最稳定的化学式是_____________。
(4)最高价氧化物对应的水化物中,碱性最强的化学式是_____________;酸性最强的化学式是_____________
(5)电子数为10的四原子分子
(6)14号原子的结构示意图为:____________________________
写出该元素最高价氧化物与氢氧化钠溶液反应的化学方程式:
________________________________________________________________________
(7)写出13号元素单质与氢氧化钠溶液反应的化学方程式:
________________________________________________________________________
13号元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式:
________________________________________________________________________
23.画出下列元素的原子结构示意图(3分)
(1)原子核外有2个电子层,核外有10个电子的原子
(2)质量数为23,中子数为12的原子
(3)最外层电子数是次外层电子数3倍的原子
22.W、X、Y、Z 4种短周期元素在元素周期表中的位置如右图所示,其中Z位于ⅦA族。下列判断错误的是 ( )
A.常压下四种元素的单质中,W单质的熔点最高
 B.Z的阴离子电子层结构与氩原子的相同
B.Z的阴离子电子层结构与氩原子的相同
C.W的氢化物的沸点比Y的氢化物的沸点高
D.Y元素的非金属性比X元素的非金属性强
Ⅱ卷(非选择题,21-25五大题,共56分)
21.下列叙述中能肯定说明金属A比金属B的活泼性强的是 ( )
A.A原子最外层电子数比B原子的最外层电子数少
B.A原子电子层数比B原子的电子层数多
C.1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多
D.常温时,A能从酸中置换出氢,而B不能
20.已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是 ( )
A.原子半径:A>B>D>C B. 原子序数:d>c>b>a
C. 离子半径:C2->D->B+>A2+ D. 原子的最外层电子数目:A>B>D>C
19.下列各组单质中,前者能将后者从化合物中置换出来的是 ( )
① ②
② ③
③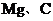 ④
④
A.只有①③ B.只有②④ C.①②③④ D.只有①②④
18.短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是( )
 A. X、Y、Z三种元素中,X的非金属性最强
A. X、Y、Z三种元素中,X的非金属性最强
B. Y的氢化物的稳定性比Z的氢化物弱
C. Y的最高正化合价为+7
D. X的单质的熔点比Z的低
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com